|
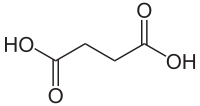
Бурштинова кислота
Буршти́нова кислота́, янта́рна кислота́, сукцина́т (бутандіова кислота, етан-1,2-дикарбонова кислота) НООССН2СН2СООН — органічна двохосновна насичена карбонова кислота. Загальні відомостіВперше була отримана у XVII сторіччі з бурштину (лат. succinum — бурштин). Подробиці відкриття історією не збережено, не відомо навіть, хто був автором її відкриття.[1] В незначних кількостях міститься у бурому вугіллі та смолах. Виявлена в бурштині, багатьох рослинах (у недозрілих ягодах аґрусу, стеблах ревеню, винограді[2] і маку[2]), в бурому вугіллі тощо[3]. Із 32 різновидів бурштину, лише декілька видів містять вільну бурштинову кислоту.[1] В смолі сучасних хвойних дерев в більшості випадків зовсім не міститься бурштинової смоли, і лише в зовсім невеликій кількості видів міститься в концентрації 0,1 %, коли в бурштині її до 4,5 %.[1] Кристали бурштинової кислоти після опромінення короткохвильовим ультрафіолетом здатні люмінесціювати, випромінюючи видиме світло.[1] Є проміжним продуктом циклу трикарбонових кислот. Сукцинат є важливим проміжним продуктом обміну живих організмів, бере участь у процесах клітинного дихання (цикл трикарбонових кислот). Утворення в смолахВважається, що бурштинова смола утворилась як результат автоокислення, якому піддавались смоли в морських розсипах, причому не усіх, а лише в розсипах, які містять мінерал глауконіт (водний алюмосилікат заліза).[1] ВластивостіЧиста кислота являє собою безбарвні кристали. Тверда речовина. Розчинна у воді та спирті, погано в ефірі, нерозчинна у бензолі, бензині, хлороформі. Метиленові групи бурштинової кислоти мають високу реакційну здатність завдяки впливу карбоксильних груп. Оскільки вона має два карбоксили — вона утворює два ряди солей (кислі і середні — зазвичай ці солі називають сукцинатами, від латинської назви бурштинової кислоти), два ряди складних ефірів, два ряди амідів і т. д.[1] Легко вступає у реакцію Фріделя—Крафтса з ароматичними сполуками, утворюючи похідні 4-арил-4-кетомасляної кислоти. При нагріванні, втрачає молекулу води, перетворюючись в циклічний ангідрид, який, будучи розчинений у воді, повільно перетворюється знову в кислоту.[1] ОтриманняУ промисловості її отримують гідруванням малеїнового ангідриду або фумарової кислоти. Бурштинова кислота може бути отримана в результаті багатьох хімічних синтезів, із акрилової кислоти, акролеїна, етилену, ацетилену; шляхом окислення природної сировини (вугілля, сланці, торф, різні нафтові фракції) або таких органічних з'єднань, як оцтовий альдегід, фурфурол, бутиролактон; до цього результату може призвести відновлення малонової або фумарової кислоти.[1] Промисловий синтез бурштинової кислоти майже у всіх країнах заснований на реакціях відновлення.[1] В Радянському союзі синтетичну бурштинову кислоту вперше почали випускати з 1966 року на Єреванському заводі хімічних реактивів.[1] Отримання з бурштинуБурштинову кислоту можна отримати — шляхом сухої перегонки зплавлених і зпресованих обрізків та крихти бурштину (звісно, не придатних для виготовлення художніх виробів).[2][1] Для цього сировину ретельно подрібнюють і розплавляють в струмені вуглекислого газу. В бурштину немає чітко визначеної точки плавлення — він плавиться в інтервалі від 150 до 300 °С.[1] При подальшому нагріванні частину кислоти відганяють і вона осідає на охолоджених стінках реторти, а те, що залишилось, захоплюється так званою «бурштиновою олією» в приймач.[1] Повторною перегонкою цього дистиляту розділяють олію і кислоту. Обидві порції бурштинової кислоти об'єднують і перекристалізовують.[1] ВикористанняБурштинову кислоту та її похідні використовують для синтезу деяких барвників, інсектицидів, пластмас, ароматичних сполук, лікарських засобів[3]. Також використовують у сільському господарстві як добриво, вона прискорює дозрівання плодів, підвищує холодо- та посухостійкість, стійкість до захворювань, врожайність, збільшує вміст вітамінів та цукрів у плодах. Примітки
Посилання
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Portal di Ensiklopedia Dunia