|
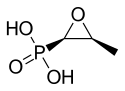
Fosfomisin
|

|
| Nama sistematis (IUPAC)
|
| [(2R,3S)-3-metiloksiran-2-il]asam fosfonat
|
| Data klinis
|
| Nama dagang
|
Monuril, Monurol, Ivozfo, dll
|
| AHFS/Drugs.com
|
monograph
|
| MedlinePlus
|
a697008
|
| Data lisensi
|
US Daily Med:pranala
|
| Kat. kehamilan
|
?
|
| Status hukum
|
Harus dengan resep dokter (S4) (AU) ℞-only (CA) POM (UK) ℞-only (US)
|
| Rute
|
intravena, Oral
|
| Data farmakokinetik
|
| Bioavailabilitas
|
30–37% (melalui mulut, dalam bentuk fosfomisin trometamin); bervariasi tergantung pada asupan makanan
|
| Ikatan protein
|
Nol
|
| Metabolisme
|
Nol
|
| Waktu paruh
|
5,7 jam (rata-rata)
|
| Ekskresi
|
Ginjal, tidak berubah
|
| Pengenal
|
| Nomor CAS
|
23155-02-4  Y Y
78964-85-9 (garam trometamin)
|
| Kode ATC
|
J01XX01 S02AA17
|
| PubChem
|
CID 446987
|
| DrugBank
|
DB00828
|
| ChemSpider
|
394204  Y Y
|
| UNII
|
2N81MY12TE  Y Y
|
| KEGG
|
D04253  Y Y
|
| ChEBI
|
CHEBI:28915  Y Y
|
| ChEMBL
|
CHEMBL1757  Y Y
|
| Sinonim
|
Fosfonomisin, fosfomisin trometamin
|
| Data kimia
|
| Rumus
|
C3H7O4P
|
| SMILES
|
eMolecules & PubChem
|
InChI=1S/C3H7O4P/c1-2-3(7-2)8(4,5)6/h2-3H,1H3,(H2,4,5,6)/t2-,3+/m0/s1  Y Y
Key:YMDXZJFXQJVXBF-STHAYSLISA-N  Y Y
|
| Data fisik
|
| Titik lebur
|
94 °C (201 °F)
|
Fosfomisin adalah antibiotik yang utamanya digunakan untuk mengobati infeksi saluran kemih bagian bawah. Fosfomisin tidak diindikasikan untuk infeksi ginjal. Kadang-kadang fosfomisin digunakan untuk infeksi prostat. Fosfomisin umumnya digunakan dengan cara diminum.[1]
Efek samping yang umum termasuk diare, mual, sakit kepala, dan infeksi jamur vagina. Efek samping yang parah mungkin termasuk anafilaksis dan diare yang berhubungan dengan Clostridioides difficile.[1] Meskipun penggunaan selama kehamilan belum terbukti berbahaya, penggunaan tersebut tidak direkomendasikan. Dosis tunggal saat menyusui tampaknya aman.[2] Fosfomisin bekerja dengan mengganggu produksi dinding sel bakteri.[1]
Fosfomisin ditemukan pada tahun 1969 dan disetujui untuk penggunaan medis di Amerika Serikat pada tahun 1996 [1][3] Fosfomisin tercantum dalam Daftar Obat Esensial Organisasi Kesehatan Dunia.[4] Organisasi Kesehatan Dunia mengklasifikasikan fosfomisin sebagai obat yang sangat penting untuk pengobatan manusia.[5] Obat ini tersedia sebagai obat generik.[6] Obat ini awalnya diproduksi oleh beberapa jenis bakteri Streptomyces, meskipun sekarang dibuat secara kimia.[3]
Sejarah
Fosfomisin (awalnya dikenal sebagai fosfonomisin) ditemukan dalam upaya bersama antara Merck & Co. dan Compañía Española de Penicilina y Antibióticos (CEPA) Spanyol. Fosfomisin pertama kali diisolasi dengan menyaring kultur kaldu Streptomyces fradiae yang diisolasi dari sampel tanah untuk mengetahui kemampuannya menyebabkan pembentukan sferoplas dengan menumbuhkan bakteri. Penemuan ini dijelaskan dalam serangkaian makalah yang diterbitkan pada tahun 1969.[7] CEPA mulai memproduksi fosfomisin dalam skala industri pada tahun 1971 di fasilitasnya yang terdapat di Aranjuez.[8]
Kegunaan dalam medis
Fosfomisin digunakan untuk mengobati infeksi kandung kemih, yang biasanya diberikan sebagai dosis tunggal melalui mulut.[9]
Fosfomisin oral tidak direkomendasikan untuk anak di bawah 12 tahun.[10]
Penggunaan tambahan telah diusulkan.[11] Masalah global terkait peningkatan resistensi antimikroba telah menyebabkan minat baru dalam penggunaannya baru-baru ini.[12]
Fosfomisin dapat digunakan sebagai pengobatan yang mujarab untuk ISK dan ISK yang rumit termasuk pielonefritis akut. Regimen standar untuk ISK yang rumit adalah dosis oral 3 g yang diberikan sekali setiap 48 atau 72 jam untuk total 3 dosis, atau dosis 6 g setiap 8 jam selama 7–14 hari ketika fosfomisin diberikan dalam bentuk IV.[13]
Fosfomisin intravena semakin banyak digunakan untuk mengobati infeksi yang disebabkan oleh bakteri yang resisten terhadap banyak obat, sebagian besar sebagai obat pendamping untuk menghindari terjadinya resistensi dan memanfaatkan aktivitas sinergisnya dengan beberapa antimikroba lainnya. Dosis harian untuk orang dewasa biasanya berkisar antara 12 hingga 24 gram.[14] Bila diberikan dalam bentuk infus kontinyu, dosis muatan fosfomisin adalah 8 g diikuti dengan dosis harian sebesar 16 g atau 24 g. Infus kontinyu disarankan pada pasien dengan fungsi ginjal normal.[15]
Resistensi
Perkembangan resistensi bakteri selama terapi merupakan kejadian yang sering terjadi dan membuat fosfomisin tidak cocok untuk terapi berkelanjutan pada infeksi berat. Mutasi yang menonaktifkan transporter gliserofosfat nonesensial membuat bakteri resistan terhadap fosfomisin.[16][17][18] Namun, fosfomisin dapat digunakan untuk mengobati bakteremia MRSA.[19]
Meresepkan fosfomisin bersama dengan setidaknya satu obat aktif lainnya mengurangi risiko berkembangnya resistensi bakteri. Fosfomisin bekerja secara sinergis dengan banyak antibiotik lain termasuk aminoglikosida, karbapenem, sefalosporin, daptomisin, dan oritavancin.[14][20]
Enzim yang memberikan resistensi terhadap fosfomisin juga telah diidentifikasi dan dikodekan baik secara kromosom maupun pada plasmid.[21]
Enzim-enzim tersebut berbeda berdasarkan identitas nukleofil yang digunakan dalam reaksi: glutation untuk FosA, basilitiol untuk FosB,[22][23] dan air untuk FosX.[21]
Secara umum, enzim FosA dan FosX diproduksi oleh bakteri Gram-negatif, sedangkan FosB diproduksi oleh bakteri Gram-positif.[21]
FosC menggunakan ATP dan menambahkan gugus fosfat ke fosfomisin, sehingga mengubah sifat-sifatnya dan membuat obat tidak efektif.[24]
Efek samping
Obat ini ditoleransi dengan baik dan memiliki insiden efek samping berbahaya yang rendah.[9]
Mekanisme kerja
Meskipun namanya (berakhiran -omisin), Fosfomisin bukanlah makrolida, tetapi anggota kelas baru antibiotik fosfonat. Fosfomisin bersifat bakterisida dan menghambat biogenesis dinding sel bakteri dengan menonaktifkan enzim UDP-N-asetilglukosamin-3-enolpiruviltransferase, yang juga dikenal sebagai MurA.[25] Enzim ini mengkatalisis langkah yang berkomitmen dalam biosintesis peptidoglikan, yaitu ligasi fosfoenolpiruvat (PEP) ke gugus 3'-hidroksil dari UDP-N-asetilglukosamin. Bagian piruvat ini menyediakan penghubung yang menjembatani bagian glikan dan peptida dari peptidoglikan. Fosfomisin adalah analog PEP yang menghambat MurA dengan mengalkilasi residu sisteina pada situs aktif (Cys 115 dalam enzim bakteri Escherichia coli).[26][27]
Fosfomisin memasuki sel bakteri melalui transporter gliserofosfat.[28]
Biosintesis
Klaster gen biosintesis fosfomisin lengkap dari Streptomyces fradiae telah diklon dan diurutkan, dan produksi heterolog fosfomisin di Streptomyces lividans telah dicapai oleh Ryan Woodyer dari kelompok penelitian Huimin Zhao dan Wilfred van der Donk.[29]
Pembuatan sintetis
Produksi fosfomisin dalam skala besar dicapai dengan membuat epoksida asam cis-propenilfosfonat untuk menghasilkan campuran rasemat fosfomisin.[30]
Referensi
- ^ a b c d "Fosfomycin Tromethamine Monograph for Professionals". Drugs.com (dalam bahasa Inggris). Diarsipkan dari versi asli tanggal 29 October 2019. Diakses tanggal 29 October 2019.
- ^ "Fosfomycin (Monurol) Use During Pregnancy". Drugs.com (dalam bahasa Inggris). Diarsipkan dari versi asli tanggal 29 October 2019. Diakses tanggal 29 October 2019.
- ^ a b Finch RG, Greenwood D, Whitley RJ, Norrby SR (2010). Antibiotic and Chemotherapy E-Book (dalam bahasa Inggris). Elsevier Health Sciences. hlm. 259. ISBN 9780702047657.
- ^ World Health Organization (2019). World Health Organization model list of essential medicines: 21st list 2019. Geneva: World Health Organization. hdl:10665/325771
 . WHO/MVP/EMP/IAU/2019.06. License: CC BY-NC-SA 3.0 IGO. . WHO/MVP/EMP/IAU/2019.06. License: CC BY-NC-SA 3.0 IGO.
- ^ World Health Organization (2019). Critically important antimicrobials for human medicine (edisi ke-6th revision). Geneva: World Health Organization. hdl:10665/312266
 . ISBN 9789241515528. . ISBN 9789241515528.
- ^ British national formulary : BNF 76 (edisi ke-76). Pharmaceutical Press. 2018. hlm. 560–561. ISBN 9780857113382.
- ^ Silver LL (2011). "Rational Approaches to Antibacterial Discovery: Pre-Genomic Directed and Phenotypic Screening". Dalam Dougherty T, Pucci MJ. Antibiotic Discovery and Development. Springer. hlm. 46. doi:10.1007/978-1-4614-1400-1_2. ISBN 978-1-4614-1400-1.
- ^ "About us: Our history". Encros. Diarsipkan dari versi asli tanggal 14 September 2011.
- ^ a b Patel SS, Balfour JA, Bryson HM (April 1997). "Fosfomycin tromethamine. A review of its antibacterial activity, pharmacokinetic properties and therapeutic efficacy as a single-dose oral treatment for acute uncomplicated lower urinary tract infections". Drugs. 53 (4): 637–656. doi:10.2165/00003495-199753040-00007. PMID 9098664.
- ^ "MONURIL SACHETS 3G". Diarsipkan dari versi asli tanggal 28 May 2014. Diakses tanggal 26 May 2014.
- ^ Falagas ME, Giannopoulou KP, Kokolakis GN, Rafailidis PI (April 2008). "Fosfomycin: use beyond urinary tract and gastrointestinal infections". Clinical Infectious Diseases. 46 (7): 1069–1077. doi:10.1086/527442
 . PMID 18444827. . PMID 18444827.
- ^ Falagas ME, Grammatikos AP, Michalopoulos A (October 2008). "Potential of old-generation antibiotics to address current need for new antibiotics". Expert Review of Anti-Infective Therapy. 6 (5): 593–600. doi:10.1586/14787210.6.5.593. PMID 18847400.
- ^ Zhanel GG, Zhanel MA, Karlowsky JA (28 March 2020). "Oral and Intravenous Fosfomycin for the Treatment of Complicated Urinary Tract Infections". The Canadian Journal of Infectious Diseases & Medical Microbiology. Hindawi Limited. 2020: 8513405. doi:10.1155/2020/8513405
 . PMC 7142339 . PMC 7142339  . PMID 32300381. . PMID 32300381.
- ^ a b Antonello RM, Principe L, Maraolo AE, Viaggi V, Pol R, Fabbiani M, et al. (August 2020). "Fosfomycin as Partner Drug for Systemic Infection Management. A Systematic Review of Its Synergistic Properties from In Vitro and In Vivo Studies". Antibiotics. 9 (8): 500. doi:10.3390/antibiotics9080500
 . PMC 7460049 . PMC 7460049  . PMID 32785114. . PMID 32785114.
- ^ Antonello RM, Di Bella S, Maraolo AE, Luzzati R (June 2021). "Fosfomycin in continuous or prolonged infusion for systemic bacterial infections: a systematic review of its dosing regimen proposal from in vitro, in vivo and clinical studies". European Journal of Clinical Microbiology & Infectious Diseases. 40 (6): 1117–1126. doi:10.1007/s10096-021-04181-x. PMC 8139892
 . PMID 33604721 . . PMID 33604721 .
- ^ Navas J, León J, Arroyo M, García Lobo JM (October 1990). "Nucleotide sequence and intracellular location of the product of the fosfomycin resistance gene from transposon Tn2921". Antimicrobial Agents and Chemotherapy. 34 (10): 2016–2018. doi:10.1128/AAC.34.10.2016. PMC 171982
 . PMID 1963292. . PMID 1963292.
- ^ Kahan FM, Kahan JS, Cassidy PJ, Kropp H (May 1974). "The mechanism of action of fosfomycin (phosphonomycin)". Annals of the New York Academy of Sciences. 235 (1): 364–386. Bibcode:1974NYASA.235..364K. doi:10.1111/j.1749-6632.1974.tb43277.x. PMID 4605290.
- ^ Castañeda-García A, Blázquez J, Rodríguez-Rojas A (April 2013). "Molecular Mechanisms and Clinical Impact of Acquired and Intrinsic Fosfomycin Resistance". Antibiotics. 2 (2): 217–236. doi:10.3390/antibiotics2020217
 . PMC 4790336 . PMC 4790336  . PMID 27029300. . PMID 27029300.
- ^ Omori K, Kitagawa H, Takada M, Maeda R, Nomura T, Kubo Y, Shigemoto N, Ohge H (April 2024). "Fosfomycin as salvage therapy for persistent methicillin-resistant Staphylococcus aureus bacteremia: A case series and review of the literature". J Infect Chemother. 30 (4): 352–356. doi:10.1016/j.jiac.2023.10.024. PMID 37922987 .
- ^ Lagatolla C, Mehat JW, La Ragione RM, Luzzati R, Di Bella S (September 2022). "In Vitro and In Vivo Studies of Oritavancin and Fosfomycin Synergism against Vancomycin-Resistant Enterococcus faecium". Antibiotics. 11 (10): 1334. doi:10.3390/antibiotics11101334
 . PMC 9598191 . PMC 9598191  . PMID 36289992 . . PMID 36289992 .
- ^ a b c Rigsby RE, Fillgrove KL, Beihoffer LA, Armstrong RN (2005). "Fosfomycin resistance proteins: a nexus of glutathione transferases and epoxide hydrolases in a metalloenzyme superfamily". Gluthione [sic] Transferases and Gamma-Glutamyl Transpeptidases. Methods in Enzymology. 401. hlm. 367–379. doi:10.1016/S0076-6879(05)01023-2. ISBN 9780121828066. PMID 16399398.
- ^ Sharma SV, Jothivasan VK, Newton GL, Upton H, Wakabayashi JI, Kane MG, et al. (July 2011). "Chemical and Chemoenzymatic syntheses of bacillithiol: a unique low-molecular-weight thiol amongst low G + C Gram-positive bacteria". Angewandte Chemie. 50 (31): 7101–7104. doi:10.1002/anie.201100196. PMID 21751306.
- ^ Roberts AA, Sharma SV, Strankman AW, Duran SR, Rawat M, Hamilton CJ (April 2013). "Mechanistic studies of FosB: a divalent-metal-dependent bacillithiol-S-transferase that mediates fosfomycin resistance in Staphylococcus aureus". The Biochemical Journal. 451 (1): 69–79. doi:10.1042/BJ20121541. PMC 3960972
 . PMID 23256780. . PMID 23256780.
- ^ García P, Arca P, Evaristo Suárez J (July 1995). "Product of fosC, a gene from Pseudomonas syringae, mediates fosfomycin resistance by using ATP as cosubstrate". Antimicrobial Agents and Chemotherapy. 39 (7): 1569–1573. doi:10.1128/aac.39.7.1569. PMC 162783
 . PMID 7492106. . PMID 7492106.
- ^ Brown ED, Vivas EI, Walsh CT, Kolter R (July 1995). "MurA (MurZ), the enzyme that catalyzes the first committed step in peptidoglycan biosynthesis, is essential in Escherichia coli". Journal of Bacteriology. 177 (14): 4194–4197. doi:10.1128/jb.177.14.4194-4197.1995. PMC 177162
 . PMID 7608103. . PMID 7608103.
- ^ Zhu JY, Yang Y, Han H, Betzi S, Olesen SH, Marsilio F, Schönbrunn E (April 2012). "Functional consequence of covalent reaction of phosphoenolpyruvate with UDP-N-acetylglucosamine 1-carboxyvinyltransferase (MurA)". The Journal of Biological Chemistry. 287 (16): 12657–12667. doi:10.1074/jbc.M112.342725
 . PMC 3339971 . PMC 3339971  . PMID 22378791. . PMID 22378791.
- ^ Krekel F, Samland AK, Macheroux P, Amrhein N, Evans JN (October 2000). "Determination of the pKa value of C115 in MurA (UDP-N-acetylglucosamine enolpyruvyltransferase) from Enterobacter cloacae". Biochemistry. 39 (41): 12671–12677. doi:10.1021/bi001310x. PMID 11027147.
- ^ Santoro A, Cappello AR, Madeo M, Martello E, Iacopetta D, Dolce V (December 2011). "Interaction of fosfomycin with the glycerol 3-phosphate transporter of Escherichia coli". Biochimica et Biophysica Acta (BBA) - General Subjects. 1810 (12): 1323–1329. doi:10.1016/j.bbagen.2011.07.006. PMID 21791237.
- ^ Woodyer RD, Shao Z, Thomas PM, Kelleher NL, Blodgett JA, Metcalf WW, et al. (November 2006). "Heterologous production of fosfomycin and identification of the minimal biosynthetic gene cluster". Chemistry & Biology. 13 (11): 1171–1182. doi:10.1016/j.chembiol.2006.09.007
 . PMID 17113999. . PMID 17113999.
- ^ Marocco CP, Davis EV, Finnell JE, Nguyen PH, Mateer SC, Ghiviriga I, et al. (2011). "Asymmetric synthesis of (−)-fosfomycin and its trans-(1S,2S)-diastereomer using a biocatalytic reduction as the key step". Tetrahedron: Asymmetry. Elsevier BV. 22 (18–19): 1784–1789. doi:10.1016/j.tetasy.2011.10.009. ISSN 0957-4166.
|

