|
ГемостазГемостаз (гемостазис[1]) — це фізіологічний процес в крові, який виконує захисну роль в організмі, при кровотечі і/чи тромбоутворенні.[2] Два найбільш досліджені процеси, які задіяні у гемостазі — це гемкоагуляція з тромбоутворенням та лізис тромбів (тромболізис і/або природня реканалізація). Фізіологічний гемостаз можна розділити на два підпроцеси, які, однак, взаємодіють між собою. У первинному (також: клітинному) гемостазі, беруть участь тромбоцити, клітини ушкодженої стінки кровоносної судини (ендотелію та гладком'язові клітини), та тканини за межами пошкодженої судини. Судина у відповідь на пошкодження звужується, тромбоцити збираються біля місця ураження (адгезія), прилипають поверхнями один до одного (агрегація) і таким чином утворюється первинне закупорювання місця ушкодження. При вторинному (також: плазматичному) гемостазі, ця «оклюзія» посилюється утворенням фібринових ниток. Важливу роль в цьому процесі відіграє активація близько десятка факторів згортання, що містяться в плазмі крові. Генетичний дефект факторів згортання може призвести до захворювань, наприклад гемофілія. Початок загоєння ран також ініціюється факторами росту, які виділяються тромбоцитами та ендотеліальними клітинами. Після закінчення загоєння ран фібрин вивільняється фібринолітичною системою плазми крові. Гіперкоагуляція — це посилене згортання крові. Фізіологічні процеси після травми судин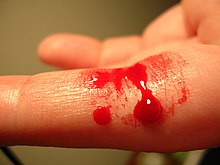 Після травмування дрібних судин, кровотеча зазвичай швидко припиняється. Гемостаз, що відповідає за це, можна розглядати як послідовність наступних процесів.
Клітинний гемостазВ крові людини в нормі знаходиться від 150.000 до 400.000 тромбоцитів на мікролітр. В клітинній мембрані тромбоцитів наявні численні глікопротеїни і рецептори, які відіграють важливу роль в клітинному гемостазі. Внутрішня клітинна стінка кровоносних судин називається ендотелієм. Зсередини вона вкрита глікокаліксисом, шаром «слизу», до якого тромбоцити не мають рецепторів. Це одна з причин того, що тромбоцити можуть залишаютися неактивними в непошкоджених судинах і не здатні прикріпитися до стінки судин. Різні фактори також протидіють активації, наприклад, простациклін та оксид азоту, а також гепарин, який синтезується тучними клітинами, чий інгібуючий вплив на гемостаз можна використовувати в терапевтичних цілях.  Адгезія та активація тромбоцитівПри пошкодженні судини кров контактує з навколишньою сполучною тканиною, включаючи колагенові волокна. Колаген — структурний білок, який знаходиться майже скрізь у позаклітинному просторі. Тромбоцити спочатку прилипають до цих волокон (тромбоцитарна адгезія), що призводить до утворення тонкого покрову рани. Адгезія забезпечується фактором Фон Віллебранда (vWF), розчинним білком крові, який утворюється ендотеліальними клітинами та мегакаріоцитами. Разом з фібронектином та ламініном, він створює зв'язок між колагеновими волокнами та рецептором на тромбоцитах (GP Ib / V / IX). Дефект фактора Фон Віллебранда призводить до синдрому Віллебранда-Юргенса. Адгезія запускає активацію тромбоцитів: вони виділяють іони кальцію, АДФ, серотонін, тромбоксан А 2 та інші речовини з так званих «електронепроникних гранул». Цей механізм залучає додаткові тромбоцити (хемотаксис). Тромбоксан А 2 також істотно сприяє звуженню судин, що протидіє сильному кровотоку. Вивільняється вміст так званих «α-гранул» тромбоцитів: коефіцієнти згортання (фактор V, фактор VIII), адгезиви (vWF, фібронектин, тромбоспондин) та фактори росту. Активізуючи різні метаболічні шляхи, все більше утворюються такі речовини, як тромбоксан А 2 та ФАТ (фактор активації тромбоцитів). Деякі з цих речовин індукують згортання плазми.  . Агрегація активованих тромбоцитів сприяє перебудові цитоскелету, що спричиняє багаторазове збільшення клітинної поверхні. В той час як тромбоцити в неактивному стані нагадують форму кришталиків, в активному стані — вони набувають сферичної форми і переносять довгі псевдоподії, за допомогою яких можуть чіплятись одне до одного, або рідше до інших клітин. З'єднані одне з одним тромбоцити врешті утворюють «тромбоцитну пробку», яку називають білим тромбом. На цьому закінчується клітинний гемостаз. Процес зазвичай займає одну-чотири хвилини, ця тривалість називається часом кровотечі. Білий тромб не дуже стійкий і може достатньо легко відриватись. Плазматичний гемостаз утворює більш міцне з'єднання. Плазматичний гемостазПлазматичний гемостаз утворює «сітку» з механічно стійкого фібрину, в який крім тромбоцитів захоплюються еритроцити, що в сукупності називається «червоним тромбом». Активовані тромбоцити мають на своїй клітинній мембрані рецепторний комплекс (глікопротеїн IIb / IIIa), з яким зв'язується фібриноген з плазми та адгезивні речовини, що виділяються з активованих тромбоцитів (фібронектин, тромбоспондин). Через «механізми зворотного зв'язку», вивільнені речовини призводять до незворотної агрегації, при якій клітинні мембрани тромбоцитів зливаються разом. Вторинний гемостаз, також відомий як каскад згортання, поділяється на три фази: фаза активації, згортання та втягування.  Фаза активаціїЧерез контакт тромбоцитів з негативно зарядженими поверхнями, такими як скло, активуються фактори XII та XI, які запускають каскад згортання (внутрішня система) Якщо фактор XII не виробляється у людини, це не призводить до значного розладу згортання, на відміну від нестачі факторів VIII, IX та XI, що призводить до гемофілії A, B і C. Нормальний фізіологічний процес (зовнішня система або екзогенний механізм) ініціюється контактом крові з тканинним тромбопластином з травмованої субендотеліальної тканини. Тканинний фактор ((ТФ), тканинний тромбопластин або фактор III) — мембранний білок, який утворюється, в адвентиції судин, та вивільняється лише ендотеліальними клітинами після активації. Він утворює комплекс з фактором VII, який перетворює його в активну форму. Внаслідок цього механізму утворюється тромбін, але процес пригнічується достатньо швидко «інгібітором шляху тканинного фактора» (ІШТФ). Коли утворюється достатня кількість тромбіну, активується так званий активаторний комплекс факторів IX та VIII. Цей комплекс у свою чергу активує фактор X. Відсутність факторів VIII або IX призводить до гемофілії — каскад переривається і згортання не відбувається. Пацієнт може стікати кров'ю до смерті від найменших пошкоджень. В обох механізмах — внутрішньому та зовнішньому — фактор X остаточно активується до фактора Xa. Це в свою чергу розщеплює протромбін (фактор II), утворюється тромбін (фактор IIa). Ця реакція на мембрані тромбоцитів відбувається лише в присутності кальцію і значно прискорюється за допомогою механізму «позитивного зворотного зв'язку» із комплексом факторів VIII та IX. Фаза активації закінчується утворенням ферментативно активного тромбіну. Фази згортання та втягуванняФерментативно активний тромбін відповідає за полімеризацію фібрину і, таким чином, за утворення червоного тромбу: у фазі згортання він розщеплює низькомолекулярні одиниці (мономери) від неактивного попередника фібриногену (фактор I), який з'єднується не ковалентно з полімерним фібрином. Під дією фактора XIII остаточно утворюються ковалентні зв'язки між мономерами і тромб стабілізується. Фібрин «зшиває» тромбоцити, які вже накопичилися, тим самим посилюючи закриття рани. У утворену «сітку» потрапляють еритроцити, утворюється так званий червоний тромб. Тромбін продовжує викликати скорочення актин-міозинового скелета всередині тромбоцитів: тромбоцити, що скорочуються, тягнуться за фібринову сітку і одночасно за краї рани, таким чином повністю закриваючи її. Скорочення — підтримується PDGF (тромбоцитарний фактор росту) — також сприяє проникненню клітин сполучної тканини, починається загоєння ран. Огляд факторів зсідання та інгібіторівФактори зсідання кровіПриродніКрім іонів кальцію (фактор IV), чинниками згортання є білки. Кожному фактору присвоюється римське число. Невелике a після числа означає, що воно знаходиться в активній формі. З історичних причин число VI більше не присвоюється, відповідний коефіцієнт ідентичний Va[3]. Не усі уже відкриті речовини і сполуки, що беруть участь у гемостазі, мають свій номер у міжнародній номенклатурі.
СинтетичніМедикаментозне посилення згортання крові Препарати, що усувають вроджений або набутий дефіцит факторів згортання, наприклад концентрат фактора VIII для гемофілії, набули особливого значення для медикаментозного лікування, вітамін K і концентрат протромбіну для кровотечі при лікуванні кумарином або замороженою свіжою плазмою з дисемінованою внутрішньосудинною коагуляцією. Якщо є виражений брак тромбоцитів, їх можна замінити у вигляді тромбоцитарних концентратів. Дію гепарину можна скасувати антидотом - протаміном. Гемостаз також може бути підсилений за рахунок пригнічення природного антагоніста коагуляції, фібринолізу. Препарати з таким механізмом дії називаються антифібринолітиками. Транексамова кислота, і ε-амінокапронова кислота використовуються в якості активних інгредієнтів. Раніше у кардіохірургії використовувся апротинін, був знятий з фарм. ринку деяких європейських країн в листопаді 2007 р — через ризик ренальної дисфункції, масивних кровотеч та підвищеної смертності під час кардіохірургічного лікування.[4][5][6]
Інгібітори зсідання кровіПриродніЩоб уникнути згортання крові при відсутності травм, плазма крові містить різні інгібіторні речовини. Інгібітори протеази пригнічують утворення фібрину. Антитромбін інгібує кілька коагуляційних протеаз у фазах активації та згортання. Інгібіторний ефект значно посилюється його кофактором, гепарином. Гепарин складається з ендотеліальних клітин і тучних клітин. Тромбомодулін, який також походить з ендотелію, зв'язується з тромбіном і активує білок С, який інактивує кофактори Va і VIIIa після зв'язування з білком S. Природні (фізіологічні) антикоагулянти:[7]
СинтетичніМедикаментозне пригнічення згортання крові Зазвичай до, під час і після операцій, а також при багатьох інших захворюваннях, антикоагулянтні препарати (які помилково називають розріджувачами крові) часто застосовуються для запобігання тромбозу та легеневої емболії . На сьогодні найпоширенішою причиною тривалої терапевтичної антикоагуляції є фібриляція або миготіння передсердь. При цій серцевій аритмії існує підвищений ризик емболії, який у багатьох пацієнтів доводиться знижувати, розріджуючи кров. Друга найпоширеніша причина — тромбоз, як правило, глибоких вен нижніх кінцівок. Пригнічення згортання крові в гострій фазі призначене для запобігання подальшого розширення тромбозу та подальшого рецидиву. ГепаринГепарин та «гепариноїди» можуть використовуватися для інгібування коагуляції in vivo. Це ланцюг цукрів, який має сильний негативний заряд, та приєднується до вже згаданого білкового антитромбіну. Цей комплекс тепер більш ефективно зв'язує фактори тромбіну та Xa, які тим самим виходять з процесу, каскад згортання припиняється. Ефекти починаються відразу після внутрішньовенного введення. Лікарський гепарин зазвичай отримують з тканин тварин. КумариниІншою можливістю є так звані антагоністи вітаміну K, такі як похідні кумарину фенпрокумон та варфарин. Вітамін К необхідний як кофермент для синтезу більшості факторів згортання. Кумарин починає свою дію в печінці і запобігає зниженню вітаміну К (філохінон). Він впливає на γ- карбоксилювання факторів згортання (II, VII, IX, X) і сам піддається окисленню (вивільнення електронів). Без подальшого зниження (поглинання електронів) вітамін К залишається недіючим. Ефект набуває чинності лише через певний час (дікілька днів) АнтиагрегантиАцетилсаліцилова кислота може перешкоджати агрегації тромбоцитів, тобто клітинному гемостазу. Циклооксигеназа(ЦОГ), яка необхідна для синтезу фактора тромбоцитів тромбоксану A 2, необоротно інгібується шляхом приєднання залишку оцтової кислоти. Клопідогрель також діє на агрегацію тромбоцитів, що гальмує АДФ-залежну активацію тромбоцитів шляхом незворотного блокування рецепторів. Абциксимаб — це рекомбінантне моноклональне антитіло, яке блокує тромбоцитний глікопротеїн IIb / IIIa, тим самим запобігаючи агрегацію тромбоцитів. Тірофібан має той самий механізм дії. ФібринолітикиФібринолітики активізують плазміноген і, таким чином, сприяють розчиненню тромбів (тромболізу). Цей механізм використовується для лікування інфарктів, легеневої емболії, тромбозів вен ніг, периферичних оклюзійних захворювань, а також протягом «чотиригодинного вікна», для гострих інфарктів мозку. У той час як активні речовини, такі як стрептокіназа та урокіназа, мають неспецифічну дію як на фібриноген, так і на фібрин, нові речовини, такі як Альтеплаза (плазміногений активатор рекомбінантної тканини, англ. rt-PA), мають селективність щодо зв'язаного фібрину в тромбах, що зменшує системні побічні ефекти, особливо кровотечі. Застосування фібринолітиків відбувається лише під контролем лікаря. Інгібування «in vitro»In vitro, наприклад у пробірках крові часто використовують ЕДТА і цитрат, хелатори яких утворюють комплекс з катіонами кальцію, необхідними для згортання. Антикоагуляція гепарином можлива також in vitro. Антикоагулянт вибирається, виходячи з цього, згодом планується обстеження крові, яка не була згорнута. Для самих досліджень на коагуляцію цитрат використовується майже виключно як антикоагулянт, розбавляючи зразок крові у співвідношенні 9 + 1, 3,8 % розчином цитрату натрію. Зазвичай використовують промислово збірні трубки, які вже вміщують 0,3 мл розчину цитрату натрію, до яких доливають 2,7 мл крові. Для надійності аналізів, створених з цього приводу, важливо, щоб це співвідношення дотримувалося точно і щоб зразок крові ретельно змішувався з розчином цитрату натрію відразу після збору. Визначення здатності крові до згортання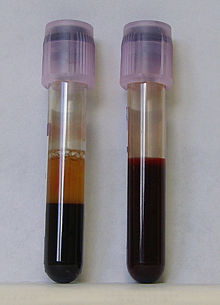 В клінічній практиці для оцінки згортальної системи крові застосовують наступні основні лабораторні параметри:
Артеріальна кров згортається швидше, ніж венозна, що пов'язано з різницею концентрації кисню і вуглекислого газу. Коагуляцію артеріальної крові можна уповільнити, додаючи вуглекислоту, але коагуляцію венозної крові можна прискорити, збільшуючи в ній вміст кисню. Див. такожПримітки
Джерела
Література
Посилання
|
Portal di Ensiklopedia Dunia