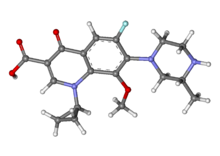
Gatifloksasin

|
|
| Nama sistematis (IUPAC)
|
| 1-Siklopropil-6-fluoro-8-metoksi-7-(3-metilpiperazin-1-il)-4-okso-kuinolin-3-asam karboksilat
|
| Data klinis
|
| Nama dagang
|
Gatiflo, Tequin, Zymar, dll
|
| AHFS/Drugs.com
|
monograph
|
| MedlinePlus
|
a605012
|
| Kat. kehamilan
|
?
|
| Status hukum
|
Hanya dengan resep
|
| Rute
|
Oral (dihentikan), Intravena (dihentikan), oftalmik
|
| Data farmakokinetik
|
| Ikatan protein
|
20%
|
| Waktu paruh
|
7 – 14 jam
|
| Pengenal
|
| Nomor CAS
|
112811-59-3  Y Y
|
| Kode ATC
|
J01MA16 S01AE06
|
| PubChem
|
CID 5379
|
| DrugBank
|
DB01044
|
| ChemSpider
|
5186  Y Y
|
| UNII
|
81485Y3A9A  Y Y
|
| KEGG
|
D08011  Y Y
|
| ChEBI
|
CHEBI:5280  Y Y
|
| ChEMBL
|
CHEMBL31  Y Y
|
| NIAID ChemDB
|
AIDSNO:044913
|
| Data kimia
|
| Rumus
|
C19H22FN3O4
|
InChI=1S/C19H22FN3O4/c1-10-8-22(6-5-21-10)16-14(20)7-12-15(18(16)27-2)23(11-3-4-11)9-13(17(12)24)19(25)26/h7,9-11,21H,3-6,8H2,1-2H3,(H,25,26)  Y Y
Key:XUBOMFCQGDBHNK-UHFFFAOYSA-N  Y Y
|
Gatifloksasin adalah antibiotik dari keluarga fluorokuinolon generasi keempat.[1] Seperti halnya antibiotik fluorokuinolon lainnya, antibiotik ini menghambat enzim bakteri DNA girase dan topoisomerase IV. Obat ini dipatenkan pada tahun 1986 dan disetujui untuk penggunaan medis pada tahun 1999.[2]
Efek Samping
Sebuah penelitian di Kanada yang diterbitkan dalam New England Journal of Medicine pada bulan Maret 2006, menyatakan bahwa gatifloksasin dapat memiliki efek samping yang signifikan termasuk disglikemia.[3] Sebuah tajuk rencana oleh Jerry Gurwitz dalam terbitan yang sama menyerukan agar Badan Pengawas Obat dan Makanan Amerika Serikat (FDA) mempertimbangkan untuk memberikan peringatan kotak hitam kepada gatifloksasin.[4] Tajuk rencana ini mengikuti distribusi surat tertanggal 15 Februari oleh Bristol Myers Squibb kepada penyedia layanan kesehatan yang menunjukkan tindakan yang diambil oleh FDA untuk memperkuat peringatan terhadap obat tersebut.[5] Selanjutnya, Bristol Myers Squibb melaporkan akan menghentikan produksi Tequin, mengakhiri penjualan obat tersebut setelah stok yang ada habis, dan mengembalikan semua hak kepada Kyorin.[6]
Sebaliknya, gatifloksasin oftalmik umumnya dapat ditoleransi dengan baik. Konsentrasi obat sistemik yang diamati setelah pemberian oral 400 mg (0,01 ons) gatifloksasin kira-kira 800 kali lebih tinggi dibandingkan dengan tetes mata gatifloksasin 0,5%. Diberikan sebagai obat tetes mata, gatifloksasin memiliki paparan sistemik yang sangat rendah. Oleh karena itu, paparan sistemik yang dihasilkan dari larutan mata gatifloksasin kemungkinan besar tidak menimbulkan risiko toksisitas sistemik.[butuh rujukan]
Kontraindikasi
Obat ini dikontraindikasikan kepada orang yang memiliki hipersensitivitas terhadapnya.[7]
Dalam Budaya Masyarakat
Ketersediaan
Gatifloksasin saat ini tersedia di Amerika Serikat dan Kanada hanya sebagai solusi oftalmik.[butuh rujukan]
Pada tahun 2011, Persatuan Kementerian Kesehatan dan Kesejahteraan Keluarga India melarang pembuatan, penjualan, dan distribusi gatifloksasin karena efek sampingnya yang merugikan.[8]
Di Cina, gatifloksasin dijual dalam bentuk tablet dan juga formulasi obat tetes mata.[butuh rujukan]
Referensi
- ^ Burka JM, Bower KS, Vanroekel RC, Stutzman RD, Kuzmowych CP, Howard RS (July 2005). "The effect of fourth-generation fluoroquinolones gatifloxacin and moxifloxacin on epithelial healing following photorefractive keratectomy". American Journal of Ophthalmology. 140 (1): 83–87. doi:10.1016/j.ajo.2005.02.037. PMID 15953577.
- ^ Fischer J, Ganellin CR (2006). Analogue-based Drug Discovery (dalam bahasa Inggris). John Wiley & Sons. hlm. 501. ISBN 9783527607495.
- ^ Park-Wyllie LY, Juurlink DN, Kopp A, Shah BR, Stukel TA, Stumpo C, et al. (March 2006). "Outpatient gatifloxacin therapy and dysglycemia in older adults". The New England Journal of Medicine. 354 (13): 1352–1361. doi:10.1056/NEJMoa055191. hdl:1807/16915
 . PMID 16510739. Note: publication date 30 March; available on-line 1 March
. PMID 16510739. Note: publication date 30 March; available on-line 1 March
- ^ Gurwitz JH (March 2006). "Serious adverse drug effects--seeing the trees through the forest". The New England Journal of Medicine. 354 (13): 1413–1415. doi:10.1056/NEJMe068051. PMID 16510740.
- ^ Lewis-Hall F (February 15, 2006). "Dear Healthcare Provider" (PDF). Bristol-Myers Squibb. Diakses tanggal May 1, 2006.
- ^ Schmid RE (May 1, 2006). "Drug Company Taking Tequin Off Market". Associated Press. Diarsipkan dari versi asli tanggal November 25, 2007. Diakses tanggal 2006-05-01.
- ^ Peggy Peck (2 May 2006). "Bristol-Myers Squibb Hangs No Sale Sign on Tequin". Med Page Today. Diakses tanggal 24 February 2009.
- ^ "Two drugs banned". The Hindu. Chennai, India. 19 March 2011. Diarsipkan dari versi asli tanggal 6 March 2012.

