|
Réaction d'AppelLa réaction d'Appel est une réaction organique convertissant un alcool en chlorure d'alkyle en utilisant la triphénylphosphine et le tétrachlorure de carbone[1]. L'utilisation de tétrabromure de carbone ou de dibrome comme source d'halogène produit des bromures d'alkyle, tandis que l'utilisation d'iodométhane ou de diiode donne des iodures d'alkyle. La découverte de cette réaction est crédité au chimiste allemand Rolf Appel (en) qui lui donne son nom[2], bien qu'elle fût découverte auparavant[3]. Une des forces de cette réaction vient du fait que si le carbone portant la fonction alcool était chiral, ce centre stéréogénique se retrouve inversé dans le chlorure d'alkyle obtenu en fin de réaction (voir mécanisme ci-dessous)[4]. La réaction est quelque peu similaire à la réaction de Mitsunobu, où la combinaison d'une organophosphine comme accepteur d'oxo, d'un composé diazo comme accepteur d'hydrogène, et d'un nucléophile est utilisée pour convertir un alcool en ester, et si l'alcool était chiral, après l'hydrolyse de cette ester, obtenir le même alcool qu'au départ mais avec son centre stéréogénique inversé[5],[6]. 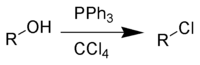 Cette réaction est devenue de moins en moins utilisée du fait de la restriction de l'usage du tétrachlorure de carbone du fait du protocole de Montréal. De plus cette réaction produit des éléments halogénés toxiques et coproduit des composés organophosphorés qui doivent être séparés du produit voulu[7]. Le réactif phosphoré peut aussi être utilisé en quantité catalytique[8],[9]. Le bromure d'alkyle correspondant peut aussi être synthétisé par addition du bromure de lithium comme source d'ions bromures. D'autres donneurs d'halogènes tels que la famille des 1,3-dihalo-5,5-diméthylhydantoïnes, comprenant les variants 1,3-dichloro (DCH), 1,3-dibromo (DBH) et 1,3-diiodo-5-5-diméthylhydantoïnes (DIH) ont été proposés comme des alternatives renouvlables aux tétrahalométhanes (CX4). Le mécanisme est supposé être identique qu'avec les tétrachlorure de carbone, est rapide et fournit de hauts rendements[10].  MécanismeLe mécanisme de la réaction d'Appel est ici illustré par la transformation du géraniol du chlorure de géranyle[11]. La réaction débute par la formation de sel de phosphonium (3). La déprotonation de l'alcool, formant le chloroforme, produit un alcoolate (5). La suite de la réaction est la substitution nucléophile du chlorure porté par le sel de phosphonium sur l'alcoolate pour former le chlorure d'alkyle final (8). Dans le cas d'un alcool primaire ou secondaire, cette réaction se fait en une seule étape par un mécanisme de type SN2. Dans le cas d'un alcool tertiaire, la réaction se fait par un mécanisme de type SN1, donc en deux étapes, la première produisant un intermédiaire organophosphine (7) et un ion chlorure (6).La principale force derrière cette réaction et d'autres similaires est la formation d'une liaison double forte P=O[12]. VariantesLa réaction d'Appel est également efficace sur les acides caboxyliques ; de ce fait, elle a été utilisée pour les convertir en oxazolines, oxazines et thiazolines[13]. Notes et références
Voir aussi |
Portal di Ensiklopedia Dunia

