|
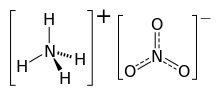
Amonium nitrat
Amonium nitrat adalah suatu senyawa kimia, yang merupakan garam nitrat dari kation amonium. Senyawa ini memiliki rumus kimia NH4NO3, disederhanakan menjadi N2H4O3. Senyawa ini adalah padatan kristal putih dan sangat larut dalam air. Senyawa ini utamanya digunakan dalam pertanian sebagai pupuk kaya-nitrogen.[4] Penggunaan utama lainnya adalah sebagai komponen campuran peledak yang digunakan dalam konstruksi pertambangan, penggalian, dan konstruksi sipil. Senyawa ini adalah penyusun utama ANFO, sebuah industri peledak populer yang menyumbang 80% bahan peledak yang digunakan di Amerika Utara; formulasi serupa telah digunakan dalam alat peledak terimprovisasi. Banyak negara menghapusnya dalam aplikasi konsumen karena kekhawatiran akan potensi penyalahgunaannya. KeberadaanAmonium nitrat ditemukan sebagai mineral alami (amonia nitre—analog amonium garam dan mineral nitre lainnya seperti natrium nitrat) di daerah paling kering di Gurun Atacama di Chile, sering Sebagai kerak di tanah dan/atau bersamaan dengan nitrat lainnya, klorat, iodat, dan mineral halida. Amonium nitrat ditambang di sana di masa lalu, namun hampir 100% bahan kimia yang saat ini digunakan adalah sintetik. ProduksiProduksi industri amonium nitrat mengandung asam basa amonia dengan asam nitrat:[5]
Amonia digunakan dalam bentuk anhidratnya (yaitu bentuk gas) dan asam nitrat terkonsentrasi. Reaksi ini berlangsung keras karena sifatnya yang sangat eksotermik. Setelah larutan terbentuk, biasanya pada konsentrasi sekitar 83%, kelebihan air diuapkan menjadi kandungan amonium nitrat (AN) sebesar 95% sampai konsentrasi 99,9% (AN meleleh), tergantung pada kadarnya. Lelehan AN kemudian dibuat menjadi "prills" atau manik-manik kecil dalam menara semprot, atau menjadi butiran dengan menyemprotkannya dan berjatuhan di drum yang berputar. Potongan atau butiran tersebut dapat dikeringkan lebih lanjut, didinginkan, lalu dilapisi untuk mencegah pengeringan. Potongan atau butiran ini adalah produk AN yang khas dalam perdagangan. Amonia yang dibutuhkan untuk proses ini diperoleh dengan proses Haber dari nitrogen dan hidrogen. Amonia yang dihasilkan oleh proses Haber dioksidasi menjadi asam nitrat oleh proses Ostwald. Metode produksi lain adalah varian dari proses Odda: Produknya, kalsium karbonat dan amonium nitrat, dapat secara terpisah dimurnikan atau dijuan tergabung sebagai kalsium amonium nitrat. Amonium nitrat dapat pula dibuat melalui reaksi metatesis: ReaksiAmonium nitrat bereaksi dengan logam hidroksida, melepaskan amonia dan membentuk alkali logam nitrat:
Amonium nitrat tidak meninggalkan residu ketika dipanaskan:
Amonium nitrat juga terbentuk dalam atmosfer Bumi dari emisi NO, SO2, dan NH3, dan merupakan komponen sekunder dari PM10.[6] BencanaAmonium nitrat terurai menjadi gas dinitrogen oksida dan uap air bila dipanaskan (bukan reaksi eksplosif); namun, dapat diinduksi untuk meluruh secara eksplosif oleh ledakan. Stok bahan yang besar bisa menjadi risiko kebakaran utama karena oksidasi pendukungnya, dan mungkin juga meledak, seperti yang terjadi pada bencana di Texas City pada tahun 1947, yang menyebabkan perubahan besar dalam peraturan untuk penyimpanan dan penanganannya. Dua kelas utama insiden yang mengakibatkan ledakan adalah:
Referensi
Pranala luar
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||