|
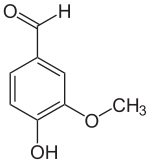
Vanillina
 La vanillina (o vaniglina) è la molecola che conferisce alla vaniglia il suo tipico profumo. Chimicamente è un'aldeide aromatica, precisamente è la 4-idrossi-3-metossibenzaldeide. A temperatura ambiente è un solido cristallino bianco (o giallo tenue se poco pura) dal caratteristico aroma di vaniglia; abbastanza solubile in acqua, si scioglie molto meglio in etanolo (500 g/l a 20 °C) e nei più comuni solventi organici. La vanillina sintetica viene ora utilizzata più spesso dell'estratto di vaniglia naturale come aromatizzante in alimenti, bevande e prodotti farmaceutici.[2] I semi di vaniglia ne contengono una percentuale compresa tra l'1,5% ed il 4%. L'estratto di vaniglia naturale contiene una miscela di diverse centinaia di composti oltre alla vanillina. StoriaLa vaniglia era coltivata nell'America Centrale già in epoca precolombiana; gli europei la scoprirono solo nei primi decenni del Cinquecento, con la conquista del Messico da parte di Hernán Cortés, quando videro che gli aztechi la usavano come un aroma per il cioccolato.[3] Tuttavia fu solo nel 1858 che Nicolas-Theodore Gobley identificò la vanillina come sostanza a sé,[4] mentre nel 1874 i chimici tedeschi Ferdinand Tiemann e Wilhelm Haarmann ne ottennero la prima sintesi di laboratorio producendola a partire dalla coniferina, presto sostituita dal più economico eugenolo, e poi dal guaiacolo.[5][6] 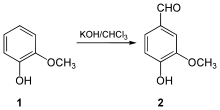 Verso la fine del XIX secolo, la vanillina semisintetica veniva prodotta dall'eugenolo proveniente dall'olio di chiodi di garofano, che fu successivamente soppiantata, negli anni '30, da quella prodotta a partire dagli scarti dell'industria della carta, contenenti lignina.[7] Mentre la vanillina è ancora prodotta a partire dalla lignina, la maggior parte della vanillina sintetica è oggi sintetizzata in un processo a due fasi dai precursori del guaiacolo e acido gliossilico.[3][8] PreparazioneBiosintesiL'esatta biosintesi della vanillina da parte della V. planifolia è sconosciuta, anche se vi sono diverse ipotesi al riguardo. La biosintesi della vanillina generalmente accettata è quella della via fenilpropanoide, a partire dalla L-fenilalanina,[9] che viene deaminata dalla fenilalanina ammoniaca liasi (PAL) per formare acido cinnamico. La posizione para dell'anello viene quindi idrossilata dall'enzima citocromo P450 cinnamato 4-idrossilasi (C4H / P450) per creare acido p-cumarico.[10] Quindi l'enzima 4CL lega l'acido p-cumarico al coenzima A (CoA) per creare la p-cumaroil CoA. L'enzima HCT quindi converte la p-cumaroil CoA in 4-cumaroil shichimato chinato. Questo subisce l'ossidazione dell'enzima P450 che produce il caffeoil shichimato chinato. L'HCT elimina lo shichimato chinato dal CoA per creare il caffeoil CoA e la 4CL rimuove il CoA per produrre l'acido caffeico. L'acido caffeico viene sottoposto a una metilazione dalle COMT per dare acido ferulico. Infine, la vanillina sintasi catalizza l'idratazione del doppio legame nell'acido ferulico che consente la formazione di vanillina.[10] Produzione naturale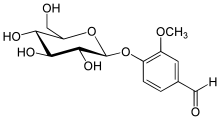 La vanillina naturale è estratta dai baccelli del seme di Vanilla planifolia un'orchidea originaria del Messico, oggi coltivata nelle zone tropicali di tutto il mondo. Il Madagascar è attualmente il più grande produttore di vanillina naturale. Al momento del raccolto, i baccelli verdi contengono vanillina nella forma del suo β-D-glucoside, e sono sprovvisti sia del sapore che dell'odore caratteristico.[11] Dopo essere stati raccolti, il sapore caratteristico viene sviluppato attraverso un processo di stagionatura che dura diversi mesi, i cui metodi variano a seconda dei produttori. In generale i baccelli vengono sbianchiti in acqua calda, per arrestare i processi di deterioramento dei tessuti vegetali. Quindi, per 1-2 settimane, durante il giorno, vengono stesi al sole e ogni notte avvolti in panni e imballati in scatole a tenuta stagna per sudare. Durante questo processo, i baccelli diventano marrone scuro e gli enzimi del baccello rilasciano vanillina come molecola libera. Infine, i baccelli vengono essiccati e ulteriormente invecchiati affinché i sapori si sviluppino ulteriormente.[12] Produzione chimicaLa richiesta di aroma di vaniglia ha di gran lunga superato l'offerta di baccelli di vaniglia. La vanillina in commercio, usata in pasticceria, in profumeria e in quasi tutti i prodotti igienici, è di origine sintetica. La si prepara per ossidazione dell'eugenolo (che si trova nell'olio di chiodi di garofano) con permanganato di potassio o ozono oppure per reazione del guaiacolo con formaldeide in un lento processo che ha tempi di reazione dell'ordine di giorni. Un'altra fonte industriale di vanillina sono gli scarti solforici dell'industria della carta.[11] Questi contengono acido ligninsolfonico che, trattato ad alta temperatura e ad alta pressione con agenti ossidanti e alcalini, si decompone in svariati prodotti, tra cui la vanillina che viene successivamente estratta dalla miscela e purificata per distillazione e cristallizzazione. Si stima che la produzione mondiale di vanillina sintetica sia di circa 12 000 tonnellate l'anno; la vanillina di origine naturale, ottenuta dalle 2 000 tonnellate/anno di semi di vaniglia raccolti nel mondo, ammonta a circa 40 tonnellate l'anno. DistribuzioneLa vanillina è il principale aroma della vaniglia. I baccelli di vaniglia stagionati contengono circa il 2% di vanillina secca; su baccelli di alta qualità, la vanillina relativamente pura può essere visibile come una polvere bianca sulla parte esterna del baccello. Si trova anche nel Leptotes bicolor, una specie di orchidea originaria del Paraguay e del sud del Brasile,[13] e nel pino rosso cinese. A concentrazioni più basse, la vanillina contribuisce al sapore e ai profili aromatici di prodotti alimentari diversi come l'olio di oliva,[14] il burro,[15] il lampone[16] il litchi[17] e altri frutti. L'invecchiamento in botti di rovere impartisce l'aroma di vanillina ad alcuni vini, aceti o bevande alcoliche.[18][19] In altri alimenti, il trattamento termico genera vanillina a partire da altre sostanze chimiche. In questo modo, la vanillina contribuisce al sapore e all'aroma del caffè[20] e dello sciroppo d'acero,[21] e anche di alcuni prodotti integrali quali la farina di avena.[22] UsiLa vanillina viene principalmente usata per coprire gli odori, come l'odore di lievito naturale in pasticceria, e per invogliare al consumo del prodotto, specialmente nei prodotti dolciari.[23] Trova massiccio impiego nell'industria alimentare per aromatizzare i dolci da forno (le cosiddette "merendine"), torte e creme, gelati, liquori, ecc. Sui prodotti in vendita spesso viene semplicemente dichiarata in etichetta sotto la dicitura "aromi" ed è parte della preparazione di molte varietà di cioccolato. In commercio la si trova sotto forma di polvere bianca, venduta in bustine, oppure come liquido da usarsi a gocce, contenuto in fialette. Nella farmacopea antica la vaniglia veniva usata per eccitare il senso di fame e quindi invogliare l'individuo a cibarsi quand'era in condizioni di apatia verso il cibo. Viene utilizzata in laboratorio per la visualizzazione delle macchie sulle lastrine usate in cromatografia su strato sottile. Il reattivo viene preparato sciogliendo la vanillina in etanolo e acido solforico, dopo l'applicazione occorre un riscaldamento; l'utilizzo è specifico per alcoli e chetoni. PrecauzioniLa vaniglia e la vanillina possono causare reazioni allergiche o emicranie in soggetti ipersensibili al prodotto.[24][25] Note
Voci correlateAltri progetti
Collegamenti esterni
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||