|
PoissonPoisson
Nom vulgaire ou nom vernaculaire ambigu :
l'appellation « Poisson » s'applique en français à plusieurs taxons distincts. Mérou géant nageant parmi des bancs d'autres poissons.
Taxons concernés et de la super-classe mais aussi plusieurs espèces parmi les Agnathes.Articles connexes Les poissons sont des animaux vertébrés aquatiques à branchies, pourvus de nageoires et dont le corps est généralement couvert d'écailles. On les trouve abondamment aussi bien en eau douce, en eau saumâtre et en eau de mer, depuis les sources de montagne (omble de fontaine, goujon) jusqu'au plus profond des océans (grandgousier, poisson-ogre). Leur répartition est toutefois très inégale : 50 % des poissons vivraient dans 17 % de la surface des océans[1]. Les poissons ont une très grande importance pour les humains :
Dans la classification phylogénétique[2], obtenue par application des méthodes cladistiques, les poissons forment un groupe paraphylétique de vertébrés, donc non reconnu, car il exclut les tétrapodes (vertébrés terrestres). La super-classe des Poissons (les Pisces) de la classification classique n'est reconnue que par certains systématiciens évolutionnistes[3]. Les espèces actuelles (non éteintes) de poissons sont réparties dans quatre taxons : les Pétromyzontides (lamproies), les Chondrichtyens (raies, requins et chimères), les Actinoptérygiens (poissons les plus communs), les Sarcoptérygiens (Dipneustes et Actinistiens). On y associe parfois les Myxinoïdes. Le premier inventaire ichtyologique de France semble être celui de Pierre Belon, en 1555, La nature et la diversité des poissons avec leurs pourtraicts représentés au plus près du naturel[4]. Définition et classificationÉtymologieLe substantif masculin[5],[6],[7] poisson (prononcé : [pwasɔ̃] en français standard)[6] est issu, par l'intermédiaire de l'ancien français peis, pois, du latin piscis, de même sens[5],[6]. Définition Le terme poisson est plus précisément employé pour désigner les crâniates non tétrapodes, c'est-à-dire des animaux avec un crâne cartilagineux ou osseux qui protège la partie antérieure du système nerveux, possédant des branchies toute leur vie et qui peuvent posséder des nageoires, mais pas de pattes[8]. Les poissons ne forment pas un groupe phylogénétiquement homogène, contrairement aux oiseaux ou aux mammifères (voir plus bas). Un poisson typique est « à sang froid » ; il possède un corps allongé lui permettant de nager rapidement ; il extrait le dioxygène de l'eau en utilisant ses branchies ; il possède deux paires de nageoires, les nageoires pelviennes et les nageoires latérales, habituellement une ou deux nageoires dorsales, une nageoire anale et une nageoire caudale ; il possède une mâchoire double, pour les gnathostomes, ou simple, pour les agnathes ; sa peau est généralement recouverte d'écailles ; il est ovipare.  Chacune de ces caractéristiques comporte toutefois des exceptions. Les thons, les espadons et certaines espèces de requins sont entre sang chaud et sang froid, et peuvent élever leur température corporelle au-dessus de celle de l'eau ambiante[9]. Et de la même façon, la lampris-lune semble être un cas unique de poisson à sang chaud. La forme du corps et les performances natatoires varient considérablement, des nageurs très rapides capables de parcourir dix à vingt longueurs de leur corps par seconde (thons, saumons) aux poissons très lents mais mieux manœuvrants (comme les anguilles ou les raies) qui ne dépassent pas 0,5 longueur par seconde[10]. Plusieurs groupes de poissons d'eau douce extraient le dioxygène de l'air comme de l'eau en utilisant des organes variés. Les dipneustes possèdent deux poumons similaires à ceux des tétrapodes ; les gouramis ont un « organe labyrinthe » qui fonctionne de la même manière ; les Corydoras extraient le dioxygène par l'estomac ou l'intestin[11]. La forme du corps et la position des nageoires varient énormément, comme en témoigne la différence entre les hippocampes, les lophiiformes, les poissons globes ou les saccopharyngiformes. De même, la surface de la peau peut être nue (murènes) ou couverte d'écailles de différents types : placoïdes (requins et raies), cosmoïdes (cœlacanthes), ganoïdes, cycloïdes et cténoïdes[12]. Certains poissons passent même davantage de temps hors de l'eau que dedans, comme les périophthalmes qui se nourrissent et interagissent entre eux sur des terrains boueux et ne retournent dans l'eau que pour se cacher dans leur terrier[13]. Certaines espèces peuvent être ovovivipares ou vivipares. Le poisson le plus petit (Schindleria brevipinguis) mesure à peine 8 mm, le plus grand (le requin baleine) atteint 16 m. Quelques espèces de poissons dulçaquicoles possèdent des poumons. Ces organes permettent aux Erythrinus de l'Amazone d’extraire 50 % du dioxygène dont ils ont besoin, et sont l'unique moyen de respiration des Arapaima gigas ou des gymnotes. TerminologiePlusieurs types d'animaux aquatiques sont communément appelés « poissons » mais n'en sont pas vis-à-vis de la définition précédente. Les termes relatifs aux poissons viennent de différentes racines :
ClassificationÀ l'opposé des groupes tels que les oiseaux ou les mammifères, les poissons ne forment pas un clade : le groupe est paraphylétique, c'est-à-dire qu'il ne comporte pas tous les descendants de leur ancêtre commun[14],[15],[16]. Pour cette raison, la « super-classe Pisces » n'est plus utilisée en classification phylogénétique, chaque clade devant comporter tous les descendants du même ancêtre, ce qui amènerait à y adjoindre les Tétrapodes. Elle est par contre conservée dans certaines classifications évolutionnistes modernes[3]. Les poissons sont classés dans les groupes principaux suivants (en grisé et précédés de l'obèle « † », les taxons éteints) :
Certains paléontologues considèrent que les conodontes sont des chordés et les considèrent comme des poissons primitifs ; voir l'article Vertébré. Les différents groupes de poissons pris tous ensemble comprennent plus de la moitié des vertébrés connus. Il y a près de 28 000 espèces de poissons existantes (sans compter les espèces disparues), dont près de 27 000 poissons osseux, le reste étant formé d'environ 970 requins, raies et chimères et environ 108 lamproies et myxines[17]. Un tiers de toutes ces espèces est renfermé dans les neuf plus grandes familles, qui sont (des plus grandes aux plus petites) : Cyprinidae, Gobiidae, Cichlidae, Characidae, Loricariidae, Balitoridae, Serranidae, Labridae, et Scorpaenidae. D'un autre côté, environ 64 familles sont monotypiques (ne contiennent qu'un seul genre, parfois monospécifique). On suppose que le nombre total d'espèces de poissons en existence serait de 32 500[17]. GénomiqueLes poissons contemporains sont les vertébrés chez lesquels on observe les plus grands et les plus petits génomes (parmi les vertébrés), phénomène qui a une « signification évolutive » encore incomprise[18]. Le génome est plus petit chez les poissons à nageoires à rayons que chez les poissons cartilagineux, hormis chez les polyploïdes (qui explique en grande partie les variations de taille de génome au sein de ces deux groupes)[18]. Le génome des poissons d'eau douce (et eurybiontes) est plus grand que celui des espèces apparentées marines et sténobiontes[18]. Les différences de taille de génome ne semblent pas liées au taux métabolique propre à l'espèce mais elles sont positivement corrélées avec la taille des œufs, ce qui peut évoquer un lien avec l'évolution des soins parentaux[18]. Évolution  De par leur diversité morphologique, physiologique, comportementale et écologique, les poissons représentent un remarquable succès évolutif[21]. Dans un contexte évolutif, l'ensemble des taxons désignés par le terme poisson n'est plus considéré homogène, ces taxons ayant des histoires évolutives différentes et formant donc différents clades[2]. Certains pensent que les poissons ont évolué à partir d'une créature du type ascidie (dont les larves ont des ressemblances avec les poissons primitifs) ; les premiers ancêtres des poissons auraient alors conservé leur forme larvaire à l'état adulte par néoténie, mais l'inverse est aussi possible. Les fossiles candidats au statut de « premier poisson » connus sont Haikouichthys, Myllokunmingia et Pikaia. Les tout premiers fossiles de poissons ne sont guère nombreux, ni de bonne qualité : peut-être les poissons primitifs étaient-ils rares ou mal fossilisables ou les conditions taphonomiques mauvaises. Cependant, le poisson devint une des formes de vie dominantes du milieu aquatique et a donné naissance aux branches évolutives menant aux vertébrés terrestres comme les amphibiens, les reptiles et les mammifères. L'apparition d'une mâchoire articulée semble être la raison majeure de la prolifération ultérieure des poissons, car le nombre d'espèces de poissons agnathes devint très faible. Les premières mâchoires ont été trouvées dans les fossiles de placodermes. On ignore si le fait de posséder une mâchoire articulée procure un avantage, par exemple, pour la préhension ou la respiration. Les poissons ont aussi coévolué avec d'autres espèces (prédateurs, pathogènes et parasites notamment, mais aussi parfois des espèces symbiotes). Durant leurs migrations (longues et sur de longues distances pour les saumons et lamproies, et plus encore pour les anguilles), ils peuvent transporter (dispersion) un certain nombre de propagules d'autres organismes (ectoparasitisme, endozoochorie, œufs viables non digérés[22], etc.). AgnathesLes agnathes regroupent des animaux à corde dorsale et à crâne, mais sans mâchoires. Leur vie en milieu aquatique les a fait longtemps classer parmi les poissons. La monophylie des agnathes actuels est débattue[23],[24],[3] :
La plupart des études récentes basées sur les comparaisons de séquences d'ADN soutiennent que les myxines et les lamproies sont étroitement apparentées. On parlera alors du groupe des cyclostomes[23]. Les myxines et lamproies partagent des caractères morphologiques ancestraux à tous les craniés, qui sont perdus chez les gnathostomes. Leur bouche rudimentaire, qui se comporte comme une ventouse, ne possède pas de mâchoires, et ne peut donc pas modifier son ouverture. Leur squelette est cartilagineux et composé d'une capsule crânienne et d'une colonne vertébrale sans côtes. Si les agnathes actuels sont peu nombreux, de nombreux fossiles d'agnathes sont présents dans les sédiments du paléozoïque. Les agnathes furent les tout premiers crâniates à apparaître. Poissons cartilagineux (Chondrichtyens) Chez les Chondrichthyens, aussi appelés « poissons cartilagineux », il n'y a globalement pas d'ossification endochondrale. Le squelette est donc très majoritairement composé de cartilage, et pas d'« os vrai »[2]. On peut y trouver les différentes espèces de requins, de raies et de chimères. Il faut ajouter que les « os vrais » peuvent tout de même être observés chez les Chondrichtyens, mais en petite quantité[25]. La généralisation de l'os enchondral ne se trouvera que chez les ostéichtyens, étant par ailleurs leur synapomorphie principale. Les principales synapomorphies des chondrichthyens incluent une couche de cartilage calcifié prismatique et, chez les mâles, les nageoires pelviennes portent des claspers pelviens (organes servant à l'accouplement)[2]. Poissons osseux (Ostéichtyens au sens classique) Comme leur nom l'indique, l'innovation la plus notable des poissons osseux est l'os. Le tissu osseux périchondral qui renforçait certains cartilages se généralise, et conduit à deux types d'os d'origines différentes :
On observe aussi la présence de sacs aériens connectés au tube digestif qui donneront les poumons des vertébrés terrestres et les vessies natatoires des Actinoptérygiens. Ces sacs aériens sont soupçonnés chez certains Gnathostomes fossiles. Les tentatives d'émancipation du milieu aquatique seraient alors apparues dans ce clade. Les principales fonctionnalités évolutives explorées au niveau des poissons osseux sont l'articulation de la mâchoire, de plus en plus structurée, et la forme et la mobilité des nageoires. Poisson à nageoires charnues (Sarcoptérygiens) On peut par exemple compter comme poissons à nageoires charnues (sarcoptérygiens) les cœlacanthes, les dipneustes ou encore les tétrapodes. Plusieurs innovations se retrouvent dans ce groupe :
Il apparait donc évident, vu les membres de ce groupe, que pour rendre holophylétique le groupe des poissons (c'est-à-dire pour qu'il contienne tous les descendants de son dernier ancêtre commun, et donc le considérer valide du point de vue cladiste), il faudrait y inclure tous les vertébrés terrestres dont les humains font évidemment partie. Certains évolutionnistes ont souligné que l'idée d'appeler l'homme un poisson était absurde et qu'il était donc préférable d'accepter comme valides les groupes paraphylétiques[26]. Morphologie et anatomieMorphologieAspect général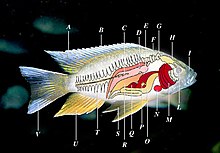 A Nageoire dorsale B Rayon C Ligne latérale D Rein E Vessie natatoire F Appareil de Weber G Oreille interne H Cerveau I Narine L Orbite M Branchie N Cœur O Estomac P Vésicule biliaire Q Rate R Gonades S Nageoire ventrale ou pelvienne (par paire) T Colonne vertébrale U Nageoire anale V Nageoire caudale.  1 Opercule 2 Ligne latérale 3 Nageoire dorsale 4 Nageoire molle ou adipeuse 5 Pédoncule caudal ou queue 6 Nageoire caudale 7 Nageoire anale 8 Photophores 9 Nageoire ventrale ou pelvienne (par paire) 10 Nageoire pectorale (par paire) Épiderme  Les cellules épidermiques sont toutes vivantes, éliminations sans modification, elles tombent. Peu épais (5 -9 couches cellulaires), il y a des échanges osmotiques et ioniques. Certains poissons pélagiques développent sur leur épiderme une coloration à fort contraste dorso-ventral. L'interprétation la plus classique est qu'il s'agirait d'une coloration cryptique permettant une sorte de camouflage anti-prédateur baptisée ombre inversée : la coloration sombre dorsale leur permet de se confondre avec les fonds marins et les rend moins visibles d'un prédateur aviaire ; la coloration blanche du ventre aurait une valeur adaptative, en les rendant moins visibles d'un prédateur venant des profondeurs (requin, thon) qui est ébloui par la luminosité des rayons solaires (confusion avec la lumière ambiante à travers la fenêtre de Snell)[28]. Nageoires La plupart des poissons se déplacent en contractant alternativement les muscles insérés de chaque côté de la colonne vertébrale. Ces contractions font onduler le corps de la tête vers la queue. Lorsque chaque ondulation atteint la nageoire caudale, la force propulsive créée pousse le poisson vers l'avant. Les nageoires du poisson sont utilisées comme stabilisateurs. La nageoire caudale sert aussi à augmenter la surface de la queue, augmentant ainsi la poussée lors de la nage, et donc la vitesse. Le corps fuselé des poissons permet de diminuer les frictions lorsqu'ils nagent, et donc d'éviter qu'ils soient ralentis par la résistance de l'eau. De plus, leurs écailles sont enrobées d'un mucus qui diminue les frottements. AlimentationPresque toutes les formes d'alimentation sont observées chez les poissons, mais les modes parasitaires semblent rares ou inexistants (la lamproie n'est pas un poisson au sens taxonomique le plus restrictif du terme). Le régime alimentaire d'une espèce mal connue ou nouvellement découverte peut être étudié par des analyses du contenu stomacal et des analyses isotopiques. Des cailloux, microplastiques, et parfois du sédiment et des os ou écailles de poissons sont souvent trouvés dans les estomacs de poissons (une étude ayant porté sur 5 000 estomacs de poissons appartenant à plus de 70 espèces démersales différentes, échantillonnés à intervalles bathymétriques de 250 m au nord-est de l'océan Atlantique, à des profondeurs allant de 500 à 2 900 m[29]. Des cailloux ou graviers n'ont été trouvés que dans les estomacs de poissons pêchés à 500–1000 m de profondeur (taux : 4,6 % à 500 m de profondeur, 1,1 % à 750 m et 1,3 % à 1 000 m[29]. Des sédiments étaient présents dans 9 % des estomacs et des écailles chez 7 % des poissons, des estomacs avec des contenus. Sédiments et échelles co-produites dans l'estomac des poissons d'alimentation principalement benthopélagiques[29]. AnatomieÉcologie et comportementComportement social De nombreuses espèces de poissons, tels les demoiselles (Pomacentridés), les poissons-zèbres (Cyprinidés) ou les néons (Characidés), etc. ont un instinct grégaire et préfèrent vivre en bancs. D'autres, tels les requins, sont plutôt solitaires. Certains sont même si agressifs que la rencontre d'un congénère peut entraîner la mort de l'un d'eux après une rude bataille : c'est le cas du combattant du Siam (Anabantidés) chez les mâles. La plupart des poissons sont ovipares : la femelle dépose ses ovules et le mâle les féconde, de manière externe ; cependant, certains poissons sont ovovivipares, comme de nombreux requins, et il y a alors un accouplement avec fécondation interne. Certains s'occupent de leurs œufs ou de leurs petits (protégés dans la bouche des parents chez certaines espèces comme celles de la famille des Apogonidae, ou dans une poche ventrale du mâle chez les hippocampes) et d'autres (qui pondent beaucoup plus d’œufs) abandonnent leurs œufs à leur sort, dans l'eau ou sur un support. Dans les années 2010, des études scientifiques relèvent chez plusieurs espèces une sensibilité et des comportements sociaux plus complexes qu'imaginés jusqu'alors[30]. Par exemple, des raies manta ont démontré des comportements associés avec la conscience de soi. Placés dans un test du miroir, les individus ont démontré un comportement inhabituel, apparemment destiné à vérifier si le comportement de leur reflet correspond toujours à leurs propres mouvements[31]. Des labres nettoyeurs ont également passé le test du miroir dans une expérience indépendante, réalisée en 2018[32],[33]. Des cas d'usages d'outils chez les poissons ont également été mentionnés, notamment chez des poissons de la famille des choerodons, ceux du genre Toxotes et chez la morue de l'Atlantique[34]. En 2019, des chercheurs ont démontré que les Amatitlania siquia, une espèce de poisson monogame, développent une attitude pessimiste quand ils sont privés de la présence de leur partenaire[35],[36]. CyclesLa plupart des poissons ont un cycle nycthéméral (et dorment la nuit[37], en pleine eau ou posés sur un substrat, parfois couchés sur le flanc) et saisonnier. Certains ont une activité plutôt nocturne. De nuit, en aquarium comme dans la nature, certains poissons changent de couleur[37],[38]. Des changements électriques du cerveau passant en phase de sommeil ou d'éveil montrent ces changements (8–13 Hz dans le noir, 18–32 Hz à la lumière chez la morue) proches de ceux observées chez les mammifères[37]. MigrationLa migration est un phénomène instinctif[39] présent chez de nombreuses espèces de poissons. Peu de poissons sont absolument sédentaires, hors quelques espèces coralliennes ou vivant dans des eaux fermées. La plupart des espèces marines et de rivière, accomplissent (individuellement ou de manière grégaire) des déplacements saisonniers ou migratoires. Beaucoup de poissons migrent de manière cycliquement régulière (à l'échelle du jour ou de l'année), sur des distances de quelques mètres à des milliers de kilomètres, en relation avec les besoins de reproduction ou en nourriture, les conditions de température ; dans certains cas, le motif de la migration n'est pas connu. Contribution aux puits de carboneÀ partir du dioxyde de carbone dissous dans l'eau, les poissons marins produisent constamment dans leur intestin des carbonates peu solubles. Par exemple, le flet européen synthétise et rejette chaque heure et en moyenne 18 micromoles de carbone par kg de poisson (sous forme de calcite)[1]. Les poissons contribueraient ainsi de 3 %[40] à 15 %[41] du puits de carbone océanique (voire 45 % si l'on prenait les hypothèses les plus « optimistes »)[1]. De plus, les poissons ont une marge de tolérance à la température[42] et un climat chaud associé à la surpêche tendent à réduire le nombre de grands poissons ; or, une petite taille du poisson et une eau plus chaude favoriseraient cette formation de carbonates de calcium ou de magnésium (qui sont éliminés avec la nécromasse, les fèces ou des boulettes de mucus)[1]. Hélas, ces carbonates plus riches en magnésium sont aussi plus solubles à grande profondeur. Ils peuvent alors relarguer une partie de leur carbone, mais en tamponnant le milieu, au point que cela pourrait expliquer jusqu'à un quart de l'augmentation de l'alcalinité titrable des eaux marines dans les 1 000 mètres sous la surface (cette anomalie de dureté de l'eau était jusqu'ici controversée car non expliquée par les océanographes)[1]. Hélas encore, c'est aussi dans les zones les plus favorables à ce piégeage du carbone (plateaux continentaux où se concentre environ 80 % de la biomasse en poisson) que la surpêche est la plus intense et que les zones mortes ont fait disparaître le plus de poissons. Les poissons et l'HommeUtilisation alimentaireLe poisson est un aliment consommé par de nombreuses espèces animales, dont l'Homme. Le mot poisson désigne donc aussi un terme de cuisine faisant référence à l'ensemble des aliments préparés à partir de poissons capturés par le biais de la pêche ou de l'élevage. Trois quarts de la planète Terre sont couverts d'eau et de nombreuses rivières sillonnent l'intérieur des terres, ce qui fait que le poisson a fini par constituer, depuis la nuit des temps, une partie importante du régime alimentaire des humains dans presque tous les pays du monde. Surpêche Pour les poissons comestibles comme la morue et le thon, la menace principale est la surpêche[43],[44]. Lorsque la surpêche persiste, elle finit par causer une diminution de la population de poissons (le « stock ») car les individus ne peuvent pas se reproduire assez vite pour compenser la perte due à la pêche. Un exemple de surpêche catastrophique très étudié est celui de la sardine du Pacifique (Sadinops sagax caeruleus), qui était pêchée près des côtes de Californie. Le maximum avait été atteint en 1937 avec 790 000 tonnes, puis la quantité pêchée a décru pour atteindre à peine 24 000 t en 1968, date à laquelle cette industrie s'arrêta faute d'être rentable. Une telle « extinction commerciale » ne veut pas dire que l'espèce elle-même est éteinte, mais seulement qu'elle n'est plus économiquement viable[45]. La pêche minotière a également localement conduit à la surpêche. La principale source de tension entre l'industrie de la pêche et la science halieutique est la recherche d'un équilibre entre la conservation des espèces pêchées, et la préservation du revenu des pêcheurs. Dans des zones comme l'Écosse, Terre-Neuve ou l'Alaska, où l'industrie des pêches est le principal employeur, le gouvernement est particulièrement impliqué dans cet équilibre[46], en maintenant à la fois un stock suffisant et des ressources suffisantes pour les pêcheurs. D'un autre côté, les scientifiques promeuvent une protection toujours accrue pour les stocks, en prévenant que de nombreux stocks pourraient disparaitre dans les cinquante prochaines années[47]. Selon le WWF, « 80 % des stocks mondiaux de poissons utilisés à des fins commerciales sont déjà surpêchés ou menacés de l’être. Par ailleurs, 40 % de tous les animaux marins capturés finissent comme prises accessoires et sont rejetés morts ou moribonds par-dessus bord. Et comme le poisson d’élevage est le plus souvent nourri avec de l’huile de poisson et/ou de la farine de poisson, les élevages contribuent également au pillage des mers »[48]. Pollution de l'eau, des sédiments et destruction des habitats Les poissons sont notamment vulnérables à de nombreux polluants (plomb, mercure et autres métaux, insecticides...) et à des problèmes de féminisation (imposex) induits par des perturbateurs endocriniens[49]. Une des menaces sur les écosystèmes (marins et d'eau douce) est la dégradation physique, chimique et écologique des habitats ; celle-ci est causée par la pollution de l'eau, la construction de grands barrages, le réchauffement, l'eutrophisation, l'acidification et la baisse du niveau d'eau par les activités humaines, et doivent faire face à la concurrence et aux pathogènes d'espèces introduites[50]. Un exemple de poisson en danger à cause d'un habitat modifié est l'Esturgeon blanc, vivant dans les cours d'eau en Amérique du Nord, ceux-ci ayant été modifiés de différentes manières[51]. Espèces exotiques envahissantes L'introduction d'espèces exotiques dont beaucoup sont devenues invasives s'est produite à de nombreux endroits et pour de nombreuses raisons, dont le ballastage des navires de commerce. Un exemple bien connu et étudié est l'introduction de la perche du Nil dans le lac Victoria. À partir des années 1960, la perche du Nil introduite pour la pêche a progressivement exterminé les 500 espèces de cichlidés que l'on ne trouvait nulle part ailleurs que dans ce lac ; certaines espèces ne survivent que grâce à des programmes de reproduction en captivité, mais d'autres sont probablement éteintes[52]. Parmi les espèces de poissons invasives ayant causé des problèmes écologiques, on peut noter les carpes, les tête-de-serpent, les tilapias, la perche européenne, la truite fario, la truite arc-en-ciel ou la lamproie marine. Conservation En 2006, la liste rouge de l'UICN comprenait 1 173 espèces de poissons menacées d'extinction[53]. Cette liste incluait des espèces comme la morue de l'Atlantique, le Cyprinodon diabolis, les cœlacanthes ou le grand requin blanc. Comme les poissons vivent sous l'eau, ils sont plus compliqués à étudier que les animaux terrestres ou les plantes, et on manque toujours d'informations sur les populations de poissons. Les poissons d'eau douce semblent particulièrement menacés, car ils vivent souvent dans des zones restreintes. Mesures de protectionOn cherche à établir des indicateurs ou indices de biodiversité en poissons, notamment pour les milieux d'eau douce, lacs[54] et mares y compris. Vers un usage éthique des poissonsDe nombreuses études ont porté sur la douleur[55],[56],[57] la souffrance[58],[59], l’évitement de la douleur[60],[61], la peur[62],[63] telle que perçue par les poissons, sur la composante d’affectivité ou de personnalité qu’ils expriment[64], des états apparentés à des émotions[65], ou sur leur bien-être en pisciculture[66],[67] ou en aquarium, avec des conclusions parfois opposées. Ces questions ont des enjeux juridiques et éthiques car les pays développés tendent à introduire de l’éthique animale et environnementale dans leurs législations (par ex en Suisse depuis 2005 : « personne ne doit de façon injustifiée causer à des animaux des douleurs, des maux ou des dommages, les mettre dans un état d’anxiété ou porter atteinte à leur dignité d’une autre manière. Il est interdit de maltraiter les animaux, de les négliger ou de les surmener inutilement », tout comme sont interdites « les autres pratiques sur des animaux qui portent atteinte à leur dignité »[68]). Dans la cultureRecordsTailleLe Paiche d'Amazonie, ou Arapaïma, est le plus gros poisson dulçaquicole : il peut atteindre 4,5 m et 200 kg. Le plus gros poisson connu est le requin-baleine (16 m, 10 t). Selon les Proceedings of the Royal Society (janvier 2006), le plus petit poisson serait Paedocypris progenetica, un cyprinidé d'eau douce découvert par Maurice Kottelat et Tan Heok Hui, du Raffles Museum (Singapour). La femelle Paedocypris est mature à partir de 7,9 mm de long. Adultes, les femelles mesurent 10,3 mm et les mâles, 11,4 mm. Il détrône un gobie nain de l'océan Indien décrit en 1981, Trimmatom nanus, adulte à 8 mm. Un poisson du même genre, Paedocypris micromethes, légèrement plus grand (femelle adulte à partir de 8,8 mm), a été identifié à Sarawak. Ces poissons vivent dans les forêts marécageuses constituées d'arbres inondés poussant sur un sol de tourbe détrempée, mou et épais de plusieurs mètres. L'eau y est rouge sombre et très acide. Selon une équipe de l'université de Washington, Photocorynus spiniceps est le plus petit vertébré connu : le mâle de cette espèce de baudroie de la famille des Linophrynidae, découverte dans les abysses du large des Philippines, long de seulement 6,2 mm, vit en parasite sur le dos d'une femelle mesurant 46 mm. Celle-ci pourvoit aux besoins en nourriture d'un mâle ne se limitant pratiquement qu'à un appareil reproducteur (Pietsch et al., Ichtyological Research, 2005[77]). Si le mâle Photocorynus spiniceps est plus petit, notons que Paedocypris progenetica détient, en moyenne mâle-femelle, le record du plus petit poisson connu (même s'il n'est plus le plus petit vertébré depuis la description en 2012 de la grenouille Paedophryne amauensis[78]). PuissanceDunkleosteus terrelli, un poisson marin à plaques cuirassées qui vivait il y a 400 Ma, mesurait jusqu'à 11 m de long et pouvait peser jusqu'à quatre tonnes. Après en avoir reconstitué la musculature, des scientifiques américains ont découvert en 2006 que les mâchoires de ce poisson étaient capables d'exercer une pression de 5 500 kg/cm2, soit à peu près deux fois celle de l'actuel requin blanc et autant que la mâchoire d'un Tyrannosaurus. De surcroît, on estime que Dunkleosteus terrelli était capable d'ouvrir et de refermer sa gueule en un cinquantième de seconde (Philip Anderson et Mark Westneat, 2006). Notes et références
AnnexesBibliographie
Articles connexesLiens externes
|

