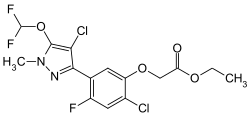
| Strukturformel
|
|
| Allgemeines
|
| Name
|
Pyraflufen-ethyl
|
| Andere Namen
|
Ethyl-2-chlor-5-(4-chlor-5-difluormethoxy-1-methylpyrazol-3-yl)-4-fluorphenoxyacetat (IUPAC)
|
| Summenformel
|
C15H13Cl2F3N2O4
|
| Kurzbeschreibung
|
farbloser geruchloser Feststoff[1]
|
| Externe Identifikatoren/Datenbanken
|
|
|
| Eigenschaften
|
| Molare Masse
|
413,18 g·mol−1
|
| Aggregatzustand
|
fest[1]
|
| Dichte
|
1,565 g·cm−3[1]
|
| Schmelzpunkt
|
126,4–127,2 °C[1]
|
| Dampfdruck
|
4,3·10−9 Pa (20 °C)[1]
|
| Löslichkeit
|
- praktisch unlöslich in Wasser (0,082 mg·l−1 bei 20 °C)[1]
- löslich in n-Heptan, Aceton und Ethylacetat[1]
|
| Sicherheitshinweise
|
|
|
| Toxikologische Daten
|
>5.000 mg·kg−1 (LD50, Ratte, oral)[1]
|
| Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa).
|
Pyraflufen-ethyl ist eine chemische Verbindung aus der Gruppe der Phenylpyrazole. Es handelt sich um den Ethylester von Pyraflufen[4][5].
Gewinnung und Darstellung
Pyraflufen-ethyl kann ausgehend von 5-(Ethoxycarbonylmethoxy)benzoylacetat durch Cyclokondensation mit Methylhydrazin zu 3-Aryl-5-hydroxypyrazol, welches durch O-Difluormethylierung und Chlorierung mit Phosphorpentachlorid zum Endprodukt umgesetzt wird, gewonnen werden.[6]
Eigenschaften
Pyraflufen-ethyl ist ein farbloser geruchloser Feststoff, der praktisch unlöslich in Wasser ist. Er ist stabil unter sauren Bedingungen, hydrolysiert jedoch langsam unter neutralen und rasch unter alkalischen Bedingungen.[1]
Verwendung
Pyraflufen-ethyl wird als Wirkstoff in Pflanzenschutzmitteln verwendet.[2] Es wird als Entlaubungsmittel für Baumwolle und Kartoffeln sowie zur Bekämpfung von bestimmten breitblättrigen Unkräutern in Baumwolle, Mais, Sojabohnen, Weizen und auf nicht-landwirtschaftlichen Flächen eingesetzt. Es wirkt durch Hemmung der Protoporphyrinogen-IX-Oxidase verursacht Schäden in den Zellmembranen.[7]
Zulassung
Ein Antrag auf Zulassung der Verbindung in der Europäischen Union wurde am 16. Juni 1997 in Belgien von der Nihon Nōyaku eingereicht. Pyraflufen-ethyl wurde 2001 für Anwendungen als Herbizid zugelassen.[8]
In Österreich und der Schweiz sind Pflanzenschutzmittel mit diesem Wirkstoff im Handel.[9]
Weblinks
Einzelnachweise
- ↑ a b c d e f g h i EU: Review report for the active substance pyraflufen-ethyl (PDF; 302 kB), 2. Juli 2002.
- ↑ a b c Eintrag zu Pyraflufen-Ethyl in der GESTIS-Stoffdatenbank des IFA, abgerufen am 12. April 2023. (JavaScript erforderlich)
- ↑ Eintrag zu 2-chloro-5-(4-chloro-5-difluoromethoxy-1-methylpyrazol-3-yl)-4-fluorophenoxyacetic acid ethyl ester im Classification and Labelling Inventory der Europäischen Chemikalienagentur (ECHA), abgerufen am 1. August 2016. Hersteller bzw. Inverkehrbringer können die harmonisierte Einstufung und Kennzeichnung erweitern.
- ↑ Externe Identifikatoren von bzw. Datenbank-Links zu Pyraflufen: CAS-Nr.: 129630-17-7, EG-Nr.: 620-437-6, ECHA-InfoCard: 100.149.228, GESTIS: 535084, PubChem: 15672202, ChemSpider: 10619119, Wikidata: Q27274790.
- ↑ Generaldirektion Gesundheit und Lebensmittelsicherheit der Europäischen Kommission: EU-Pestiziddatenbank; Eintrag in den nationalen Pflanzenschutzmittelverzeichnissen der Schweiz, Österreichs und Deutschlands, abgerufen am 6. April 2023.
- ↑ Peter Böger, Ko Wakabayashi: Peroxidizing Herbicides. Springer, 1999, ISBN 3-540-64550-0, S. 43 (eingeschränkte Vorschau in der Google-Buchsuche).
- ↑ CALIFORNIA DEPARTMENT OF PESTICIDE REGULATION: PUBLIC REPORT 2004-4 for Pyraflufen-ethyl (PDF; 94 kB).
- ↑ Richtlinie 2001/87/EG (PDF) der Kommission vom 12. Oktober 2001 zur Änderung des Anhangs I der Richtlinie 91/414/EWG des Rates über das Inverkehrbringen von Pflanzenschutzmitteln zur Aufnahme der Wirkstoffe Acibenzolar-s-methyl, Cyclanilide, Eisen(III)-phosphat, Pymetrozin und Pyraflufen-ethyl.
- ↑ Generaldirektion Gesundheit und Lebensmittelsicherheit der Europäischen Kommission: Eintrag zu Pyraflufen-ethyl in der EU-Pestiziddatenbank; Eintrag in den nationalen Pflanzenschutzmittelverzeichnissen der Schweiz, Österreichs (Eingabe von „Pyraflufen-ethyl“ im Feld „Wirkstoff“) und Deutschlands, abgerufen am 12. März 2016.

