|
Непротеїногенні амінокислоти У біохімії некодовані або непротеїногенні амінокислоти відрізняються від 22 протеїногенних амінокислот (21 в еукаріот [1]), які природним чином закодовані в геномі організмів для формування білків. Проте понад 140 непротеїногенних амінокислот зустрічаються в білках природним шляхом, і тисячі інших можуть зустрічатися в природі або синтезуватися в лабораторії. [2] Хімічно синтезовані амінокислоти можна назвати неприродними амінокислотами. Неприродні амінокислоти можуть бути отримані синтетичним шляхом з їхніх нативних аналогів за допомогою модифікацій, таких як алкілування аміном, заміна бічного ланцюга, циклізація подовження структурного зв’язку та ізостерична заміна в амінокислотному скелі. [3] Багато непротеїногенних амінокислот є важливими:
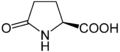
Означення шляхом заперечення Технічно будь-яка органічна сполука з функціональною групою аміну (–NH 2 ) і карбонової кислоти (–COOH) є амінокислотою. Протеїногенні амінокислоти є невеликою підмножиною цієї групи, яка має центральний атом вуглецю (α- або 2-), що містить аміногрупу, карбоксильну групу, бічний ланцюг і α-водневу ліву конформацію, за винятком гліцину, який є ахіральний, і пролін, аміногрупа якого є вторинним аміном і, отже, часто згадується як імінокислота з традиційних причин, хоча і не є імінокислотою. Генетичний код кодує 20 стандартних амінокислот для включення в білки під час трансляції. Однак є дві додаткові протеіногенні амінокислоти: селеноцистеїн і піролізин . Ці нестандартні амінокислоти не мають виділеного кодону, але додаються замість стоп-кодону, коли присутня певна послідовність, кодон UGA та елемент SECIS для селеноцистеїну, [6] послідовність UAG PYLIS для піролізину. [7] Усі інші амінокислоти називаються «непротеїногенними».
Існують різні групи амінокислот: [8]
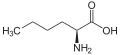
Ці групи перетинаються, але не є ідентичними. Усі 22 протеїногенні амінокислоти біосинтезуються організмами, і деякі, але не всі, з них також є абіотичними (виявлені в пребіотичних експериментах і метеоритах). Деякі природні амінокислоти, такі як норлейцин, помилково включаються в білки під час трансляції через порушення процесу синтезу білка. Багато амінокислот, таких як орнітин, є метаболічними проміжними продуктами, що виробляються біосинтетично, але не включені трансляційно в білки. Посттрансляційна модифікація амінокислотних залишків у білках призводить до утворення багатьох білкових, але непротеїногенних амінокислот. Інші амінокислоти містяться виключно в абіотичних сумішах (наприклад, α-метилнорвалін). Більше 30 неприродних амінокислот було включено у білок під час трансляції синтетичним шляхом, але вони не є біосинтетичними. [8] НоменклатураНа додаток до системи нумерації IUPAC для диференціації різних атомів вуглецю в органічній молекулі шляхом послідовного присвоєння номера кожному вуглецю, включаючи ті, що утворюють карбоксильну групу, атоми вуглецю вздовж бічного ланцюга амінокислот також можна позначати грецькими літерами., де α-вуглець є центральним хіральним вуглецем, що має карбоксильну групу, бічний ланцюг і, в α-амінокислотах, аміногрупу – вуглець у карбоксильних групах не враховується. [9] (Отже, назви IUPAC багатьох непротеїногенних α-амінокислот починаються з 2-аміно- і закінчуються на -інова кислота .) Природні не- L -α-амінокислотиБільшість природних амінокислот є α-амінокислотами в L- конфігурації, але існують деякі винятки. Не альфа Деякі не-α-амінокислоти існують в організмах. У цих структурах амінна група зміщується далі від кінця карбонової кислоти молекули амінокислоти. Таким чином, β-амінокислота має аміногрупу, приєднану до другого вуглецю, а γ-амінокислота має її на третьому. Приклади включають β-аланін, ГАМК і δ- амінолевулінову кислоту.
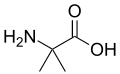
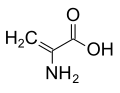
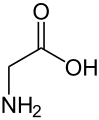
Причина, чому α-амінокислоти використовуються в білках, пов’язана з їх пошиерністю в метеоритах і пребіотичних експериментах. [10] Початкове припущення про шкідливі властивості β-амінокислот з точки зору вторинної структури [10] виявилося невірним. [11] D-амінокислотиДеякі амінокислоти містять протилежну абсолютну хіральність, хімічні речовини, які недоступні із звичайних механізмів трансляції та транскрипції. Стінки більшості бактеріальних клітин утворені пептидогліканом, полімером, що складається з аміноцукрів, зшитих короткими олігопептидами, сполученими між собою. Олігопептид не синтезується рибосомами і містить кілька особливостей, включаючи D-амінокислоти, як правило, D -аланін і D -глутамат. Ще одна особливість полягає в тому, що D -аланін рацемізується ферментами, що зв’язують PLP (кодуються alr або гомологом dadX ), тоді як D -глутамат рацемізується незалежним від кофактора ферментом (murI ). Наприклад, D -лізин присутній у Thermotoga spp., а в деяких стійких до ванкоміцину бактеріях присутній D -серин (ген vanT ). [12] [13] Без водню на α-вуглеціУсі протеїногенні амінокислоти мають принаймні один атом водню на α-вуглеці. Гліцин має два атоми водню, а всі інші мають один атом водню та один бічний ланцюг. Заміна водню, що залишився, більшим замісником, таким як метильна група, спотворює білкову основу. [10] У деяких грибах α-аміноізомасляна кислота виробляється як попередник пептидів, деякі з яких виявляють антибіотичні властивості. [14] Ця сполука подібна до аланіну, але має додаткову метильну групу на α-вуглеці замість водню. Тому він є ахіральним. Іншою сполукою, подібною до аланіну без α-водню, є дегідроаланін, який має метиленовий бічний ланцюг. Це одна з кількох природних дегідроамінокислот .
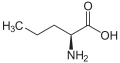
Подвійні стереоцентри амінокислотПідгрупа L -α-амінокислот неоднозначна щодо того, який із двох кінців є α-вуглецем. У білках залишок цистеїну може утворювати дисульфідний зв’язок з іншим залишком цистеїну, таким чином зшиваючи білок. Два зшиті цистеїни утворюють молекулу цистину . Цистеїн і метіонін зазвичай утворюються шляхом прямого сульфурилювання, але в деяких видів вони можуть бути отримані шляхом транссульфурування, коли активований гомосерин або серин зливається з цистеїном або гомоцистеїном, утворюючи цистатіонін . Подібною сполукою є лантіонін, який можна розглядати як дві молекули аланіну, з’єднані тіоефірним зв’язком, який зустрічається в різних організмах. Подібним чином дженколієва кислота, рослинний токсин із бобів Дженгколь, складається з двох цистеїнів, з’єднаних метиленовою групою. Діамінопімелінова кислота використовується як місток у пептидоглікані та використовується як попередник лізину (через його декарбоксилювання). Пребіотичні амінокислоти та альтернативна біохіміяУ метеоритах і в пребіотичних експериментах (наприклад, в експерименті Міллера-Юрі ) виявлено набагато більше амінокислот, ніж двадцять стандартних амінокислот, деякі з яких містяться у вищих концентраціях, ніж стандартні. Було припущення, що якби амінокислотне життя виникло десь у Всесвіті, то не більше 75% амінокислот були б спільними. [10] Найбільш помітною аномалією є відсутність аміномасляної кислоти.
Прямий бічний ланцюгГенетичний код був описаний як заморожена випадковість, і причиною, чому існує лише одна стандартна амінокислота з прямим ланцюгом, аланін, може бути просто надлишок валіну, лейцину та ізолейцину. [10] Однак, вважається, що амінокислоти з прямим ланцюгом утворюють набагато більш стабільні альфа-спіралі. [15]
ХалькогенСерин, гомосерин, O-метилгомосерин і O-етилгомосерин мають гідроксиметильний, гідроксиетиловий, O-метилгідроксиметильний і O-метилгідроксиетильний бічний ланцюг; тоді як цистеїн, гомоцистеїн, метіонін і етіонін мають тіолові еквіваленти. Еквівалентами селенолу є селеноцистеїн, селеногомоцистеїн, селенометіонін і селеноетіонін. Амінокислоти з наступним зниженням халькогену також зустрічаються в природі: кілька видів, таких як Aspergillus fumigatus, Aspergillus terreus і Penicillium chrysogenum, за відсутності сірки здатні продукувати та включати в білок телуроцистеїн і телурометіонін. [16] РольУ клітинах, особливо автотрофних, кілька непротеїногенних амінокислот зустрічаються як метаболічні проміжні продукти. Однак, незважаючи на каталітичну гнучкість PLP-зв'язуючих ферментів, багато амінокислот синтезуються як кетокислоти (наприклад, 4-метил-2-оксопентаноат до лейцину) і амінуються на останньому етапі, таким чином зберігаючи рівень непротеїногенних амінокислот у ролі проміжних продуктів досить низьким. Орнітин і цитрулін беруть участь у циклі сечовини, що є частиною катаболізму амінокислот. [17] На додаток до первинного метаболізму, кілька непротеїногенних амінокислот є попередниками або кінцевим продуктом у вторинному метаболізмі для створення невеликих сполук або нерибосомних пептидів (таких як деякі токсини). Посттрансляційне включення у білокНезважаючи на те, що вони не кодуються генетичним кодом як протеїногенні амінокислоти, деякі нестандартні амінокислоти все ж містяться в білках. Вони утворюються шляхом посттрансляційної модифікації бічних ланцюгів стандартних амінокислот, присутніх у цільовому білку. Ці модифікації часто необхідні для функціонування або регуляції білка; наприклад, в γ-карбоксиглутаматі карбоксилювання глутамату забезпечує краще зв'язування катіонів кальцію [18], а в гідроксипроліні гідроксилювання проліну є критичним для підтримки сполучних тканин . [19] Іншим прикладом є утворення гіпузину у факторі ініціації трансляції EIF5A шляхом модифікації залишку лізину. [20] Такі модифікації також можуть визначати локалізацію білка, наприклад, додавання довгих гідрофобних груп може призвести до зв’язування білка з фосфоліпідною мембраною. [21]
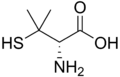
Існують деякі попередні докази того, що аміномалонова кислота може бути присутня в білку, можливо, через неправильне включення. [22] [23] Токсичні аналогиКілька непротеїногенних амінокислот є токсичними через їх здатність імітувати певні властивості протеїногенних амінокислот, таких як тіалізин . Деякі непротеїногенні амінокислоти є нейротоксичними, імітуючи амінокислоти, які використовуються як нейротрансмітери (тобто не для біосинтезу білка), включаючи квісквалінову кислоту, канаванін і азетидин-2-карбонову кислоту. [24] Цефалоспорин С має основу α-аміноадипінової кислоти (гомоглутамат), яка амідована цефалоспориновим фрагментом. [25] Пеніциламін є терапевтичною амінокислотою, механізм дії якої невідомий.
Ціанотоксини, що зустрічаються в природі, також можуть включати непротеїногенні амінокислоти. Мікроцистин і нодулярін, наприклад, походять від ADDA, β-амінокислоти. Не амінокислотиТаурин є аміносульфоновою кислотою, а не амінокарбоновою кислотою, однак іноді її вважають такою, оскільки кількості, необхідні для пригнічення ауксотрофу в певних організмах (таких як коти), ближчі до кількості «незамінних амінокислот» (ауксотрофія амінокислот), ніж у вітамінів (кофакторна ауксотрофія). Осмоліти, саркозин і гліцинбетаїн є похідними амінокислот, але мають вторинний і четвертинний амін відповідно.
Список літератури
|