|
Glukoneogenéza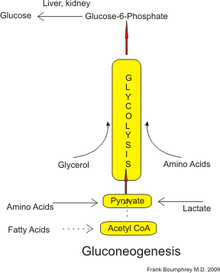 Glukoneogenéza (GNG) je metabolická dráha, ktorá vedie k vytvoreniu glukózy z niektorých nesacharidových uhlíkových substrátov. Tento proces prebieha vo všetkých živých organizmoch - v rastlinách, živočíchoch, hubách, baktériach i iných mikroorganizmoch.[1] U stavovcov prebieha glukoneogenéza hlavne v pečeni a v menšej miere v kôre obličiek. Je to jeden z dvoch hlavných procesov - druhým je rozklad glykogénu (glykogenolýza) - ktorými ľudia a mnohé zvieratá udržiavajú stabilnú hladinu glukózy v krvi, aby predišli jej zníženiu (hypoglykémii).[2] U prežúvavcov, u ktorých sú sacharidy z potravy zvyčajne metabolizované mikroorganizmami v bachore, prebieha glukoneogenéza stále bez ohľadu na postenie, nízky príjem sacharidov, pohyb a podobne.[3] U mnohých iných zvierat prebiaha často práve počas pôstu, hladovania, nízkeho príjmu sacharidov alebo intenzívneho pohybu či cvičenia. U ľudí môže substrát pre glukoneogenézu pochádzať z akýchkoľvek nesacharidových zdrojov, ktoré je možné premeniť na pyruvát alebo na niektorý z medziproduktov glykolýzy (pozri nižšie). Pri rozklade proteínov je možné využiť glukogénne aminokyseliny (ale nie ketogénne aminokyseliny). Pri rozklade lipidov (napríklad triacylglycerolov) je možné využiť glycerol a mastné kyseliny s nepárnym počtom uhlíkov (ale nie mastné kyseliny s párnym počtom uhlíkov, pozri nižšie). Pri iných metabolizmoch je možné využiť napríklad laktát z Coriho cyklu. Pri dlhšom postení je možné využiť i acetón vznikajúci z ketolátok, čím je možné docieliť premenu látok z mastných kyselín na glukózu.[4] Aj keď glukoneogenéza zvyčajne prebieha v pečeni, relatívny príspevok obličiek ku glukoneogenéze sa zvyšuje pri diabete alebo dlhšom hladovaní.[5] Glukoneogenéza je silne endergonická, ale spojením s hydrolýzou ATP alebo GTP sa z nej prakticky stane exergonický proces. Napríklad dráha vedúca od pyruvátu ku glukóza-6-fosfátu vyžaduje 4 molekuly ATP a 2 molekuly GTP, aby prebehla spontánne. Tieto ATP sú získavané z metabolizmu mastných kyselín pomocou beta oxidácie.[6] PrekurzoryU ľudí sú hlavnými prekurzormi glukoneogenézy laktát, glycerol (ktorý je súčasťou triacylglycerolov), alanín a glutamín. Celkovo zahŕňajú až 90 % zdrojov glukoneogenézy.[7] Ostatné glukogénne aminokyseliny a všetky intermediáty citrátového cyklu (pomocou premeny na oxalacetát) je možné takisto využiť ako substráty pre glukoneogenézu.[8] Všeobecne však konzumácia glukoneogénnych substrátov v potrave nevedie k zvýšenej glukoneogenéze.[9]  U prežúvavcov je hlavným substrátom pre glukoneogenézu propionát.[3][11] U ostatných organizmov vzniká propionát v beta oxidácii mastných kyselín s nepárnym počtom uhlíkov a u vetvených aminokyselín a je len subtrátom len v relatívne malom množstve.[12][13] Laktát je transportovaný naspäť do pečene v Coriho cykle, kde je premenený na pyruvát pomocou laktátdehydrogenázy. Pyruvát, prvý substrát predurčený na glukoneogenézu, potom môže byť využitý na syntézu glukózy.[8] Transaminácia alebo deaminácia aminokyselín umožňuje vstup ich uhlíkovej kostry do cyklu priamo (ako pyruvát alebo oxalacetát) alebo nepriamo (cez citrátový cyklus). Príspevok laktátu z Coriho cyklu na celkovú produkciu glukózy sa zvyšuje s dĺžkou hladovania.[14] Konkrétne, po 12, 20 a 40 hodinách hladovania u ľudských dobrovoľníkov bol príspevok laktátu z Coriho cyklu ku glukoneogenéze 41 %, 71 % a 92 %.[14] V biochémii bola dlho nezodpovedná otázka, či môžu byť na glukózy u zvierat konvertované aj mastné kyseliny s párnym počtom uhlíkom.[15] Mastné kyseliny s nepárnym počtom uhlíkov je možno oxidovať na acetylkoenzým A a propionylkoenzým A, pričom propionylkoenzým A potom môže fungovať ako prekurzor sukcinylkoenzýmu A, ktorý sa následne môže premeniť na pyruvát a vstúpiť do glukoneogenézy. Naproti tomu mastné kyseliny s párnym počtom uhlíkov sú oxidované len na acetylkoenzým A. Ten môže vstúpiť do glukoneogenézy len pomocou glyoxylátového cyklu, pri ktorom sa z neho tvoria štvoruhlíkové dikarboxylové kyseliny ako prekurzory.[8] Glyoxylátový cyklus zahŕňa dva enzýmy, malátsyntázu a izocitrátlyázu, ktoré sú prítomné v hubách, rastlinách a baktériách. Napriek niekoľkým správam o detekcii enzýmovej aktivity týchto enzýmov u zvierat boli však gény kódujúce oba tieto enzýmy nájdené len u hlístovcov, u ktorých existujú ako jeden bifunkčný enzým.[16][17] Gény kódujúce len malátsyntázu (ale nie izocitrátlyázu) boli identifikované i u iných živočíchov, napríklad článkonožcov, ostnatokožcov a dokonac i u niektorých stavovcov. Cicavce, u ktorých bola objavená malátsyntáza, zahŕňajú kloakovce (vtákopysk) a vačkovce (vačica), ale nie u placentovcov.[17] Existencia glyoxylátového cyklu u ľudí nebola potvrdená a je teda všeobecne predpokladné, že u ľudí nemôžu byť mastné kyseliny premenené na glukózu priamo. Bolo ukázané, že uhlík-14 sa objaví v glukóze, ak je dodaný v podobe mastných kyselín,[18] ale toto sa dá predpokladať na základe zabudovávania značených atómov odvodených z acetylkoenzýmu A do intermediátov citrátového cyklu, ktoré sú zameniteľné s tými odvodenými z iných fyziologických zdrojov, ako sú glukogénne aminokyseliny.[15] Bez prítomnosti ostatných glukogénnych zdrojov nemôže dvojuhlíkový acetylkoenzým A odvodený z oxidácie mastných kyselín viesť k celkovému zisku glukózy cez citrátový cyklus, pretože v citrátovom cykle sú dva atómy uhlíku uvoľnené v podobe oxidu uhličitého. Počas ketózy sa však acetylkoenzým A z mastných kyselín využíva na tvorbu ketolátok, vrátane acetónu, a až ~60 % acetónu môže byť oxidovaných v pečeni na pyruvátové prekurzory acetol (hydroxyacetón) a metylglyoxal.[19][4] Ketolátky vytvorené z mastných kyselín by teda mohli tvoriť až 11 % glukoneogenézy počas hladovania. Katabolizmus mastných kyselín produkuje aj energiu v podove ATP, ktorá je nutná pre glukoneogenézu. UmiestnenieU cicavcov sa predpokladalo, že glukoneogenéza prebieha len v pečeni,[20] obličkách,[20] črevách[21] a svaloch,[chýba zdroj] ale nové poznatky poukazujú na to, že glukoneogenéza prebieha i v astrocytoch v mozgu.[22] Tieto orgány využívajú mierne odlišné prekurzory glukoneogenézy. Pečen využíva predovšetkým lakát, glycerol a glukogénne aminokyseliny (hlavne alanín), zatiaľ čo obličky využívajú laktát, glutamín a glycerol.[23][7] Lakát z Coriho cyklu je kvantitatívne najväčším zdrojom substrátu pre glukoneogenézu, a to hlavne v obličkách.[7] Pečeň využíva glykogenolýzu i glukoneogenézu na tvorbu glukózy, zatiaľ čo obličky využívajú len glukoneogenézu.[7] Po jedle sa pečeň sústredí skôr na syntézu glykogénu a u obličiek sa zvýši glukoneogenéza.[9] Črevá využívajú hlavne glutamín a glycerol.[21] Propionát je hlavným zdrojom glukoneogenézy v pečeni prežúvavcov a ich pečeň môže zároveň využívať glukogénne aminokyseliny (napríklad alanín) vo väčšom množstve, keď sa zvýši dopyt po glukóze.[24] Kapacita buniek pečene využiť laktát na glukoneogenézu sa znižuje počas životného vývoja prežúvavcov u teliat a jahniat.[25] V tkanive ovčích obličiek bol pozorovaný vysoký obrat glukoneogenézy z propionátu.[26] Vo všetkých druhoch je tvorba oxalacetátu z pyruvátu a intermediátov citrátového cyklu obmedzená len na mitochondrie. a enzýmy konvertujúce fosfoenolpyruvát (PEP) na glukóza-6-fosfát sú prítomné v cytozole.[27] Umiestnenie enzýmu, ktorý spája tieto dve často glukoneogenézy premenou oxalacetátu na PEP - PEP karboxykináza (PEPCK) - sa medzidruhovo mení: enzým sa môže nachádzať výlučne v mitochondiách, výlučne v cytozole, alebo byť rozložený rovnomerne v oboch, ako je to u ľudí.[27] Transport PEP cez mitochondriálnu membránu sa dosahuje pomocou určených transportných proteínov, ale žiadne také enzýmy neexistujú pre oxalacetát.[27] To znamená, že u druhov, ktoré nemajú PEPCK prítomnú v mitochondriách, je nutné premeniť oxalacetát na malát alebo aspartát, presunúť ho mimo mitochondrie a potom premeniť znovu naspäť na oxalacetát, aby mohla glukoneogenéza pokračovať.[27] Metabolická dráha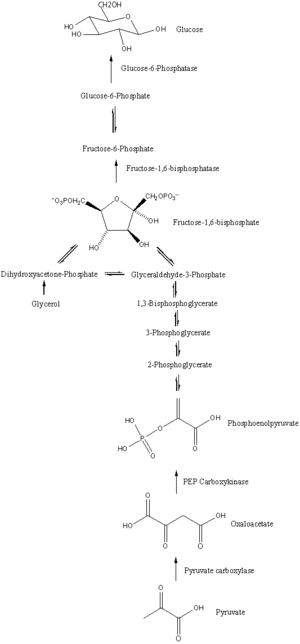 Glukoneogenéza je dráha pozostávajúca zo série 11 reakcií katalyzovaných enzýmami. Dráha začína v pečeni alebo obličke, presnejšie v mitochondrii alebo cytoplazme týchto buniek, čo záleží na použitom substráte. Mnoho reakcií je spätnými reakciami glykolýzy.
ReguláciaZatiaľ čo väčšina krokov glukoneogenézy sú spätné reakcie glykolýzy, tri regulované a silne endergonické kroky sú nahradené reakciami, ktoré sú kineticky výhodnejšie. Enzýmy hexokináza/glukokináza, fosfofruktokináza a pyruvátkináza, vystupujúce v glykolýze, sú nahradené enzýmami glukóza-6-fosfátázou, fruktóza-1,6-bisfosfatázou a PEP karboxykinázou/pyruvátkarboxylázou. Tieto enzýmy sú typicky regulované podobnými molekulami, ale s opačnými výsledkami. Ako príklad, acetylkoenzým A a citrát aktivujú enzýmy glukoneogenézy (konkrétne, pyruvátkarboxylázu a fruktóza-1,6-bisfosfatázu) a zároveň inhibujú glykolytický enzým pyruvátkinázu. Tento systém vzájomneho riadenia glykolýzy a glukoneogenézy inhibujúcich sa navzájom zabraňuje zbytočným cyklom syntézy a rozkladu glukózy. Pyruvátkinázu je možné obísť celkom 86 inými dráhami[28] nesúvisiacimi s glukoneogenézou za účelom syntézy pyruvátu a následne laktátu - niektoré z nich využívajú uhlíkové atómy pochádzajúce z glukózy. Väčšina enzámov zodpovedných za glukoneogenézu sa nachádza v cytozole. Výnimkou je pyruvátkarboxyláza, prítomná v mitochondrii, a u zvierat PEP karboxykináza (PEPCK). PEPCK existuje ako izoenzým prítomný v mitochondrii aj cytozole.[29] Rýchlosť flukoneogenézy je udávaná pôsobením kľúčového enzýmu, fruktóza-1,6-bisfosfatázy, ktorá je zároveň regulovaná pomocou prenosu signálu vďaka cAMP a jej fosforylácii. Globálna regulácia glukoneogenézy je sprostredkovaná glukagónom (ktorý sa vylučuje pri nízkej hladine glukózy v krvi). Ten spôsobuje fosforyláciu enzýmov a regulačných proteínov proteínkinázou A (kináza regulovaná cyklickým AMP), čo vedie k inhibícii glykolýzy a stimulácii glukoneogenézy. Inzulín pôsobí proti glukagónu inhibíciou glukoneogenézy. Diabetes druhého typu je spôsobený nadbytkom glukagónu a odolnosťou tela voči inzulínu.[30] Inzulín nie je schopný inhibovať génovú expresiu enzýmov, ako napríklad PEPCK, čo vedie k zvýšenej hladine glukózy v krvi (hyperglykémii).[31] Antidiabetikum metformín znižuje hladinu glukózy primárne pomocou inhibície glukoneogenézy, čím prekonáva neschopnosť inzulínu inhibovať glukoneogenézu kvôli vzniknutej rezistencii na inzulín.[32] Štúdie preukázali, že absencia heptálnej produkcie glukózy nemá významný efekt na riadenie koncentrácie glukózy v plazme počas hladovania. Kompenzačná indukcia glukoneogenézy prebieha v obličkách a črevách a je poháňaná glukagónom, glukokortikoidmi a acidózou.[33] Inzulínová rezistenciaFOX proteín FoxO6 v pečeni bežne podporuje glukoneogenézu počas hladovania, ale inzulín blokuje FoxO6 po jedle.[34] V prípade inzulínovej rezistencie inzulín neblokuje FoxO6, čo má za následok glukoneogenézu i po jedlo, zapríčiňujúc hyperglykémiu (vysokú hladinu cukru v krvi).[34] Inzulínová rezistencia je bežný prejav metabolického syndrómu a diabetu druhého typu. Z tohto dôvodu je glukoneogenéza cieľom terapie diabetu druhého typu, napríklad antidiabetikom metformínom, ktorý inhibuje glukoneogenickú tvorbu glukózy a stimuluje príjem glukózy bunkami.[35] Referencie
Pozri ajZdrojTento článok je čiastočný alebo úplný preklad článku Gluconeogenesis na anglickej Wikipédii. |
Portal di Ensiklopedia Dunia
