|
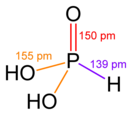
Фосфористая кислота
Фо́сфористая кислота́ (фосфо́новая кислота́, о́ртофо́сфористая кислота́; H3PO3, H2(HPO3)) — в водных растворах двухосновная кислота средней силы. Фосфористая кислота сильно раздражает кожу и слизистые оболочки. Вещество относится ко второму классу опасности. СвойстваБезводная фосфористая кислота — бесцветные гигроскопичные кристаллы. Несмотря на то, что кислота содержит три атома водорода — она двухосновная. Фосфористая кислота является кислотой средней силы и диссоциирует по двум ступеням: Константы диссоциации фосфористой кислоты при 18 °C: K1 = 5,1⋅10−2 K2 = 1,8⋅10−7. При нагревании до 250 °C безводная фосфористая кислота разлагается на фосфорную кислоту и фосфин, а водные её растворы — на фосфорную кислоту и водород. Фосфористая кислота легко окисляется галогенами, оксидами азота и пр. до фосфорной кислоты, кислородом окисляется до фосфорноватой кислоты: Соли фосфористой кислоты называются фосфитами или (по рекомендации ИЮПАК) фосфонатами. Большинство фосфитов малорастворимы в воде. Известны одно- и двузамещённые фосфиты. Фосфористая кислота и её соли являются сильными восстановителями. Однако активные металлы в кислом растворе восстанавливают H3РО3 до РH3. История изученияПроблема выяснения структурной формулы фосфористой кислоты и доказательства её двухосновного характера долгое время вызывала серьёзные споры в профессиональной среде вплоть до конца XIX века. В частности, в 1866 г. русский химик Н. А. Меншуткин в своей диссертации «О водороде фосфористой кислоты, не способном к металлическому замещению при обыкновенных условиях для кислот» пришёл к неверному выводу о трёхгидроксильной структуре кислоты и отстаивал свою точку зрения.[2] Противоречия были окончательно разрешены только к 1905 году, когда А. Е. Арбузов защитил при Казанском университете магистерскую диссертацию «О строении фосфористой кислоты и её производных». В этой работе диссертант впервые получил в чистом виде эфиры фосфористой кислоты, открыл явление их каталитической изомеризации в эфиры алкилфосфиновых кислот и нашел специальную реакцию для соединений трёхвалентного фосфора ― образование комплексных соединений с галоидными солями закиси меди. Исследование А. Е. Арбузова было удостоено Русским физико-химическим обществом премии им. Зинина и Воскресенского.[2] Кроме выяснения структуры фосфористой кислоты, диссертация А. Е. Арбузова фактически открыла путь для искусственного синтеза принципиально новой ветви органических соединений. Применённая в качественном анализе фосфористой кислоты так называемая реакция Арбузова не только дала ключ к пониманию структуры органических соединений фосфора, но и подтвердила незыблемость положений теории органических связей А. М. Бутлерова. Решение теоретической проблемы строения неорганической кислоты, в конечном счёте дало принципиальный ключ к пониманию структуры и дальнейшему лабораторному и промышленному синтезу соединений фосфора. В XX веке реакция Арбузова оказалась положена в основание широчайшей ветви мирового синтеза ФОС ― фосфорорганических соединений.[3] Эфиры фосфористой кислотыПри взаимодействии спиртов с чистым PCl3 получаются моно-, ди- и триэфиры фосфористой кислоты с общей формулой P(OR)3, легко образующие комплексы с переходными металлами и другими акцепторами. Они также легко окисляются до соответствующих фосфатов: При взаимодействии эфиров с алкилгалогенидами образуются алкилфосфонаты: ПолучениеПолучают фосфористую кислоту растворением P4O6 (P2O3) в холодной воде, гидролизом PCl3 или взаимодействием фосфитов с серной или соляной кислотами: ПрименениеФосфористую кислоту и её соли применяют как восстановители, а также широчайшим образом — в синтезе фосфорорганических соединений, путь для которого открыло исследование 1904-1905 года, получившее впоследствии название «реакции Арбузова». Говоря химическим языком, эта реакция заключается в алкилировании триалкилфосфитов алкилгалогенидами с образованием диалкилфосфонатов, — иными словами, в превращении средних эфиров фосфористой кислоты в эфиры алкилфосфиновых кислот под действием галоидных алкилов.[3] БезопасностьОртофосфористая кислота сильно раздражает кожу и слизистые оболочки. ПДК в воздухе - 0,4 мг/м³. Вещество относится ко второму классу опасности по ГОСТ 12.1.007-76. Примечания
Источники
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||