|
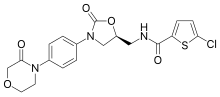
Ривароксабан
Рива́роксабан (кодовое название BAY 59-7939) — пероральный антикоагулянт из группы прямых ингибиторов фактора Xa. В частности, он используется для лечения тромбоза глубоких вен и легочной эмболии, а также для предотвращения образования тромбов при фибрилляции предсердий и после операций на бедре или колене.[4] Общие побочные эффекты включают кровотечение[4]. К другим побочным эффектам относят гематому позвоночника и анафилаксию[4]. Неясно, безопасно ли использование ривароксабана во время беременности и кормления грудью.[5] По сравнению с варфарином, он меньше взаимодействует с другими лекарствами.и не требует постоянного контроля МНО[6] Он работает, блокируя активность фактора свертывания крови Ха.[4] Разработан и выпускается немецкой фармацевтической компанией Bayer под торговым названием «Ксарелто». Применение в медицинеУ пациентов с неклапанной фибрилляцией предсердий препарат столь же эффективен, как варфарин в предотвращении негеморрагических инсультов и тромбоэмболии.[7] Применение Ривароксабана связано с более низким риском сильных и смертельных кровотечений, чем варфарин. Хотя ривароксабан и связан с более высокой частотой кровотечений в желудочно-кишечном тракте.[8] В июле 2012 года британский Национальный институт здравоохранения и медицины рекомендовал ривароксабан для профилактики и лечения венозной тромбоэмболии.[9] Мерцательная аритмияРазница в эффектах ПАНАВК (Пероральные антикоагулянты, не являющиеся антагонистами витамина К) и варфарина у людей с мерцательной аритмией, которым выполнили стентирование сосудов сердца, может быть незначительной или вообще отсутствовать. Тем не менее, ПАНАВК, вероятно, уменьшают потребность в госпитализации по сравнению с варфарином. ПАНАВК могут быть безопаснее варфарина. Один из препаратов ПАНАВК (дабигатран) может снизить частоту как больших, так и малых кровотечений. Другие препараты ПАНАВК (апиксабан и ривароксабан), вероятно, снижают частоту небольших кровотечений. Существенной разницы между препаратами ПАНАВК в каких‐либо первичных или вторичных исходах не было. Определённость доказательств варьировала от очень низкой до средней, что указывает на необходимость дополнительных исследований по этому вопросу.[10][11] Артроскопия коленного суставаСуществует небольшой риск того, что у здоровых взрослых пациентов, перенесших артроскопию коленного сустава, разовьется венозная тромбоэмболия (ТЭЛА или ТГВ). Имеются доказательства от умеренной до низкой достоверности об отсутствии пользы от использования низкомолекулярного гепарина (НМГ), аспирина или ривароксабана для снижения этого небольшого риска ТЭЛА или симптоматического ТГВ. Имеются очень низкие доказательства того, что использование НМГ может снизить риск бессимптомного ТГВ по сравнению с отсутствием лечения, но неясно, как это напрямую связано с частотой ТГВ или ТЭЛА у здоровых пациентов. Не было обнаружено никаких доказательств различий в побочных эффектах (включая большое и незначительное кровотечение), но данные, относящиеся к этому, были ограничены из-за небольшого количества событий в исследованиях, сообщающих в рамках сравнений.[12][13] ПротивопоказанияВ рекомендациях по дозировке не рекомендуется назначать ривароксабан с лекарствами, которые, как известно, являются сильными комбинированными ингибиторами CYP3A4 / P-гликопротеина, поскольку это приводит к значительно более высоким концентрациям ривароксабана в плазме.[14][15] Из-за трудностей, связанных с контролем кровотечения, прием ривароксабана следует прекратить, по крайней мере за 24 часа до операции, а затем снова начать, как только будет установлен адекватный гемостаз.[16] Побочные эффектыНаиболее серьёзный побочный эффект — это кровотечения, включая тяжёлые внутренние кровотечения.[17][18][19] Применение Ривароксабана связано с более низким риском сильных и смертельных кровотечений, чем варфарин, но связан с более высокой частотой кровотечений в ЖКТ. В октябре 2014 года, компания Портола Фармасьютикалз завершила фазы I и II клинических испытаний для andexanet Альфа в качестве антидота для ингибиторов фактора Ха с несколькими побочными эффектами, и начала исследования III фазы.[20][21] Andexanet Альфа, как ожидалось, будет утверждён в 2016 году.[22] Однако, в 2017 году соединение ещё не было одобрено FDA. В 2015 году пост-маркетинговые исследования выявили токсичность для печени, и показали необходимость дальнейших исследований для количественной оценки риска.[23][24] Препарат противопоказан людям с серьёзными заболеваниями печени и терминальной стадии почечной болезни, при которых исследований не проводилось. Ривароксабан в индивидуальной упаковке имеет предупреждение о том, что людям, использующим препарат, не следует прекращать его применения до консультации с врачом, так как это может увеличить риск инсульта.[25] В 2015 году на ривароксабан приходится наибольшее количество зарегистрированных случаев серьёзных осложнений среди регулярно контролируемых FDA лекарств.[26] АнтидотСпецифическим антидотом ривороксабана является препарат Андекса (рекомбинантный инактивированный фактор Xa). Механизм действияРивароксабан подавляет свободный фактор Ха и фактор Ха связанный в комплекс протромбиназы.[27] Это высокоселективный прямой ингибитор фактора Ха с пероральной биодоступностью и быстрым началом действия. Ингибирование фактора Ха прерывает внутренние и внешние пути свёртывания крови, препятствует образованию тромбина и развитию тромбов. Ривароксабан не подавляет тромбин (активированный фактор II) и не оказывает никакого влияния на тромбоциты.[28] Это позволяет легко корректировать дозы в антикоагулянтной терапии и отслеживать коагуляцию[28] , а также избегать ограничений в питании.[22] Нефракционированный гепарин, низкомолекулярный гепарин и фондапаринукс также ингибируют активность фактора Ха, но косвенно, путём связывания циркулирующего антитромбина (АТ III). Принимая во внимание, что орально активный варфарин и аценокумарол являются антагонистами витамина К, уменьшая количество факторов свёртывания крови, включая фактор X.[29] Ривароксабан имеет предсказуемую фармакокинетику у широкого спектра пациентов (возраст, пол, вес, раса) и имеет линейную кривую доза-эффект в восьмикратном диапазоне доз (5-40 мг).[30] ФармакодинамикаФактор свёртывания крови X (фактор Стюарта—Прауэра) играет центральную роль в каскаде коагуляции, так как активируется и внешней, и внутренней теназой. Переходя в активную форму фактор X вместе с неферментным кофактором Va и Ca2+ образует на поверхности тромбоцитов или эндотелия протромбиназный комплекс, который в свою очередь катализирует процесс превращения протромбина в тромбин. Тромбин активирует полимеризацию растворимого фибриногена, приводя к формированию фибринового сгустка (тромба). Механизм действия ривароксабан заключается в высокоселективном прямом ингибировании фактора свёртывания крови Ха, что позволяет одновременно заблокировать как внешний, так и внутренний пути коагуляции, и приостановить процесс тромбообразования. Химия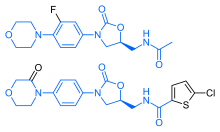 Ривароксабан имеет поразительное структурное сходство с антибиотиками группы линезолида: оба препарата имеют те же оксазолидинон-производные основные структуры. Соответственно, ривароксабан изучался на возможную противомикробную активность и митохондриальную токсичность, которая является известным осложнением долгосрочного применения линезолида. Исследования показали, что ни ривароксабан, ни его метаболиты не обладают антибактериальным действием против грам-положительных бактерий. Что касается митохондриальной токсичности, то в исследованиях In vitro, опубликованных до 2008 года выявленный риск был низким.[31] Общество и культураЭкономикаИспользование ривароксабана в 70 раз чаще варфарина, по данным Express Scripts Holding Co, крупнейшей в США компанией по работе с аптеками.[22] В 2016 году, Байер утверждал, что препарат был лицензирован в 130 странах и более 23 миллионов пациентов прошли лечение.[32] ОдобрениеВ сентябре 2008 года, Министерство здравоохранения Канады выдало регистрационное удостоверение на ривароксабан для профилактики венозной тромбоэмболии у людей, которые прошли замену тазобедренного сустава или полное эндопротезирование коленного сустава.[33] В том же месяце Европейская комиссия также выдала регистрационное удостоверение ривароксабана для профилактики венозной тромбоэмболии у взрослых пациентов, перенёсших плановые операции бедра и коленного сустава.[34] На 1 июля 2011 года Управление по санитарному надзору за качеством пищевых продуктов и медикаментов в США (FDA) одобрило ривароксабан для профилактики тромбоза глубоких вен (ТГВ), который может привести к тромбоэмболии лёгочной артерии (ТЭЛА), у взрослых, перенёсших эндопротезирование тазобедренного и коленного сустава.[35] 4 ноября 2011 года FDA США одобрило ривароксабан для профилактики инсульта у пациентов с неклапанной фибрилляцией предсердий.[36] ИсследованияИсследователи из Школы медицины Университета Дьюка были обвинены в сокрытии клинических данных, используемых для оценки ривароксабана.[37] Они проводили клинические испытания ривароксабана ROCKET AF.[38] В клиническом исследовании, опубликованном в 2011 году в медицинском журнале в Новой Англии[39], которое возглавил Роберт Калиффи, (представитель FDA[40])[39], нашли, что ривароксабан более эффективен, чем варфарин в снижении вероятности ишемических инсультов у пациентов с фибрилляцией предсердий.[39] Валидность исследования была поставлена под вопрос в 2014 году, когда фармацевтическими компаниями Байер и Джонсон и Джонсон было установлено, что использованные приборы мониторинга крови INRatio не функционируют должным образом.[37][38] Последующий анализ исследований Школы медицины Университета Дьюка, опубликованных в феврале 2016 года, обнаружил, что это не оказало существенного влияния на эффективность и безопасность испытаний.[41] Примечания
Ссылки
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||