|
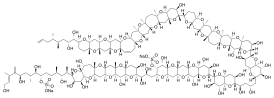
Майтотоксин
Майтотоксин — токсин небелковой природы, продуцируемый динофлагеллятами вида Gambierdiscus toxicus. Является одним из самых токсичных веществ, обнаруженных в живой природе, и, одновременно, одним из самых сложных по структуре веществ природного происхождения. Майтотоксин чрезвычайно токсичен (доза в 130 нг/кг массы тела, при внутрибрюшинном введении, летальна для мышей)[1] и обладает, вероятно, самым сложным строением из всех известных небелковых веществ природного происхождения (правильность установления структуры и пространственного строения молекулы майтотоксина и в настоящее время вызывает сомнения, а попытки осуществить его полный синтез, начатые ещё в середине 1990-х годов, до сих пор не увенчались успехом). История открытия и изученияИзначально майтотоксин был выделен из рыб вида Ctenochaetus striatus (полосатый хирург), обитающих в экосистемах коралловых рифов и питающихся планктоном (биоаккумуляция токсина в организме некоторых видов хищных рыб (барракуды, морской окунь, мурены, сибас и др.), питающихся полосатым хирургом, приводит к отравлению людей, употребляющих рыбу этих видов в пищу). На Таити этот вид рыб известен как «maito», что и дало название этому токсину[2][3]. Структура и пространственное строение молекулы майтотоксина были установлены к середине 1990-х годов с использованием методов аналитической химии (масс-спектрометрия и двумерная спектроскопия ЯМР с предварительной частичной окислительной деградацией молекулы данного токсина). Но сомнения относительно правильности установления пространственного строения майтотоксина остаются до сих пор[4]. Необычность и сложность структуры (в том числе наличие в молекулах множества хиральных центров) таких соединений как майтотоксин, палитоксин и др. делают установление их строения само по себе очень сложной задачей и требуют привлечения усилий как наиболее компетентных учёных, так и использования самых передовых методов химического и физико-химического анализа (в том числе таких, которые ранее просто не существовали)[4]. Особую сложность представляет установление стереохимии (пространственного строения) подобных соединений. Даже само по себе получение достаточных количеств таких веществ является непростой задачей. Единственный доступный источник получения — выделение из живых организмов, которые осуществляют биосинтез либо биоаккумулируют их в себе (причём, как правило, содержание их очень невелико). К примеру, для получения в чистом виде майтотоксина пришлось на протяжении года культивировать динофлагеллят вида Gambierdiscus toxicus для получения около 4000 литров культуры (с концентрацией клеток 2⋅106/л), а затем применить многостадийный процесс выделения, концентрирования и очистки этого соединения. В итоге удалось получить порядка 5 мг химически чистого майтотоксина[4]. Работы над осуществлением полного синтеза майтотоксина были начаты в 1996 году и продолжаются (с перерывами) по настоящее время под руководством Кирьякоса Николау. Возглавляемые им группы учёных пока что смогли осуществить синтез некоторых отдельных частей, из которых состоит молекула майтотоксина[5][6][7][8][2]. Молекула майтотоксина состоит из 32 конденсированных колец, содержит 28 гидроксильных и 22 метильные группы, а также 2 эфира серной кислоты. Кроме того, в ней есть 98 хиральных центров. Всё это делает задачу по выполнению полного химического синтеза майтотоксина исключительно сложной. ТоксичностьLD50 — 50 нг/кг массы тела (для мышей), что делает майтотоксин наиболее токсичным из всех известных веществ небелковой природы. Физиологическое действие майтотоксина состоит в нарушении гомеостаза внутриклеточного содержания Ca2+. Резкое повышение содержания ионов Са2+ внутри клеток, в конечном счёте, приводит к их гибели. Точный молекулярный механизм действия майтотоксина неизвестен, но предполагается, что он связывается с Ca-АТФазой, превращая её в ионный канал, через который ионы Ca2+ начинают неконтролируемо поступать во внутриклеточное пространство[9][10][11][12] Примечания
|
||||||||||||||||||||||||||||||||||||||||||