Tetróxido de xenônio
Alerta sobre risco à saúde
|

|
|
| Nome IUPAC
|
Tetraóxido de xenônio
Óxido de xenônio (VIII)
|
| Outros nomes
|
Tetróxido de xenônio
|
| Identificadores
|
| Número CAS
|
12340-14-6
|
| ChemSpider
|
21106492
|
| SMILES
|
|
| InChI
|
1/O4Xe/c1-5(2,3)4
|
| Propriedades
|
| Fórmula molecular
|

|
| Massa molar
|
195.29 g mol−1
|
| Aparência
|
Amarelo Sólido Baixa intensidade −36°C
|
| Densidade
|
? g cm−3, Sólido
|
| Ponto de fusão
|
−35.9 °C
|
| Ponto de ebulição
|
0 °C[1]
|
| Estrutura
|
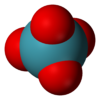
| Forma molecular
|
Tetraédrica[2]
|
| Momento dipolar
|
0 D
|
| Termoquímica
|
Entalpia padrão
de formação ΔfHo298
|
+153.5 kcal mol−1 [3]
|
Entropia molar
padrão So298
|
? J.K−1.mol−1
|
| Riscos associados
|
| Classificação UE
|
Explosivo 
|
| Compostos relacionados
|
| Compostos relacionados
|
Ácido Perxênico
Trióxido de Xenônio
|
| Página de dados suplementares
|
| Estrutura e propriedades
|
n, εr, etc.
|
| Dados termodinâmicos
|
Phase behaviour
Solid, liquid, gas
|
| Dados espectrais
|
UV, IV, RMN, EM
|
Exceto onde denotado, os dados referem-se a
materiais sob condições normais de temperatura e pressão
Referências e avisos gerais sobre esta caixa.
Alerta sobre risco à saúde.
|
Tetróxido de xenônio é um composto químico de xenônio e oxigênio com fórmula molecular XeO4, notável por ser um composto relativamente estável de um gás nobre. É um sólido amarelo cristalino que é estável abaixo de -35,9 °C , acima dessa temperatura ele é muito propenso a explodir, decompondo-se em xenônio e oxigênio ( ).[4][5]
).[4][5]
Todos os oito elétrons de valência do átomo de de xenônio estão envolvidos nas ligações com o oxigênio, e o estado de oxidação do átomo de xenônio é +8. O oxigênio é o único elemento que pode trazer o xenônio até o seu estado de oxidação mais alto, mesmo o flúor só consegue formar o  .
.
Reações
Em temperaturas acima de -35,9 °C, tetróxido de xenônio é muito propenso a explosão, decompondo-se em xenônio gasoso e oxigênio com  :
:

 é um óxido ácido e, ao reagir com água forma o instável ácido perxênico (
é um óxido ácido e, ao reagir com água forma o instável ácido perxênico ( , e ao reagir com bases forma o perxenato correspondente:
, e ao reagir com bases forma o perxenato correspondente:


Também se conhece os compostos  e
e  , instáveis e que também apresentam
, instáveis e que também apresentam  com número de oxidaçãode +8. Eles são obtidos pela reação do tetróxido de xenônio com o
com número de oxidaçãode +8. Eles são obtidos pela reação do tetróxido de xenônio com o  .[6]
.[6]
Síntese
Todas as sínteses começam a partir dos perxenatos, que são acessíveis a partir dos xenatos através de dois métodos. Um deles é o desproporcionamento de uma solução básica de xenatos para perxenatos e  :
:

Outro é a oxidação de uma solução básica de xenato pelo ozônio:

O tetróxido de xenônio pode ser obtido pelo tratamento da solução de perxenato resultante com um sal de Bário  formando precipitado de perxenato de bário que é combinado com ácido sulfúrico formando o ácido perxênico instável e sulfato de bário. O ácido perxênico formado é desidratado formando XeO4.
formando precipitado de perxenato de bário que é combinado com ácido sulfúrico formando o ácido perxênico instável e sulfato de bário. O ácido perxênico formado é desidratado formando XeO4.
O ácido perxênico formado pela reação do  com
com  ou resultante da reação de uma solução de perxenato é instável e lentamente sofre dismutação em ácido xênico e oxigênio:
ou resultante da reação de uma solução de perxenato é instável e lentamente sofre dismutação em ácido xênico e oxigênio:
 .
.
Referências
- ↑
Lide, David R. (1998). Handbook of Chemistry and Physics 87 ed. Boca Raton, FL: CRC Press. 494 páginas. ISBN 0-849-30475-X. OCLC 30677089
Lide, David R. (1999). CRC handbook of chemistry and physics : CRCnetBASE 1999. Boca Raton, FL: Chapman & Hall/CRCnetBASE. ISBN 0-849-39720-0. OCLC 41485442
- ↑ G. Gundersen, K. Hedberg, J. L.Huston (1970). «Molecular Structure of Xenon Tetroxide, XeO4». J. Chem. Phys. 52 (2): 812–815. doi:10.1063/1.1673060
- ↑ Gunn, Stuart R. (1 de maio de 1965). «The Heat of Formation of Xenon Tetroxide1». Journal of the American Chemical Society. 87 (10): 2290-2291. ISSN 0002-7863. doi:10.1021/ja01088a038
- ↑ H.Selig , J. G. Malm , H. H. Claassen , C. L. Chernick , J. L. Huston (1964). «Xenon tetroxide -Preparation + Some Properties». Science. 143 (3612). 1322 páginas. JSTOR 1713238. PMID 17799234. doi:10.1126/science.143.3612.1322
- ↑ J. L. Huston, M. H. Studier, E.N. Sloth (1964). «Xenon tetroxide - Mass Spectrum». Science. 143 (3611). 1162 páginas. JSTOR 1712675. PMID 17833897. doi:10.1126/science.143.3611.1161-a
- ↑ Housecroft, C. E. (2008). Inorganic chemistry (em inglês) 3 ed. Harlow (Inglaterra): Pearson Education Limited. ISBN 978-0-13-175553-6
Nota


















