|
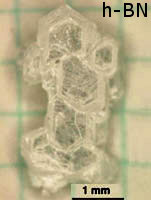
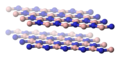
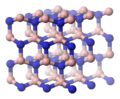
Nitreto de boroO nitreto de boro é um composto químico binário do boro, que apresenta fórmula molecular BN. É um composto que apresenta somente ligações covalentes. O nitreto de boro é obtido junto com o óxido de boro reagindo-se o boro com oxigênio e nitrogênio do ar atmosférico, em temperaturas elevadas. É um isolante elétrico, porém, conduz o calor tão bem quanto os metais. É empregado na obtenção de materiais tão duros quanto o diamante. Nitreto de boro cúbico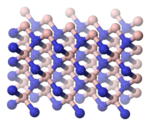 O nitreto de boro cúbico (c-BN) é um material artificial extremamente duro, mas com uma dureza inferior ao do diamante à temperatura ambiente, apesar de mais estável quimicamente. Atinge 2000 °C sem grandes perdas de dureza, enquanto o diamante já grafitiza em torno de 900 °C. Tal qual o diamante, o c-BN é um isolante elétrico e um excelente condutor de calor. É amplamente utilizado como um abrasivo para ferramentas industriais, em especial para a usinagem de peças de aços e materiais de grande dureza. FabricaçãoO c-BN é produzido a partir do tratamento do nitreto de boro hexagonal a altas pressões e temperaturas, da mesma forma que é produzido o diamante artificial a partir da grafite. A conversão direta de nitreto de boro hexagonal em nitreto de boro cúbico ocorre a pressões superiores a 18 GPa e temperaturas entre 1730 °C e 3230 °C. A adição de pequenas quantidades de óxido de boro pode reduzir a pressão requerida entre 4 GPa a 76 GPa, e a temperatura em torno de uns 1500 °C. Industrialmente, são utilizados diferentes tipos de catalisadores para provocar a reação, os quais variam segundo o método de produção. Exemplo: lítio, potássio ou magnésio, seus nitretos, água com compostos de amoníaco, etc. Nitreto de boro hexagonalA forma cristalina mais estável é a hexagonal, também chamada de h-BN, α-BN, g-BN e nitreto de boro grafítico. O nitreto de boro hexagonal (grupo pontual = D3h; grupo espacial = P63/mmc) tem uma estrutura em camadas semelhante à do grafite. Dentro de cada camada, os átomos de boro e nitrogênio são ligados por fortes ligações covalentes, enquanto as camadas são mantidas juntas por forças fracas de van der Waals.
No entanto, o “registro” entre as camadas dessas folhas é diferente do padrão observado no grafite, pois os átomos estão eclipsados, com os átomos de boro sobrepostos e acima dos átomos de nitrogênio. Esse registro reflete a polaridade local das ligações B-N, bem como as características N-doador/B-aceitador entre camadas. Da mesma forma, existem muitas formas metaestáveis que consistem em poliptipos empilhados de forma diferente. Portanto, o h-BN e o grafite são vizinhos muito próximos, e o material pode acomodar o carbono como um elemento substituinte para formar BNCs. Foram sintetizados híbridos BC6N, nos quais o carbono substitui alguns átomos de B e N.[4] A monocamada de nitreto de boro hexagonal é análoga ao grafeno, tendo uma estrutura de treliça em forma de favo de mel com quase as mesmas dimensões. Ao contrário do grafeno, que é preto e condutor elétrico, a monocamada de h-BN é branca e isolante. Ela foi proposta para ser usada como substrato isolante atômico plano ou como barreira dielétrica de tunelamento em eletrônica 2D.[5] Nitreto de boro wurtziteA forma wurtzita do nitreto de boro (w-BN; grupo pontual = C6v; grupo espacial = P63mc) tem a mesma estrutura da lonsdaleita, um raro polimorfo hexagonal de carbono. Como na forma cúbica, os átomos de boro e nitrogênio são agrupados em tetraedros.[6] Na forma wurtzita, os átomos de boro e nitrogênio são agrupados em anéis de 6 membros. Na forma cúbica, todos os anéis estão na configuração de cadeira, enquanto no w-BN os anéis entre as “camadas” estão na configuração de barco. Relatórios otimistas anteriores previam que a forma wurtzita era muito forte e foi estimada por uma simulação como tendo uma força 18% maior do que a do diamante. Como existem apenas pequenas quantidades do mineral na natureza, isso ainda não foi verificado experimentalmente.[7] Sua dureza é de 46 GPa, um pouco mais dura do que os boretos comerciais, mas mais suave do que a forma cúbica do nitreto de boro.[8]
Estabilidade térmicaO BN hexagonal e cúbico (e provavelmente o BN wurtzita) apresentam estabilidade química e térmica notáveis. Por exemplo, o h-BN é estável à decomposição em temperaturas de até 1.000 °C no ar, 1.400 °C no vácuo e 2.800 °C em uma atmosfera inerte. A reatividade do h-BN e do c-BN é relativamente semelhante, e os dados do c-BN estão resumidos na tabela abaixo.
A estabilidade térmica do c-BN pode ser resumida da seguinte forma:
Ver tambémReferências
|
Portal di Ensiklopedia Dunia