|
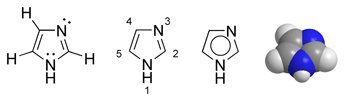
Imidazol
Imidazol é um composto orgânico de fórmula C3H4N2. Este composto aromático heterocíclico é classificado como alcaloide. Imidazol também pode se referir a classe de compostos heterocíclicos com estrutura de anel aromático similar, mas com vários substituintes. Esta classe de composto heterocíclicos e importante bloco de construção de compostos bioquímicos como histidina e seu hormônio relacionado histamina. Imidazol também serve como base ou ácido fraco. Muitos fármacos contêm o anel imidazólico, como antifúngicos e o nitroimidazol.[5][6][7][8][9] DescobertaImidazol foi primeiramente sintetizado por Heinrich Debus em 1858, mas vários derivados de imidazole foram descobertos anteriormente, na década de 1840. Esta síntese, mostrada abaixo, utiliza glioxal e formaldeído na presenca de amônia . Ainda que seja considerada de baixa eficiência, esta reação ainda e utilizada.[10]  Estrutura e propriedadesImidazol possui um anel planar de 5-membros, solúvel em água e outros solventes polares, com um dipolo de 3.61D. Sua ocorrência está relacionada a duas formas tautoméricas equivalentes, em função do átomo de hidrogênio poder estar localizado em qualquer um dos dois átomos de nitrogênio. É classificado como composto aromático em função da presença de um sexteto de ligações. Algumas estruturas de ressonância estão relacionadas abaixo:  AnfotericidadeImidazol é composto anfótero, i.e. pode ser usado como ácido ou como base. Como ácido, o pKa of e 14.5, sendo menos ácido do que ácidos carboxílicos, fenóis, e imidas. O próton ácido está localizado no nitrogênio N-1. Como base,o pKa do conjugado ácido e aproximadamente 7, tornando este composto cerca de sessenta vezes mais básico que piridina. Preparação Imidazol pode ser sintetizado por inúmeros métodos. Na literatura, estes métodos são comumente classificados de acordo com a forma e o número de ligações que são feitas para formar o anel imidazólico. Por exemplo, o método de Debus forma as ligações (1,2), (3,4), e (1,5) utilizando cada reagente como um fragmento do anel, logo este seria um método de formação de 3 ligações, conforme pode ser visto abaixo:  Aplicações biológicasImidazol está presente em várias moléculas de importância biológica, como o aminoácido histidina, que possui o anel imidazólico em sua cadeia lateral. Histidina pode ser descarboxilada e transformada em histamina, conforme abaixo:  Outra aplicação do imidazol é a purificação de proteínas recombinantes marcadas com um cauda de histina, através de cromatografia de afinidade com iões metálicos imobilizados. O imidazol é utilizado na etapa de eluição, no qual um excesso deste composto é aplicado na coluna, competindo pela ligação com o metal através de coordenação química, libertando assim as proteínas. Imidazole tem se tornado bastante importante para industria farmacêutica. Imidazoles sintéticos estão presentes em muitos fungicidas, antiprotozoários e anti-hipertensivos. Imidazol também faz parte do composto teofilina, um estimulante do sistema nervoso central, encontrado em folhas de chá e em feijões. Também esta presente em fármacos anticancer, como mercaptopurina, que interfere no genoma. Aplicações industriaisImidazol tem sido utilizado intensivamente como inibidor de processos corrosivos em metais de transição, como o cobre. Derivados de imidazol possuem importância industrial e tecnológica, como o polibenzimidazol (PBI). O PBI contem o anel imidazólico fusionado com o anel benzênico e possui e aplicado contra incêndios. Sais de imidazolSais de imidazol são formados através da protonação ou substituição no nitrogênio do imidazol. Estes sais são utilizados como precursores de carbenos estáveis. Sais onde o o imidazol esta desprotonado também são possíveis. Derivados do imidazolTodos terminam em "azol"[11]:
IndicaçõesOs derivados do imidazol são usados para tratar as seguintes micoses e protozoonoses[12]:
Ver também
Referências
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Portal di Ensiklopedia Dunia