|
ピレスロイドピレスロイド(pyrethroid)とは、除虫菊 (Tanacetum cinerariifolium (Trevir.) Sch. Bip.) に含まれる殺虫成分の総称で、今日では各種誘導体が合成され、各地で広く殺虫剤として利用されている。天然に産するピレスロイドは菊酸を共通構造として持っており、ピレトリン I (Pyrethrin I) とピレトリン II (Pyrethrin II) を主成分とする6種の化合物の混合物である。また、微量成分のピレスロイドとしてシネリン I、シネリン II あるいはジャスモリン I、ジャスモリン II も含まれ、いずれもピレトリンと同様な作用を有する。 人工的に合成したピレトリンの誘導体は合成ピレスロイドと呼ばれ、アレスリンなどが知られている。開発初期の合成ピレスロイドには菊酸構造が存在したものの、現在の合成ピレスロイドに、もはや共通の化学構造は存在しない。 いずれのピレスロイド類も、昆虫類・両生類・爬虫類の神経細胞に作用し、イオンチャネルの1種であるNa+チャネルを持続的に開いて、脱分極を生じさせる神経毒である。しかしながら、哺乳類・鳥類に対する毒性は低い。このため殺虫剤として使用しても哺乳類や鳥類にとっては比較的安全である。 ただし、例えば特異体質のヒトで、ピレスロイド類を吸入した場合に、喘息発作などを誘発する場合があるため、そのような体質の場合は注意が必要である。 構造天然ピレスロイドは、水酸基を有したピレスロロンと、カルボキシ基を有した菊酸とが脱水縮合して、エステル結合した構造をしている。 菊酸 →詳細は「菊酸」を参照
菊酸(きくさん、chrysanthem(um)ic acid)はシクロプロパンカルボン酸の1種で、テルペノイドである。1891年にシュラクデンホーフェン (Schlagdenhauffen) とレーブ (Reeb) が、除虫菊を水蒸気蒸留する方法で単離した。菊カルボン酸 (chrysanthemum-monocarboxylic acid) とも呼ばれる。 化学式 C10H16O2 で、分子量は168.23である。IUPAC名は (1R,3R)-2,2-ジメチル-3-(2-メチル-1-プロペニル)シクロプロパンカルボン酸、CAS登録番号は4638-92-0。常圧での融点は17 ℃から21 ℃程度で、不安定な黄色の油様物質として存在し、殺虫作用を持つ。しかし、光、空気酸化により分解して失活する。不揮発性で、水などの極性溶媒には溶け難い。 ピレスロロンピレスロロン(Pyrethrolone) は、ピレトリンのエステル結合を加水分解した際に、菊酸から切り離される、 (1S)-2-メチル-4-オキソ-3-(2Z)-2,4-ペンタジエニル-2-シクロペンテン-1-オールに付けられた慣用名である。 利用 経緯1910年に、スイスのチューリッヒ工科大学に所属していたヘルマン・シュタウディンガーが、シロバナムシヨケギクの殺虫成分を発見し、その化学構造式を発表した。同氏はこれをピレトリンと命名し、昆虫の体内での作用や、温血動物には無害であることなどを発表した。これを受けて、乾燥させたシロバナムシヨケギクの花の粉末が農薬として利用され、その後、除虫菊は世界的に広く利用されていった。さらに、マラリアや黄熱病などを媒介する蚊を駆除する目的でも、除虫菊は活用されていった。 日本へは明治時代に除虫菊が導入され、1890年に大日本除虫菊(金鳥)創業者の上山英一郎が、江戸時代以来の「蚊遣り火」に除虫菊を応用した蚊取線香を発明し、それが普及した結果、日本ではピレスロイドが殺虫剤として広く利用されるようになった。第2次世界大戦前の日本は、殺虫剤として用いるための除虫菊の世界的な産地であった。例えば、広島県の因島市などは除虫菊の主産地の1つとして知られていた[1]。しかし戦争によってその座を失った。敗戦後の日本では工業化が進むにつれて、住友化学が除虫菊に含まれるピレスロイドを工業的に全化学合成する技術を確立した[2]。このような背景もあり、今日では除虫菊の利用がかつてより減少し「蚊取り線香」と呼ばれる製品であっても、合成されたピレトリンやアレトリン等の合成ピレスロイドを殺虫成分として使用している[注釈 1]。 また、特に第2次世界大戦以降は、DDTなど有機塩素系農薬が強力な殺虫剤として汎用されていった。しかし、有機塩素系農薬の環境中での残留性・生物への蓄積性が問題となり、DDTが1973年にアメリカ合衆国環境保護庁(EPA)によって製造禁止措置が実施された[3][注釈 2]。この結果、再び合成ピレスロイドも、疾患を媒介する虫の駆除のために、一般的に利用されるようになり、さらに、新規の合成ピレスロイドの開発も進んでいった。 日本などでは、蚊取り線香やスプレー式殺虫剤に合成ピレスロイドが利用される。一方で、中央アフリカなどでは、合成ピレスロイドを吸着させた蚊帳も利用されている。 しかしピレスロイド耐性の蚊が1996年に発見され、さらにダニ・トコジラミ・ゴキブリにも耐性種が発見されたため、製薬会社はオキサジアゾール(メトキサジアゾンなど)を配合するなどの対策を講じた[4]。 特色天然ピレスロイドのピレトリンは、光・酸素・アルカリに不安定で、環境中に揮発した後は速やかに分解・失活する短時間作用型の防虫剤であり、この性質は農薬としては欠点でもある。また除虫菊を原料とするのでは、天候に左右され大量生産は困難であるため、20世紀前半から合成ピレスロイドが研究され、実用化されるようになった。 合成ピレスロイドの実用化により、農薬・家庭内殺虫剤として、ピレスロイド系薬剤が広く利用されるようになり、エアロゾル剤(殺虫スプレー缶)、燻蒸剤、揮発製剤(防虫シート)、乳剤(防疫用・園芸用)と、多様な利用形態が開発されている。 ピレスロイドは、哺乳類や鳥類に対して、あまり毒性を発揮せずに[5]、昆虫などには強い毒性を発揮するという選択毒性を有するため、最も身近に利用されている殺虫剤である。害虫駆除のためのピレスロイドの利点を列挙すると、速効性、忌避効果(嫌がってピレスロイド濃度の高い部分に近づかない)、フラッシングアウト(隠れている虫を追い出して殺す効果)、安全性(人間など、恒温動物に対して有害性が極めて低く、光や酸素で速やかに分解されるため、残効性が無い)が挙げられる[5]。 天然ピレスロイドピレトリンピレトリン (Pyrethrin)は1919年と1923年に山本の構造決定の報告があるが、1924年にスイスのヘルマン・シュタウディンガーとレオポルト・ルジチカによって、殺虫活性物質の主成分の構造が決定され、彼らによりピレトリンと命名された。 ピレトリンは混合物で、ピレトリン I とピレトリン II が含まれ、いずれも殺虫作用を持つ。昆虫類の神経には強力に作用するが、哺乳類や鳥類に対する作用は比較的弱く、昆虫の致死に必要な濃度程度では、哺乳類や鳥類に対しては事実上作用を示さないため、除虫菊としての使用を含め、人畜用の防虫剤として古くから利用されてきた。しかしながら、光や空気酸化により速やかに失活するので、作用時間が短い。また、ヒトであっても、皮膚に直接塗布した際などに、アレルギーを誘発する場合がある。 なお、哺乳類や鳥類に対して全くの無害というわけではない。ヒトの場合でも、高い濃度で大量のピレトリンに曝露されると、皮膚の紅斑、皮膚炎、丘疹、掻痒などの皮膚症状、気管支喘息、傾眠、血管運動神経性の鼻炎、アナフィラキシー様反応、口唇のしびれ感、吐き気、下痢、耳鳴り、頭痛、情動不安、協調運動障害、間代性痙攣、知覚麻痺、衰弱など神経症状が現れる場合がある。重篤な場合は、中枢性の呼吸停止により、死亡に至る場合がある。また、劇症のアレルギーであるアナフィラキシー様反応などに陥った場合も、放置すると危険である。
シネリン 1945年に除虫菊から再発見されたピレスロイドである。ピレトリンと同様な作用を持つ。皮膚に直接塗布してアレルギーを誘発する例がある。大量のシネリンに曝露されると、紅斑、皮膚炎、丘疹、掻痒などの皮膚症状、喘息、傾眠、血管運動神経性鼻炎、アナフィラキシー様反応、口唇のしびれ感、吐き気、下痢、耳鳴り、頭痛、情動不安、協調運動障害、間代性痙攣、知覚麻痺、衰弱など神経症状が現れる場合がある。重篤な場合は中枢性の呼吸停止により死に至る場合がある。
ジャスモリン ジャスモリン(Jasmoline)のアルコール成分は、ジャスミンの香り成分であるジャスモンの4位に、ヒドロキシ基が付いたアルコールである。他のピレスロイドと同様に殺虫作用を持つ。
合成ピレスロイドアレスリン アレスリンII (R = −COOCH3) →詳細は「アレスリン」を参照
アレスリン(Allethrin)はピレトリンの構造を元に、初めて全化学合成によって創造された殺虫剤で、構造が異なるアレスリン I、アレスリン II が知られている。なお、いずれも立体不明の混合物として合成および命名されているので、アレスリンと呼んだ場合は、8種の異性体混合物を指す。
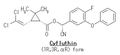
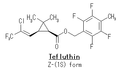
その他の合成ピレスロイド
脚注注釈
出典
関連項目 |
Portal di Ensiklopedia Dunia