|
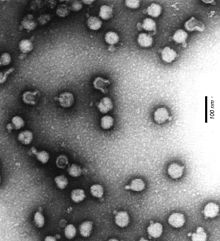
AlphavirusAlphavirus (nella letteratura in lingua italiana talora Alfavirus) è un genere di virus ad RNA a singolo filamento positivo, unico membro della famiglia dei Togaviridae, di medie dimensioni, forma rotondeggiante, nucleocapside a simmetria icosaedrica avvolto da membrana lipoproteica, in grado di infettare numerosi vertebrati per mezzo di artropodi[1]. Ubiquitari e distribuiti in sette gruppi sierologici[2], gli Alphavirus determinano due gruppi di patologie: encefaliti[3] e sindromi febbrili con eruzioni cutanee e poliartriti[4]. TassonomiaIl genere Alphavirus è rappresentato da una trentina di specie di virus patogeni trasmessi da zanzare distribuiti in sette gruppi sierologici[2][5]. La specie tipo è il virus Sindbis. In passato il genere Alphavirus era classificato fra gli Arbovirus, precisamente nel gruppo A degli Arbovirus, assieme a virus a RNA classificati successivamente nelle famiglie Flaviviridae[6] e Arteriviridae[7]. Caratteristiche viraliMorfologia Al microscopio elettronico i virioni degli Alphavirus appaiono costituiti da un nucleocapside a simmetria icosaedrica (numero di triangolazione T = 4) ricoperto da una membrana lipoproteica virale. I virioni appaiono di forma sferica (diametro di circa 40 nm) o pleiomorfi (diametro di circa 60-70 nm) localizzati nel citoplasma della cellula ospite. La membrana virale è originata dalla membrana della cellula infettata; sulla sua superficie appaiono prolungamenti lunghi circa 10 nm costituiti da glicoproteine virali, di cui due (denominate E1 ed E2) sono antigenicamente ben caratterizzate e permettono una classificazione sierologica degli Alphavirus[8]. Proprietà fisico-chimicheLa massa molecolare dei virioni è 52 x 106 dalton. I virioni hanno una densità di flottazione in saccarosio di 1,18-1,19 g cm−3; il coefficiente di sedimentazione è di 280 svedberg (s20,w). Il punto di inattivazione termica (Thermal inactivation point, TIP) è a 58 °C. I virioni sono costituiti per il 30% in peso di lipidi, presenti nella membrana lipoproteica virale, di composizione simile ai lipidi delle membrane cellulari delle cellule ospiti. La longevità in vitro (Longevity in vitro, LIV) è 0,35 giorni (a 37 °C in terreno di coltura). In vitro le proprietà dei virioni sono stabili in ambiente blandamente alcalino (pH 7-8). L'infettività è ridotta dopo irraggiamento. A causa della presenza di lipidi, i virioni sono sensibili al trattamento con solventi organici (per esempio, etere) e detergenti[9]. GenomaIl genoma degli Alphavirus è costituito da un singolo filamento positivo di RNA di circa 11800 nucleotidi[10]. L'estremità 5' porta un cappuccio di 7-metil guanosina metilata e l'estremità 3' una coda poliadenilata. Dopo la penetrazione nella cellula infettata, l'RNA virale scapsidato funziona da RNA messaggero, dirigendo la sintesi delle proteine virali. Viene sintetizzato dapprima un singolo lungo polipeptide che successivamente viene tagliato in frammenti per formare un certo numero di proteine più piccole. Si ha prima la traduzione dell'estremità 5', che codifica per le proteine funzionali; dopo la replicazione del genoma vengono prodotti mRNA subgenomici che produrranno le proteine strutturali corrispondenti all'estremità 3'[11]. I nucleocapsidi completi acquistano l'involucro dalla membrana plasmatica cellulare e solo allora il virione diviene infettivo. Patogenicità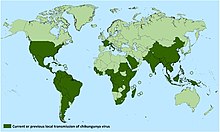  Gli Alphavirus sono diffusi in tutto il mondo e sono in grado di causare malattie anche all'uomo. Le infezioni da Alfavirus si diffondono attraverso artropodi vettori, soprattutto zanzare. Una volta che un vertebrato viene morso dalla zanzara infetta, il virus può entrare nel flusso sanguigno, provocando viremia. A loro volta le zanzare acquisiscono il virus ingerendo sangue di un ospite viremico; il virus si moltiplica nei tessuti e negli organi della zanzara, comprese le ghiandole salivari. Nella maggior parte dei casi i vertebrati infettati appaiono sani e non infetti (per esempio, gli uccelli nell'encefalite equina dell'ovest (Western equine encephalitis virus). Altre volte, tuttavia, compaiono malattie. Nell'uomo queste ultime sono essenzialmente di due categorie:
Nel singolo individuo la comparsa delle malattie da Alphavirus può essere impedita dal sistema immunitario: nell'immunità specifica sono coinvolti anticorpi neutralizzanti e cellule T; gli Alphavirus sono in grado di provocare inoltre la produzione di interferone[12].
Note
Bibliografia
Altri progetti
Collegamenti esterni
|
Portal di Ensiklopedia Dunia