|
HenipavirusHenipavirus
Microscopie électronique en transmission montrant un virus Hendra intact ainsi qu'une nucléocapside libre, marqués à l'or colloïdal avec le sérum d'un humain convalescent[1]. Espèces de rang inférieur Position :
Henipavirus est un genre de virus de la famille des Paramyxoviridae[3], ordre des Mononegavirales, virus à ARN monocaténaire de polarité négative et à génome non segmenté. On y compte notamment le virus Hendra, initialement classé comme morbillivirus des équidés, et le virus Nipah, à l'origine d'épidémies d'infections à virus Nipah en Asie du Sud et du Sud-Est : le mot « henipavirus » est une contraction de ces deux noms de virus. Les virus du genre Henipavirus sont caractérisés par leur grande taille (18,2 kilobases[4]), leur occurrence naturelle chez les chauves-souris du genre Pteropus (roussettes), et leur émergence récente comme pathogène zoonotique potentiellement mortel chez les animaux domestiques et les humains. L'ARN de ces virus a également été identifié dans les déjections de roussettes paillées africaines au Ghana[5], indiquant la présence du virus en Afrique subsaharienne, dans la mesure où cette chauve-souris est très largement distribuée sur le continent. StructureLes virions d’Henipavirus sont pléomorphes, c'est-à-dire qu'ils présentent des formes variables, avec une taille variant de 40 à 600 nm de diamètre[6]. Ils sont recouverts d'une enveloppe virale formée d'une bicouche lipidique recouvrant des protéines de matrice notées M. La surface du virus présente des glycoprotéines G assurant l'adhérence (attachment en anglais) du virus sur la cellule hôte, en particulier sur l'éphrine B2, une protéine hautement conservée présente chez de nombreux mammifères[7],[8], et des trimères de protéines F assurant la fusion de la membrane virale avec la membrane plasmique de la cellule hôte, un effet collatéral étant la formation dans grands syncytia résultant de la fusion de plusieurs cellules hôtes voisines sous l'effet de cette protéine virale[9] ; la structure tridimensionnelle de la protéine d'attachement G du virus Nipah a été établie par cristallographie aux rayons X[10]. L'intérieur du virus est constitué d'un ARN viral et d'une protéine N de nucléocapside complexée avec une protéine L fonctionnant comme enzyme de type ARN polymérase ARN-dépendante elle-même liée à une phosphoprotéine P indispensable à l'activité enzymatique de la protéine L.  Génome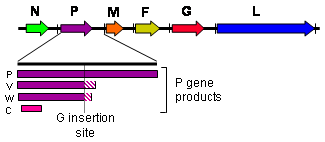 Le génome des Henipavirus est long de 18,2 kilobases et code six protéines structurelles[4]. Comme c'est la règle chez les paramyxovirus[13], le nombre de nucléotides dans ce génome est un multiple de six, ce qu'on appelle « la règle de six[14] ». Un écart par rapport à cette règle, par mutation ou formation d'un génome incomplet, rend inefficace la multiplication du virus[15], vraisemblablement du fait de contraintes structurelles dues à l'interaction entre l'ARN et la nucléoprotéine N du virus[16]. Ces virus expriment plusieurs protéines différentes à partir de leur gène P à la suite d'un processus d'édition des ARN messagers, dans ce cas par une modification post-transcriptionnelle consistant en l'ajout d'un ou deux résidus de guanosine au niveau d'un site d'édition du gène P avant sa transcription par les ribosomes de la cellule hôte[11] : le gène P produit ainsi une protéine P à partir de l'ARN messager non modifié, une protéine V dans le cas de l'insertion d'un résidu de guanosine, et une protéine W dans le cas de l'insertion de deux résidus de guanosine ; un quatrième produit de transcription, la protéine C, résulte d'un cadre de lecture ouvert alternatif. Si la phosphoprotéine P contribue à l'activité ARN polymérase ARN-dépendante de la protéine L, les protéines V, W et C jouent un rôle d'inhibiteur des défenses antivirales de la cellule hôte, sans que les mécanismes exacts de leur mode d'action soit bien compris[11],[12]. Virus de HendraApparitionL'Hendravirus a été découvert en Australie en septembre 1994, quand il a causé la mort de trente chevaux et d'un entraîneur à Hendra, une banlieue de Brisbane dans le Queensland. Le premier cas connu, une jument, est morte deux jours après être tombée malade. Elle était logée avec vingt-trois autres chevaux. Dix-neuf d'entre eux ont été contaminés et douze ont succombé. L'entraîneur et un garçon d'écurie qui avaient nourri la jument sont tombés malades moins d'une semaine après le décès de l'animal. Ils présentaient alors les symptômes de la grippe. Le garçon d'écurie a récupéré, mais l'entraîneur est mort de problèmes respiratoires et rénaux. Ils avaient été probablement contaminés par les éternuements de la jument. Le deuxième cas était en fait antérieur. Le virus avait déjà frappé en , dans le nord de Mackay à 1 000 km de Brisbane, mais les deux n'ont été reliés que plus tard. L'infection a tué deux chevaux et leur propriétaire. Ce dernier a été admis à l'hôpital pour une méningite, trois semaines après avoir assisté à l'autopsie de ses chevaux. Il a récupéré, mais 14 mois plus tard, il développait des troubles neurologiques et mourait peu après. C'est la présence de l'Hendravirus dans le cerveau du patient qui a permis le diagnostic a posteriori. À la suite d'analyses sériques de la faune dans les secteurs de manifestation du virus, il est apparu que les chauves-souris Pteropus étaient la source la plus probable de l'infection[17], avec une séroprévalence de 47 %. Aucune des 46 autres espèces n'était positive. La présence du virus dans l'appareil reproducteur et l'urine des chauve-souris permet de penser que les chevaux ont été contaminés par l'exposition à l'urine ou au liquide amniotique des chauve-souris. Autres casTrois cas supplémentaires sont signalés : deux à Cairns dans le Queensland, en et en , et un troisième à Townsville, toujours dans le Queensland, en . Chacun a eu comme conséquence la mort d'un cheval. Un vétérinaire ayant participé à l'autopsie du cheval de Townsville a développé une maladie lié à ce virus, mais a récupéré.  La distribution des chauve-souris correspond aux sites où des cas sont apparus. Par ailleurs, leur aspect saisonnier indiqueraient qu'ils sont liés au cycle de reproduction des Pteropus. Dans la mesure où il n'y a aucune preuve de transmission directe entre la chauve-souris et l'homme, on pense que celui-ci ne peut être infecté que par l'intermédiaire d'un hôte. PathologieLes chauves-souris ne sont pas affectées par le virus Hendra. Chez les humains, on observe des symptômes respiratoires (hémorragie et œdème pulmonaire) ou encéphaliques — dans ce cas, ils se traduisent par une méningite. Chez les chevaux, l'infection entraîne habituellement un œdème pulmonaire et une congestion nasale. Virus NipahApparitionLes premières épidémies liées au virus Nipah ont eu lieu à Singapour et en Malaisie en 1998. Cependant le virus Nipah a été identifié en 1999 où il a causé un cas de maladie neurologique et respiratoire aux fermes de porc en Malaisie péninsulaire, ayant pour résultat le décès de 115 personnes sur 265[18] et l'euthanasie d'un million de porcs[19]. À Singapour, onze cas dont un mortel se sont produits avec des ouvriers d'abattoir exposés aux porcs importés des fermes malaisiennes affectées. Les réservoirs naturels du virus Nipah sont les chauves-souris frugivores du genre Pteropus. La déforestation en Asie du Sud-Est a entraîné la destruction de leur habitat. Elles ont donc migré afin de trouver de la nourriture, et se sont réfugiées vers les fermes où elles ont infecté la nourriture des porcs. En effet, le virus est contenu entre autres dans leur salive. Le porc contaminé excrète par de fortes toux le virus et contamine à son tour l'homme. Il est donc un hôte intermédiaire et aussi un puissant vecteur de l'infection. Les symptômes de l'infection du cas malaisien étaient principalement encéphalitiques chez l'homme et respiratoires chez les porcs. Les manifestations postérieures ont causé des maladies respiratoires chez l'homme, augmentant la probabilité de la transmission humain-à-humain et indiquant l'existence des contraintes plus dangereuses du virus. Autres casSix cas supplémentaires de virus Nipah se sont produits depuis 1998, un en Inde et cinq au Bangladesh. Tous les emplacements de ces cas se trouvent en dessous de la zone des espèces de Pteropus (Pteropus giganteus). Comme avec le virus Hendra, la synchronisation des manifestations indique un effet saisonnier.
Onze cas isolés d'encéphalite dus au virus Nipah ont été également référencés au Bangladesh depuis 2001. Le virus Nipah a été isolé dans la chauve-souris de Lyle (Pteropus lylei) au Cambodge[22] et l'ARN viral a été trouvé dans l'urine et la salive de la chauve-souris de Lyle et des larves de Horsfield (Hipposideros larvartus) de Thaïlande[23]. Les cas cambodgiens montrent que le virus est identique à 98 % avec le virus causant les cas de 1998. On n'a observé aucune infection humaine ou d'autres espèces au Cambodge ou en Thaïlande. En à Nouméa, Nouvelle-Calédonie, trois roussettes du parc forestier ont été diagnostiquées porteuses du virus Nipah[24]. Les animaux ont été euthanasiés[25]. PathologieChez l'humain, les infectés présentent de la fièvre, des maux de tête et de la somnolence. La toux, la douleur abdominale, la nausée, le vomissement, la faiblesse, les problèmes avec l'ingestion et la vision brouillée sont relativement communs. 1/4 des patients ont eu des malaises et environ 60 % sont devenus comateux et ont pu avoir besoin d'aide respiratoire. Les patients présentant des formes graves de la maladie ont développé de l'hypertension grave, une fréquence cardiaque et une température très élevées. Le virus Nipah est également connu pour causer des encéphalites lors des rechutes. Parmi les cas malaisiens initiaux, un patient a présenté une encéphalite environ 53 mois après son infection initiale. Il n'y a aucun traitement définitif pour l'encéphalite de Nipah, indépendamment des mesures de support, telles que la ventilation mécanique et la prévention de l'infection secondaire. La ribavirine, un médicament antiviral, a été testée dans les infections malaisiennes et les résultats sont encourageants, cependant des études sont encore nécessaires. Chez les autres animaux, particulièrement chez les porcs, le virus cause des syndromes respiratoires et neurologiques. Causes d'apparitionL'apparition des henipavirus s'est faite en parallèle de l'apparition d'autres virus zoonotiques dans les décennies récentes. Les virus responsables du SRAS et de la maladie à virus Ebola (entre autres) ont aussi été probablement 'hébergés' par des chauves-souris et sont capables d'infecter une variété d'autres espèces. L'apparition de chacun de ces virus a été liée à une augmentation des contacts entre les chauves-souris et les humains, impliquant parfois un hôte intermédiaire. Le contact accru est conduit par l’empiétement humain dans le territoire des chauves-souris (dans le cas de Nipah, les élevages porcins sont dans ledit territoire) et par le mouvement des chauves-souris vers les populations humaines dû aux changements dans l'habitude alimentaire et à la perte d'habitat. Il est évident que la perte d'habitat des chauves-souris en Asie du sud et en Australie (en particulier le long de la côte est) aussi bien que l'empiétement des logements humains et de l'agriculture dans les habitats restants, vont créer un plus grand contact entre les hommes et les chauves-souris. Notes et références
Voir aussiRéférences biologiques
Bibliographie
Liens externes
|
