|
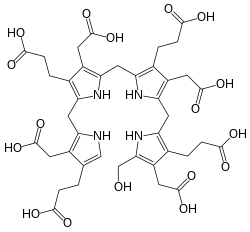
Hydroxymethylbilan
Hydroxymethylbilan (HMB), auch bekannt als Prä-Uroporphyrinogen, ist eine organische Verbindung, die in lebenden Organismen bei der Synthese von Porphyrinen vorkommt, einer Gruppe kritischer Substanzen, zu denen Hämoglobin, Myoglobin und Chlorophyll gehören. HMB gehört zur Naturstoffklasse der Bilane, einer Untergruppe der Gallenfarbstoffe. StrukturDie Verbindung ist ein substituiertes Bilan, eine Kette aus vier Pyrrolringen, welche durch Methylenbrücken untereinander verknüpft sind. Die Kette beginnt mit einer Hydroxymethylgruppe −CH2−OH und endet mit einem Wasserstoffatom anstelle der verknüpfenden Methylenbrücken. Die anderen beiden Kohlenstoffatome jeder Pyrroleinheit sind jeweils mit einer Essigsäuregruppe −CH2-COOH und einer Propionsäuregruppe −CH2-CH2-COOH substituiert.[1] StoffwechselHMB wird durch das Enzym Porphobilinogen-Deaminase gebildet, indem vier aus 5-Aminolävulinsäure entstandene Porphobilinogen-Moleküle zu HMB umgesetzt werden:[2]  Das Enzym Uroporphyrinogen-III-Synthase schließt die Kette, um Uroporphyrinogen III zu bilden:[2]  Uroporphyrinogen III ist ein Porphyrinogen; einer Verbindungsklasse mit dem Hexahydroporphin-Makrozyklus als zentralem Strukturelement. In Abwesenheit des Enzyms unterliegt die Verbindung einer spontanen Cyclisierung und wird zu Uroporphyrinogen I.[3][4] Einzelnachweise
|
||||||||||||||||||||||||
Portal di Ensiklopedia Dunia