|
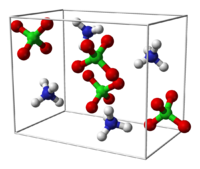
بيركلورات الأمونيوم
فوق كلورات الأمونيوم أو بيركلورات الأمونيوم هي مركب عضوي صيغته NH4ClO4. وهو ملح لحمض البيركلوريك والأمونيا. وهو مؤكسد قوي مما يفسر استخدامه بشكل أساسي في المواد الدافعة الصلبة للصواريخ. وكان سبباً في العديد من الحوادث مثل كارثة بيبكون وتحطم رحلة طيران جنوب أفريقيا رقم 295. الإنتاجتنتج فوق كلورات الأمونيوم (وتدعى أحياناً AP) بتفاعل الأمونيا مع حمض البيركلوريك، وهي السبب الرئيسي في الإنتاج الصناعي لحمض البيركلوريك. كما تنتج أيضاً بمعالجة أملاح الأمونيوم مع فوق كلورات الصوديوم، حيث تستغل هذه الطريقة أن ذوبانية NH4ClO4 هي حوالي 10% من ذوبانية فوق كلورات الصوديوم.[5] تتبلور فوق كلورات الأمونيوم إلى بلورات عديمة اللون لشبكتها البلورية شكل مجسم معيني. التفككتتفكك فوق كلورات الأمونيوم قبل الانصهار، مثلها مثل باقي أملاح الأمونيوم. ويؤدي تسخينها باعتدال إلى نشوء الكلور والنيتروجين والأوكسيجين والماء.
احتراق فوق كلورات الأمونيوم معقد إلى حد ما وتم دراسته بشكل موسع. حيث تتفكك البلورات قبل انصهارها، بالرغم من مشاهدة طبقة سائلة رقيقة على سطح البلورات خلال عملية الاحتراق تحت ضغط عالي.[6] وقد يؤدي التسخين الشديد إلى الانفجار. التفاعل التام لا يترك رواسب. والبلورات النقية لا تصمد أمام اللهب تحت ضغط أقل من 2 باسكال. فوق كلورات الأمونيوم هي مؤكسد من الصنف الرابع (يمكن أن تجري تفاعل انفجاري) عندما يكون حجم الحبيبات أقل من 15 ميكرون.[7][8] التطبيقاتتستخدم الغالبية العظمى من فوق كلورات الأمونيوم لصناعة الدوافع الصلبة.[9] عند مزج فوق كلورات الأمونيوم مع وقود (كبودرة الألومنيوم و/أو المطاط الصناعي)، يمكن أن يولد احتراق مكتفي ذاتياً على ضغوط أكبر بكثير من الضغط الجوي النظامي. وهي مؤكسد قوي استخدم لعقود طويلة في دوافع صواريخ الوقود الصلب — لصواريخ الفضاء (متضمناً المعززات ذات الوقود الصلب للمركبات الفضائية) وعسكرياً وفي صواريخ الهواة وفي بعض الألعاب النارية. بعض الإيبوكسي اللاصق «القابل للكسر» يحتوي معلق من فوق كلورات الأمونيوم. وعند التسخين لدرجة 300 °س، يتحطم اللاصق العضوي، وينكسر المفصل المتماسك. السميةفوق الكلورات بحد ذاتها قليلة السمية، فمثلاً لفوق كلورات الصوديوم جرعة المميتة للنصف LD50 قيمتها 2-4 غ/كغ ويتخلص منها سريعا بعد دخولها للمعدة.[5] لكن التعرض لها على المدى الطويل يؤدي إلى مشاكل متعددة، بما أن لها نفس أثر اليود. المراجع
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Portal di Ensiklopedia Dunia