|
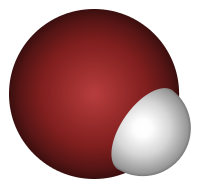
بروميد الهيدروجين
بروميد الهيدروجين هو جزيء ثنائي الذرة يتكون من عنصري H Br. وهو مادة بدء ومركب وسيط في صناعة العقاقير الطبية ، وعامل مساعد في معالجة البترول. التحضيرويمكن تحضيره بتفاعل الهيدروجين (H) مع البروم (Br) مباشرة أو بمعالجة أحد أملاح(HBr) مثل بروميد الصوديوم (NaBr) بحمض قوي غير متطاير. ويُسمى محلول بروميد الهيدروجين في الماء حمض الهيدروبروميك ويُستخدم كل من غاز بروميد الهيدروجين (HBr) ومحلوله المائي في صنع مركبات عضوية عديدة. استخدامات بروميد الهيدروجينهناك العديد من الاستخدامات (HBr) في التخليق الكيميائي. على سبيل المثال، يتم استخدام HBR لإنتاج بروميدالألكيل من الكحول: ::ROH + HBr → RBr + H2O يضاف بروميد الهيدروجين ل الكينات لإعطاء بروموالكان ، وهي عائلة هاما من مجموعة البروميدات العضوية ::RCH=CH2 + HBr → RCH(Br)–CH3 يضاف بروميد الهيدروجين ل الكينات لإعطاء بروموالكين . والكيمياء الفراغية لهذة الأنواع المضافة دائماً عكسية: :RC≡CH + HBr → RC(Br)=CH2 قاعدة ماركوفنيكوف التي تنص على : عند إضافة متفاعل غير متماثل (HX أو H-OSO3H) إلى الكين غير متماثل فان الجزء الموجب من المتفاعل يضاف إلى ذرة الكربون الحاملة لعدد أكبر من ذرات الهيدروجين والجزء السالب يضاف إلى ذرة الكربون الحاملة لعدد اقل من ذرات الهيدروجين . ::RC(Br)=CH2 + HBr → RC(Br2)–CH3 التحضير الصناعييتم إنتاج بروميد الهيدروجين (جنبا إلى جنب مع حمض الهيدروبروميك hydrobromic) بمستويات أصغر بكثير من الكلوريدات المقابلة. في التحضير الصناعي الابتدائي، يتحد الهيدروجين و البروم وتقترن في درجات حرارة تتراوح بين 200-400 درجة مئوية. وعادة ما يتم تحفيز التفاعل بواسطة البلاتين أو الاسبستوس.[7] تخليقه في المختبربروميد الهيدروجين يمكن تخليقه في المختبر بعدة طرق. يمكن تحضير في المختبر عن طريق التقطير لمحلول الصوديوم أو بروميد البوتاسيوم مع حمض الفوسفوريك أو حمض الكبريتيك المخفف:[8] :2 KBr + H2SO4 → K2SO4 + 2HBr المراجع
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Portal di Ensiklopedia Dunia