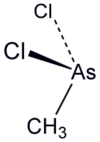|
Метилдихлороарсин
Мети́лдихло́роарси́н — арсенорганічна сполука складу CH3AsCl2. Має токсичну дію на шкіру та органи дихання. У період Першої світової війни застосовувався збройними силами Третього Рейху як отруйна речовина шкірно-наривної дії. У контексті військового застосування має позначення MD. Фізичні властивостіМетилдихлороарсин — це безбарвна рухлива рідина, що не димить на повітрі. Він добре розчиняється в органічних розчинниках. Розчиняючись у воді, зазнає гідролізу. Леткість метилдихлороарсину — 74,9 мг-хв/м³ при 20 °C. ОтриманняІсторичні методиВперше метилдихлороарсин був синтезований у 1858 році А. Беєром за двома різними методами: шляхом розкладання трихлорокакодилу за температури 40—50 °C та дією хлороводню на какодилову кислоту: Він також може бути отриманий хлоруванням диметиларсину: У 1906 році був запропонований метод отримання дією на метиларсенатну кислоту трихлоридом фосфору, який виступає одночасно і відновником, і хлорувальним агентом: Лабораторні методиОтримання у лабораторних умовах можливе шляхом реакції Маєра диметилсульфату із арсенітом натрію, синтезованим in situ. Для цього в колбу місткістю близько 1 л вносять розчин гідроксиду натрію (120 г NaOH та 150 мл води), 100 г оксиду As2O3 і нагрівають суміш на водяній бані (80 °C) до повного розчинення оксиду. Після цього при активному перемішуванні і без нагрівання поступово додають 64 г диметисульфату. Ця реакція є сильноекзотермічною і швидкість додавання має регулюватися таким чином, щоб температура розчину не перевищувала 85 °C. До колби під'єднують кульковий холодильник і вміст кип'ятять протягом 2 годин, внаслідок чого утворюється натрієва сіль метиларсенатної кислоти: Суміш охолоджують і пропускають крізь неї газуватий діоксид сірки до насичення (близько 6 годин), після чого кип'ятять протягом 1 години. При цьому на дні колби збирається оліїстий метиларсиноксид, який при охолодженні насичують пропусканням хлороводню: Вміст колби переганяють із холодильником Лібіха: спочатку відділяється надлишок хлороводню, а згодом — суміш хлороводню й метилдихлороарсину. Перегонку завершують після припинення утворення оліїстих продуктів. Суміш розділяють ділильною воронкою, а отриманий метилдихлороарсин ще раз переганяють. Отримання метилдихлороарсину у промислових масштабах здійснюють саме за цим методом. Також можливий синтез метилдихлороарсину через стадію отримання магнійорганічних сполук, в якому вихідними речовинами слугують галогеноалкани, магній і трихлороарсин. Для цього у колбу вносять 200 мл безводного тетрагідрофурану і 37 г рідкого метилхлориду. Поступово додаючи до суміші магній у кількості 17,8 г, температуру підтримують у діапазоні менше 60 °C (реакція сильноекзотермічна). Після повного додавання реакційну суміш перемішують протягом 5 хвилин та охолоджують на льоду до температури 0 °C. По завершенню охолодження у колбу по краплях додають розчин трихлориду арсену в гексані (132 г AsCl3 у 500 мл гексану). Реакційна суміш має активно перемішуватися протягом 2 годин, а її температура залишатися на рівні 0 °C. Після перемішування, для розчинення хлориду магнію, необхідно додати 100 мл холодної води і швидко перемішати суміш протягом 10 хвилин. Отриманий розчин переносять у ділильну воронку і відокремлюють нижній органічний шар, який згодом фільтрують і переганяють у вакуумі для відділення тетрагідрофурану й гексану. У вакуумі метилдихлороарсин переганяється за температури 100 °C. Кінцевий продукт може мати домішки диметилхлороарсину й триметиларсину. Хімічні властивостіЗа своїми хімічними властивостями метилдохлороарсин аналогічний до етилдихлороарсину. У воді він швидко гідролізується до метилзаміщеного арсиноксиду (безбарвних кристалів із запахом асафетиди): При дії лугів він так само розкладається: У розчинах сірководню метилдихлороарсин здатен хлоруватися до метилтетрахлороарсину, котрий є нестійким і розкладається за 0 °C: Він окиснюється у метиларсенатну кислоту під дією бромної води: Як і у випадку інших галогенованих арсинів, при дії аміаку утворюється імін: При дії сірководню утворюється метилсульфід: В розчинах етерів метилдихлороарсин не взаємодіє з магнієм та цинком, однак за наявності незначної кількості води протікає бурхлива реакція із утворенням полімерного метиларсину (CH3As)x, метану і водню. У присутності безводного хлориду алюмінію метилдихлороарсин здатен приєднувати ацетилен, утворюючи β-хлоровінільні похідні арсину (CH3)AsCl(CH=CH·Cl) та (CH3)As(CH=CH·Cl)2. ТоксичністьМетилдихлороарсин має подразнюючу дію на дихальні шляхи. При його вдиханні він діє як отруйна речовина задушливої дії та спричинює бронхопневмонію та набряк легень. Ураження відбувається при його концентрації у повітрі більше 0,1 мг/л (при 15-хвилинній дії), концентрація вище 0,3 мг/л може бути смертельною. Шкірна дія метилдихлороарсину проявляється не так сильно, як у близькоспорідненого до нього люїзиту. Утворення пухирців на уражених ділянках шкіри відбувається без прихованого періоду. Порогова концентрація, при якій виникає подразнення шкіри, становить 0,1—0,5 мг/см², а утворення пухирців — 3—5 мг/см². Джерела
|
||||||||||||||||||||||||||||||||||||