|
Изобарный процесс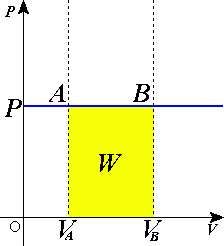  Изобари́ческий — термодинамический изопроцесс, происходящий в физической системе при постоянном внешнем давлении[1]. Согласно закону Гей-Люссака, в идеальном газе при изобарном процессе отношение объёма к температуре постоянно: . Если использовать уравнение Клапейрона — Менделеева, то работа, совершаемая газом при расширении или сжатии газа, равна Количество теплоты, получаемое или отдаваемое газом, характеризуется изменением энтальпии: ТеплоёмкостьМолярная теплоёмкость при постоянном давлении обозначается как В идеальном газе она связана с теплоёмкостью при постоянном объёме соотношением Майера Молекулярно-кинетическая теория позволяет вычислить приблизительные значения молярной теплоёмкости для различных газов через значение универсальной газовой постоянной R:
Теплоёмкости можно также определить исходя из уравнения Майера, если известен показатель адиабаты, который можно измерить экспериментально (например, с помощью измерения скорости звука в газе или используя метод Клемана — Дезорма). Изменение энтропииИзменение энтропии при квазистатическом изобарном процессе равно В случае, если изобарный процесс происходит в идеальном газе, то следовательно, изменение энтропии можно выразить как Если пренебречь зависимостью от температуры (это предположение справедливо, например, для идеального одноатомного газа, но в общем случае не выполняется), то См. такжеПримечания
Литература
|
Portal di Ensiklopedia Dunia















