|
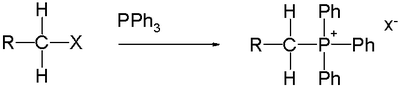
第四級ホスホニウムカチオン第四級ホスホニウムカチオン(だいよんきゅうホスホニウムカチオン)とは、ホスホニウムイオンの4つの水素全てが炭化水素基によって置換されてできたカチオンである。 第四級ホスホニウム塩は第四級ホスホニウムカチオンと他のアニオンとの塩で一般式R4P+X−を持つ。通常ホスホニウムは第四級の有機物誘導体であり、例えば塩化テトラフェニルホスホニウム(C6H5)4P+ Cl-や沃化テトラメチルホスホニウム[P(CH3)4]+I−などである。 アルキルトリフェニルホスホニウム塩は、ウィッティヒ反応中のウィッティヒ試薬の調製に広く使用されており、この塩は、トリフェニルホスフィン(トリフェニルホスファン)とハロゲン化炭化水素との反応によって製造できる。 アルキル基がメチル基や(図の様な)立体障害のない第一級アルキル基であれば反応効果は非常に良好だが、アルキル基が第二級アルキル基なら反応効果は通常良好でなく、第三級アルキル基は、イリド(大陆:叶立德,鎓内盐、港臺:偶極體)試薬として調製できない。ホスホニウム塩は安定な化合物であり、通常はエタノール中で再結晶し精製できる。 Wittig試薬(イリド)を調製するには、先ずホスホニウム塩をジエチルエーテルやテトラヒドロフランなどの非プロトン性極性溶媒に懸濁し、(フェニルリチウムやn-ブチルリチウムの様な)強塩基を加えて脱プロトン化する。 ある研究[1]では、芳香族環に活性化基がある場合、酢酸ホスホニウムを合成する出発物質としてベンジルアルコール(フェニルメタノール)を使用すると論述している。 酢酸ホスホニウム中のアセチル基は、その後のウィッティヒ反応に影響を与えない。 利用と製法PH4+イオンを直接含む塩は非常に稀だが、この種のイオンは工業上の用途がある塩化テトラヒドロキシメチルホスホニウムの製造時に必要な反応中間体である[2]:
有機ホスホニウム塩は、実験室で常用される試薬で、 P-H結合を持つ有機ホスホニウム塩はホスフィンのプロトン化によって製造できる。
多くの有機四級ホスホニウムカチオン( PR+
テトラフェニルホスホニウムカチオン( PPh+ 有機ホスホニウム塩ウィッティヒ試薬の調製に用いるアルキルトリフェニルホスホニウムの塩はトリフェニルホスフィンとハロアルカンの反応によって容易に製造できるので[3]、ウィッティヒ反応用のウィッティヒ試薬の調製に広く使用される。 アルキル基がメチル基または障害を受けない第一級アルキル基なら反応効率は高いが、第二級以上のアルキル基ならば反応効果は非常に低く、第三級イリドは形成できない。この種の塩は安定な化合物であるため、エタノールからの再結晶によって精製できる。 ウィッティヒ試薬(イリド)を調製する時は、ホスホニウム塩をエーテルやテトラヒドロフランなどの溶媒に懸濁しフェニルリチウムやn-ブチルリチウムなどの強塩基を加える。 還元反応ホスホニウム塩は穏やかな酸化剤に対して安定ですがナトリウムや水素化アルミニウムリチウムなどの還元剤によって以下の様に還元することができる[4]。
分析化学酢酸ホスホニウムは酢酸(溶媒)中では強塩基なので、酢酸水銀の存在下、メチルバイオレットを指示薬として過塩素酸で滴定でき、滴定の終点は緑色である[4]。
ハロゲン化ホスホニウムホスフィン(R3P)及びハロゲン(X2)の反応でR3PX2型ハロゲン化ホスホニウムを合成できる。化合物のPh3PBr2(高融点固体)は、トリフェニルホスフィンと臭素との反応によって生成し、「臭化ヨードトリフェニルホスホニウム」又は「二臭化トリフェニルホスホニウム」と呼ばれる。二臭化物と二塩化物は共に市販の試薬でアルコールやフェノールのハロゲン化の様なハロゲン化反応に於ける試薬に用いられる [5]。 化合物二塩化トリフェニルホスホニウムPh3PCl2は報告に拠ると、極性溶媒中ではイオン性化合物(PPh3Cl)+Cl−であり、非極性溶媒及び固体中では、三角錐を有する二峰性分子である[6]。 関連項目脚注
|
Portal di Ensiklopedia Dunia