|
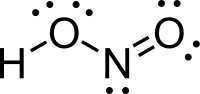
Salétromossav
A salétromossav (HONO vagy HNO2) a nitrogén egyik oxosava, savanhidridje a dinitrogén-trioxid (N2O3). Színtelen, szúrós szagú folyadék, egyértékű, középerős sav. Tiszta állapotban még nem állították elő, de híg vizes oldatban és alacsony hőmérsékleten jól ismert és fontos reagens. Kémiai tulajdonságaiA salétromossav bomlékony vegyület. A bomlás melegítés hatására is végbemegy, de akár homok vagy üvegszilánk is kiválthatja. A bomlás termékei a salétromsav, a víz és a nitrogén-monoxid. A képződő nitrogén-monoxid reakcióba lép a levegő oxigénjével, és vörösbarna színű nitrogén-dioxiddá oxidálódik. A képződő nitrogén-dioxid miatt viselkedhet különösen a töményebb salétromossav oxidálószerként. Köztes oxidációs állapotú vegyület, ezért oxidáló és redukáló hatású is lehet. Enyhe oxidálószer, a jodidiont jóddá oxidálja. A reakciója hidrogén-jodiddal a következő: A kén-hidrogént kénné oxidálja, ammóniával reagálva nitrogénné alakul. Viselkedhet redukálószerként is, ekkor salétromsavvá oxidálódik. A kálium-permanganátot például redukálja. Az aromás aminokat diazóniumsókká alakítja, ezért szerves festékek előállítására használják. SóképzésEgyértékű savként viselkedik. A salétromossav sói a nitritek, ezek NO−2 (nitrit) aniont tartalmaznak, általában vízben oldhatóak. A természetben gyakoriak, legnagyobb jelentősége a tartósítószerként használatos nátrium-nitritnek (NaNO2) van. Vizes oldatuk többnyire lúgos kémhatású, mert a nitrition protont képes felvenni a vízmolekuláktól. A nitritek mérgező hatásúak, mert a vér hemoglobinját methemoglobinná alakítják. ElőállításaA dinitrogén-trioxid vízben oldva salétromossavat ad, de mivel a savanhidrid is igen ritka (már -10 °C felett bomlik), ezért a salétromossav legkönnyebben a sójából (például nátrium-nitritből) szabadítható fel, kénsavval. ElőfordulásaA salétromossav a természetben kis mennyiségben fordul elő, sói viszont nagymértékben megtalálhatóak. FelhasználásaA salétromossavat a szerves vegyiparban alkalmazzák az azofestékek gyártásakor. A reakcióját kálium-permanganáttal az analitikai kémiában használják térfogatos elemzésekre. Források
Hivatkozások
|
||||||||||||||||||||||||||||||||||||
Portal di Ensiklopedia Dunia