|
Foszfor
A foszfor (nyelvújításkori magyar nevén vilany) egy nemfémes, szilárd kémiai elem. A rendszáma 15, vegyjele P. Neve görög eredetű, jelentése „fényhozó”. Az ún. biogén elemek közé tartozik, részt vesz fontos szerves molekulák, például a DNS, RNS felépítésében. FelfedezéseAz elemet először Hennig Brand alkimista állította elő 1669-ben úgy, hogy először napokig vizeletet rothasztott, főzéssel besűrítette, majd a lombikban maradt anyagot vörösizzásig hevítve ledesztillálta, és a keletkező gőzöket víz alatt kondenzáltatta. A keletkező viaszszerű anyag levegőre kerülve sötétben is világított, láng nélkül. A világító anyagot „hideg tűz”-nek nevezte el. A foszfor szó a görög φως (phos = fény) és φορος (phoros = hordozó) szóból származik. A foszfor egyedülálló az elemek között azzal, hogy először fedezték fel állati/emberi testnedvben, majd utána a növény- és az ásványvilágban, valamint az első elem, melynek ismerjük felfedezőjét. Allotrop módosulatai
Gyulladási hőmérsékletek
Kémiai tulajdonságaiA három foszfor kémiailag azonos módon viselkedik. A foszfor égésekor foszfor-pentoxid keletkezik, amely kiváló vízmegkötő anyag, bőrre kerülve égési sebet okoz. A foszfor-pentoxid vízzel való reakciójának egyenlete: Ekkor foszforsav keletkezik. A foszforsav nem mérgező, üdítően savanyú ízű anyag, ezért ízesítésre használják (pl.: kóla). A foszforsav sói a foszfátok, savmaradékionja a foszfátion. Előfordulása
ElőállításaA foszfort kalcium-foszfátból (Ca3(PO4)2) állítják elő. A kalcium-foszfátot kvarchomokkal és szénnel keverik össze, majd a levegőt kizárva hevítik.[5] FelhasználásaA foszfor minden növény és állat számára létfontosságú. A legtöbb bányászott foszfort műtrágyázásra használják, mert a műveletlen termőföldben kis mennyiségben, oldhatatlan sók formájában van jelen, és ez a növények számára feldolgozhatatlan. Növényvédő szerekben is felhasználják. Az élelmiszeripar nagyon sok foszfort használ fel, főleg savanyítóanyagként, foszforsav formájában. Irinyi János a fehérfoszfort a mai biztonsági gyufa elődjéhez használta. A mai biztonsági gyufa dobozának dörzsfelületéhez már a jóval biztonságosabb vörösfoszfort alkalmazzák. Ezen kívül mosószerekbe is kerülnek foszfátok. VegyületeiA foszfor az antimon, bizmut és a nemesgázok kivételével minden elemmel képez biner (két különböző atomból álló) vegyületet. A bizmut, higany és ólom kivételével a többi fémmel közvetlenül is egyesül. Fémmel alkotott biner vegyületei a foszfidok, hidrogénnel alkotott binerje a foszfin (PH3). 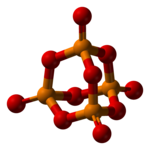 OxidokA tetrafoszfor-dekaoxid, (melyet gyakran foszfor-pentoxidnak neveznek, bár P2O5 összegképletű vegyület nem létezik) az égetett foszfor: A tetrafoszfor-dekaoxid oldásával kapjuk a foszforsavat, amely nem mérgező, savanyú ízű anyag, üdítőket ízesítenek vele. E 338-as adalékanyag. A foszfor másik fontos oxidja a tetrafoszfor-hexaoxid („foszfor-trioxid”, P4O6) a foszforossav anhidridje. Keveset tudunk a foszfor-monoxidról (PO), mely a nitrogén-monoxid analógja, pedig a csillagközi gázfelhőkben ez a legelterjedtebb foszformolekula. További foszfor-oxidok: P4O7, P4O8, P4O9. Ezek gyűrűje a tetrafoszfor-dekaoxidéval azonos, csak kevesebb oxigénatom kapcsolódik a gyűrűhöz. OxosavakA foszfornak számos oxosava ismert, ezek közül messze a legfontosabb az ortofoszforsav (H3PO4), a pirofoszforsav (difoszforsav; H4P2O7) és a trifoszforsav (H5P3O10). A foszforsav különböző sóit és savanyú sóit az élelmiszer- és mosószeriparban, valamint fogkrémekben használják. Megtalálható a csontokban, fogakban kalcium-foszfát alakjában. Az élőlények örökítőanyaga, a DNS nukleinsavak foszforsavval alkotott észtere. A foszforsav a „ragasztóanyag” szerepét játssza a hosszú nukleinsav-láncban. A trifoszforsav adenozinnal alkotott észtere, az ATP a szervezet sejtjeinek energiahordozója. Energialeadáskor a difoszforsav adenozin-észterére, ADP-re bomlik le. SzulfidokA foszfor a kénnel is sokféle vegyületet alkot. Ezek közül iparilag két fontos van:
HalogénvegyületekA foszfor biner halogénvegyületeinek három típusa van:
ahol X = F, Cl, Br vagy I. Mind a 12 vegyület ismert, közülük gyakorlati szempontból legfontosabb a foszfor-triklorid (PCl3). További példák: foszfor-pentabromid, foszfor-pentaklorid, foszfor-trijodid. Ismertek vegyes foszfor-halogenidek is, melyekben kétféle halogénatom is van. Más vegyületekA foszfornak oxigénnel vagy kénnel és halogénnel sokféle vegyülete ismert, pl. POCl3, POF2Cl, PSF3. Az egyszeres P−N-kötést tartalmazó vegyületek a foszfazánok és ciklofoszfazánok, a P=N kettős kötést tartalmazók a foszfazének. Ezek molekulaszerkezetének sok részlete máig ismeretlen és intenzív kutatás tárgya. A C−P-kötés tartalmazó foszfororganikus vegyületek száma és jelentősége óriási. Két példa: foszkarnet, perzinfotel. Jegyzetek
Források
További információk
Kapcsolódó szócikkekA Wikimédia Commons tartalmaz Foszfor témájú médiaállományokat.
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Portal di Ensiklopedia Dunia









