|
HedgehogHedgehog (en français : hérisson), est une protéine. Elle est présente chez les invertébrés (c'est une protéine de polarité segmentaire, impliquée dans le contrôle des patrons de développement embryonnaire). Il y a 3 gènes homologue du gène Hedgehog chez les vertébrés. La voie de signalisation de Hegdehog est complexe et fait intervenir plusieurs autres protéines. Patched et Wingless, notamment, sont aussi nécessaires à la segmentation et à la différenciation et permettent la régulation de l’expression de Hedgehog. Il y a plusieurs homologues du gène hedgehog chez les vertébrés, comme Sonic hedgehog, Indian Hedgehog et Desert Hedgehog, tous aussi importants pour le développement embryonnaire[1]. Plusieurs maladies sont d’ailleurs associées à la mutation du gène. L’expression ectopique du gène est en effet associée chez les vertébrés à des tumeurs au niveau de la peau, des glandes mammaires et du système nerveux[2]. De plus, des conséquences fatales ont été observées chez des fœtus humains dont la voie de hedgehog était déréglée. Par exemple, des défauts de la croissance du cerveau et de plusieurs autres organes. Même à l’état adulte, hedgehog reste important pour la réparation des tissus et le bon renouvellement des cellules[3]. Découverte Le gène de polarité segmentaire Hedgehog fut découvert dans les années 1970 par Christiane Nusslein-Volhard et Eric Wieschaus lors de criblages génétiques de mutations chez la drosophile[3]. Leur article sur les mutants de polarité segmentaire décrivant leur découverte du gène Hedgehog, publié en 1978, leur a valu le Prix Nobel de physiologie ou médecine en 1995[4]. Chez la drosophile sauvage, l’épiderme antérieur possède des denticules. En effet, chaque segment de la mouche à fruit est recouvert de bande de ces petites excroissances cutanées. La partie postérieure de l’animal est toutefois nue. Les recherches de Nusslein-Volhard et Wieschaus montrent que la mutation du gène hedgehog (hh) remplace complètement la partie postérieure nue de la drosophile par des bandes de denticules similaire à celles du côté antérieur. La drosophile mutante étant recouverte de ces "épines", le nom anglais hedgehog (hérisson) fut donné à ce gène[2]. Plus tard, des homologues de hedgehog furent découverts chez les vertébrés. ProtéineChez les invertébrésIl n’y a qu’un seul gène hedgehog (hh) chez la drosophile, le modèle étudié pour le gène hedgehog des invertébrés. Chez elle, ce gène est impliqué principalement dans la prolifération cellulaire et la polarisation des segments de son embryon. Par exemple, il participe à la formation de l'aile de la mouche[3]. La protéine hedgehog est composée de deux domaines ; le premier est le domaine terminaison amine ou HhN, se terminant par un acide aminé composé d’un amine libre NH2. Celui-ci agit en tant que molécule de signalisation. Ensuite, il y a le domaine de terminaison carboxyle, ou HhC, un acide aminé portant un groupe carboxyle COOH. Ce domaine est de grande importance, puisqu’il a un effet auto-catalytique permettant à hedgehog de se scinder lui-même en ses deux domaines. Par la suite, un cholestérol peut être ajouté au domaine scindé HhN à son extrémité carboxyle et un acide palmitique à son extrémité amine. Ce n’est que le domaine HhN coupé et modifié qui peut être sécrété par la cellule[5]. DrosophileChez la drosophile (mouche à fruit ou mouche à vinaigre), ce gène est impliqué dans la détermination des patrons des segments, des yeux et des membres chez l’embryon et influence donc la différenciation de plusieurs tissus durant le développement[6],[7]. La protéine agit notamment comme un morphogène, c’est-à-dire qu’on observe un gradient du gène selon les régions de l’embryon. En effet, des concentrations différentes de Hedgehog mènent à des cellules différentes à des endroits différents de l’embryon[8]. Chez les vertébrés Il y a trois homologues hedgehog majeurs chez les vertébrés. La protéine Sonic Hedgehog (Shh) est la plus étudiée, car son expression se répartit dans tout l’organisme, contrairement aux protéines Indian Hedgehog et Desert Hedgehog, qui sont plus localisées dans l'animal et agissent plus après la naissance. En effet, alors que Desert hedgehog est exprimé dans les cellules des testicules, Indian hedgehog se situe plutôt dans le tube digestif et le cartilage[9]. Ce gène participe à la segmentation dorso-ventrale du tube neural, à l'asymétrie gauche-droite et la différenciation antéro-postérieure des membres de l'animal[10]. Particulièrement, Sonic Hedgehog est de grande importance pour l'organisation du système nerveux. Dans l’embryon, la protéine Shh est sécrétée majoritairement dans la notochorde et la plaque neurale de l’embryon et différencie les neurones. La concentration de Shh diminue donc en s’éloignant de la notochorde[3]. Lors de la formation du tube neural, le précurseur du système nerveux ventral de l'embryon, la protéine diffuse selon un gradient de concentration de la notochorde vers le plancher de la plaque neurale pour créer les différents types de neurones[11]. Shh est aussi exprimé dans les bourgeons des membres des mammifères et est donc très important pour la formation des membres et des doigts[5],[9]. Voie de signalisationRégulation de Hedgehog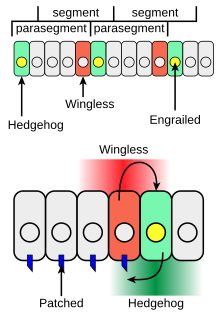 L’expression de hedgehog est tout d’abord activée par un facteur de transcription : Engrailed. Les cellules exprimant Engrailed sécrètent Hedgehog et régulent donc son expression en inhibant un répresseur de Hedgehog. De plus, une autre protéine, nommée Wingless, permet de maintenir l’expression de Hedgehog. Wingless et Hedgehog sont produits dans des bandes cellulaires adjacentes de l’embryon et forment une boucle de rétroaction positive, où chaque protéine régule l’expression de l’autre. En effet, lorsque Hedgehog se lie à son récepteur Patched, il stimule l’expression de Wingless. À leur tour, les cellules sécrétant Wingless maintiennent l’expression de Engrailed et de Hedgehog[8],[11],[13]. Hedgehog subit de nombreuses modifications à la suite de la traduction pour aider à sa bonne expression. Comme mentionné précédemment, à l’extrémité carboxyl de la protéine, il se forme un lien covalent avec une molécule de cholestérol, ce qui permet au domaine de HhN de se fragmenter et d'être libérée. De plus, du côté amino-terminal de la protéine, un acide palmitique est attaché. D'ailleurs, pour être sécrétée par une cellule, le domaine HhN nécessite une autre protéine transmembranaire, nommée Dispatched, agissant comme transporteur et reconnaissant les stérols présents sur le domaine de hedgehog[14]. Le cholestérol est donc de grande importance pour la voie hedgehog, car il intervient en deux points cruciaux. Premièrement, il permet à la protéine de diffuser à partir d’où il se trouve, car il est plus fluide dans la membrane. Malgré le fait qu’on ne comprend pas encore totalement comment se produit la diffusion de hedgehog dans les différentes parties de l’animal, on sait que les stérols sont de grande importance pour cet aspect. De plus, il est nécessaire au fonctionnement de Patched, le récepteur de hedgehog, puisqu'il reconnait aussi les stérols associés à hh et permet leur liaison[15],[10]. Mécanismes de la voie Hedgehog chez les invertébrésLa voie de signalisation hedgehog est une voie importante dans le développement des invertébrés. Impliquée dans l’embryogenèse et la morphogenèse, elle joue un rôle majeur dans l’orientation des cellules souches et leur différenciation. En l’absence de hedgehog, une protéine transmembranaire nommée Patched empêche l’activité d’un récepteur : Smoothened. D'autres protéines sont impliquées pour former un grand complexe composé de la protéine costal-2, de la kinase sérine-thréonine fused (fu), du répresseur de fused (su(fu)) et du facteur de transcription Cubitus interruptus (Ci). Le récepteur Patched est lui-même lié au facteur Ci du complexe[8],[3],[16]. Dans les conditions où hedgehog est absent, Patched reste lié à Smoothened et Ci est clivée en une forme répressive Ci-R. Ce fragment migre alors dans le noyau pour agir comme inhibiteur de la transcription. Toutefois, lorsque hedgehog est présent, il agit comme un ligand et s’attache au récepteur Patched. Ceci permet de lever l’inhibition qu’exerçait Patched sur Smoothened. Smoothened est alors phosphorylé (ajout d'un groupe phosphate) par des kinases et change de conformation, entraînant son accumulation dans la membrane. Cela a pour effet de libérer Ci du complexe, qui n’est alors pas clivée et peut donc entrer de manière intacte dans le noyau, où elle agit comme un activateur de la transcription[16]. Mécanismes de la voie Hedgehog chez les vertébrés Chez les vertébrés, la voie de signalisation de hedgehog est, quoique similaire, plus complexe que chez les invertébrés. En effet, les protéines de cette voie sont homologues à celles des invertébrés et diffèrent selon l’espèce. La différence majeure est l'utilité de cils primaires, des organelles absentes chez la drosophile mais présentes dans toutes les cellules des vertébrés. Chez les mammifères par exemple, lorsque hedgehog se lie à son récepteur Patched, Smoothened est libéré mais cette fois-ci, il migre dans l’axonème du cil, c'est-à-dire la partie centrale du cil[15]. De plus, deux récepteurs protéiques sont associées à Shh, soit Patched 1 et Patched 2, similaires à Patched chez les invertébrés. Lorsque Sonic hedgehog est présent dans les cellules, il se lie au récepteur Patched 1, ce qui inhibe la répression de Smoothened sur la transcription. Ce dernier peut donc migrer au niveau de la membrane plasmique et activer des facteurs de transcription appelés GLI (GLI1, GLI2 ET GLI3). Ceux-ci entrent dans le noyau de la cellule et régulent l’activité des gènes cibles. Le fonctionnement des protéines GLI est peu compris. Toutefois, ceux-ci semblent être homologues au facteur de transcription Ci vu précédemment dans la voie de hedgehog des invertébrés. En effet, tout comme Ci, certains facteurs GLI sont activateurs de la transcription et d’autres sont répresseurs[17],[3]. Pathologies associées Plusieurs pathologies sont associées à la mutation du gène hedgehog chez les animaux, notamment des anomalies des membres et des syndromes polymalformatifs. En effet, des mutations qui contribuent à une répression du signal de hedgehog peuvent être responsables de malformations allant du bec de lièvre ou de la cyclopie, jusqu’à de sévères malformations du cerveau. On observe par exemple des cas d’holoprosencéphalie, causant la mort de l’embryon[3],[9]. Une mutation d'un des gènes GLI (facteur de transcription de la voie de Sonic hedgehog) peut aussi être fatale puisque son bon fonctionnement est nécessaire à l'activation de hedgehog. On compte entre autres le syndrome de Greig, se caractérisant par une fusion des doigts, un périmètre crânien plus large, une distance inter-orbitale importante. Le syndrome Pallister-Hall, plus fatal encore, cause une malformation de l'hypothalamus, de l'hypophyse et des reins et donc la mort avant la naissance [9]. Sachant que hedgehog participe à la prolifération cellulaire, il est normal qu'une sur-expression des composants de sa voie de signalisation puisse conduire à des tumeurs. En effet, hedgehog est la voie la plus impliquée dans les cancers. Sa dérégulation peut conduire à la croissance ectopique ou à la prolifération non contrôlée des cellules et mener à l’apparition de cancers dans plusieurs tissus. Chez l'humain, cette voie participe d'ailleurs de façon importante à la régulation de la cancérogenèse dans plusieurs aspects. En effet, on remarque un accroissement de la division cellulaire et une diminution de l’adhérence cellulaire et de l’apoptose. Les mutations possibles de hedgehog ont donc un impact très important sur les mécanismes de la prolifération cellulaire et peuvent mener à de nombreuses formes de cancers[16]. De plus, il faut noter que, chez l’adulte, la voie de signalisation Shh est aussi assez importante puisqu'elle peut contribuer au maintien et au contrôle des tissus sains de l'individu. Des recherches ont en effet montré que cette voie permet le renouvellement de plusieurs cellules souches, comme celles de la moelle osseuse et de l’intestin, et est aussi responsable de la vascularisation des tissus[3]. Il est donc certain que la connaissance de la voie hedgehog est importante pour connaître les impacts que peuvent avoir une mutation de cette voie sur l'animal, embryon comme adulte, et que les recherches devront avancer sur le sujet pour pouvoir mieux comprendre ces pathologies. Notes et références
Voir aussi |