Formamide
Identification
Nom UICPA
Formamide
Synonymes
méthanamide
No CAS
75-12-7
No ECHA
100.000.766
No CE
200-842-0
SMILES
InChI
InChI : vue 3D InChI=1/CH3NO/c2-1-3/h1H,(H2,2,3)/f/h2H2
Apparence
liquide incolore, hygroscopique, visqueux[ 1]
Propriétés chimiques
Formule
C H 3 N O [Isomères]
Masse molaire [ 4] 45,040 6 ± 0,001 5 g /mol C 26,67 %, H 6,71 %, N 31,1 %, O 35,52 %,
pK a
0,3
Moment dipolaire
3,73 ± 0,07 D [ 2]
Diamètre moléculaire
0,431 nm [ 3]
Propriétés physiques
T° fusion2,5 °C [ 1]
T° ébullition(décomposition) : 210 °C [ 1]
Solubilité
dans l'eau : très bonne[ 1] bonne dans l'éthanol
Paramètre de solubilité δ
39,3 MPa 1/2 25 °C )[ 5] 17,9 cal 1/2 ·cm -3/2 [ 6]
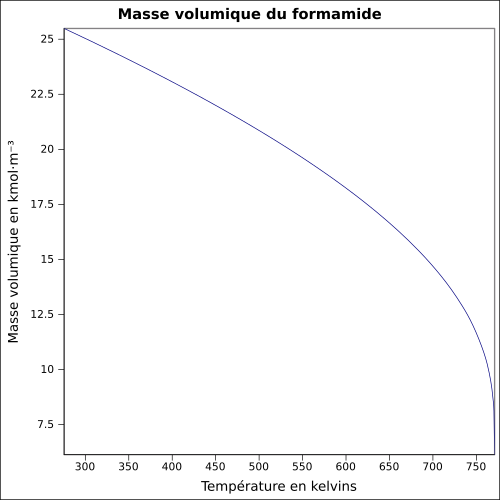
Masse volumique
1,133 4 g ·cm -3 [ 7] équation[ 8]
ρ
=
1.2486
/
0.20352
(
1
+
(
1
−
T
/
771
)
0.25178
)
{\displaystyle \rho =1.2486/0.20352^{(1+(1-T/771)^{0.25178})}}
-3 et température en kelvins, de 275,60 à 771 K.-3 à 25 °C.
T (K)
T (°C)
ρ (kmol·m-3 )
ρ (g·cm-3 ) 275,60
2,45
25,488
1,14801 308,63
35,48
24,87088
1,12021 325,14
51,99
24,5556
1,10601 341,65
68,5
24,23562
1,0916 358,17
85,02
23,91064
1,07696 374,68
101,53
23,58035
1,06208 391,19
118,04
23,24438
1,04695 407,71
134,56
22,90232
1,03154 424,22
151,07
22,55371
1,01584 440,73
167,58
22,19805
0,99982 457,25
184,1
21,83476
0,98346 473,76
200,61
21,46318
0,96672 490,27
217,12
21,08254
0,94958 506,79
233,64
20,69197
0,93199 523,3
250,15
20,29045
0,9139
T (K)
T (°C)
ρ (kmol·m-3 )
ρ (g·cm-3 ) 539,81
266,66
19,87677
0,89527 556,33
283,18
19,44949
0,87602 572,84
299,69
19,00688
0,85609 589,35
316,2
18,5468
0,83537 605,87
332,72
18,06661
0,81374 622,38
349,23
17,56294
0,79105 638,89
365,74
17,03139
0,76711 655,41
382,26
16,46605
0,74165 671,92
398,77
15,85867
0,71429 688,43
415,28
15,19711
0,68449 704,95
431,8
14,46233
0,6514 721,46
448,31
13,62124
0,61351 737,97
464,82
12,60662
0,56781 754,49
481,34
11,23335
0,50596 771
497,85
6,135
0,27633
T° d'auto-inflammation>500 °C [ 1]
Point d’éclair
154 °C (coupelle ouverte)[ 1]
Pression de vapeur saturante
à 20 °C : environ 2 Pa [ 1] équation[ 8]
P
v
s
=
e
x
p
(
100.3
+
−
10763
T
+
(
−
10.946
)
×
l
n
(
T
)
+
(
3.8503
E
−
6
)
×
T
2
)
{\displaystyle P_{vs}=exp(100.3+{\frac {-10763}{T}}+(-10.946)\times ln(T)+(3.8503E-6)\times T^{2})}
T (K)
T (°C)
P (Pa) 275,6
2,45
1,0350 308,63
35,48
21,09 325,14
51,99
72,96 341,65
68,5
219,2 358,17
85,02
584,21 374,68
101,53
1 405,14 391,19
118,04
3 093,59 407,71
134,56
6 308,64 424,22
151,07
12 035,07 440,73
167,58
21 659,04 457,25
184,1
37 033,99 473,76
200,61
60 530,86 490,27
217,12
95 069,44 506,79
233,64
144 130,61 523,3
250,15
211 751,68
T (K)
T (°C)
P (Pa) 539,81
266,66
302 508,99 556,33
283,18
421 493,41 572,84
299,69
574 284,12 589,35
316,2
766 926,56 605,87
332,72
1 005 919,14 622,38
349,23
1 298 212,88 638,89
365,74
1 651 226,84 655,41
382,26
2 072 881,66 671,92
398,77
2 571 652,66 688,43
415,28
3 156 643,62 704,95
431,8
3 837 681,99 721,46
448,31
4 625 436,29 737,97
464,82
5 531 556,71 754,49
481,34
6 568 840,13 771
497,85
7 751 400
Thermochimie
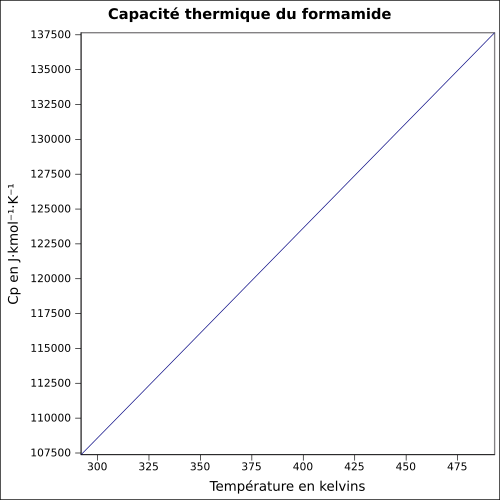
Cp
équation[ 8]
C
P
=
(
6.3400
E
4
)
+
(
150.60
)
×
T
{\displaystyle C_{P}=(6.3400E4)+(150.60)\times T}
-1 ·K-1 et température en kelvins, de 292 à 493 K.-1 ·K-1 à 25 °C.
T
T
Cp
(
J
k
m
o
l
×
K
)
{\displaystyle ({\tfrac {J}{kmol\times K}})}
Cp
(
J
k
g
×
K
)
{\displaystyle ({\tfrac {J}{kg\times K}})}
292
18,85
107 380
2 384 305
31,85
109 333
2 427 312
38,85
110 387
2 451 318
44,85
111 291
2 471 325
51,85
112 345
2 494 332
58,85
113 399
2 518 338
64,85
114 303
2 538 345
71,85
115 357
2 561 352
78,85
116 411
2 585 359
85,85
117 465
2 608 365
91,85
118 369
2 628 372
98,85
119 423
2 651 379
105,85
120 477
2 675 385
111,85
121 381
2 695 392
118,85
122 435
2 718
T
T
Cp
(
J
k
m
o
l
×
K
)
{\displaystyle ({\tfrac {J}{kmol\times K}})}
Cp
(
J
k
g
×
K
)
{\displaystyle ({\tfrac {J}{kg\times K}})}
399
125,85
123 489
2 742 405
131,85
124 393
2 762 412
138,85
125 447
2 785 419
145,85
126 501
2 809 426
152,85
127 556
2 832 432
158,85
128 459
2 852 439
165,85
129 513
2 875 446
172,85
130 568
2 899 452
178,85
131 471
2 919 459
185,85
132 525
2 942 466
192,85
133 580
2 966 472
198,85
134 483
2 986 479
205,85
135 537
3 009 486
212,85
136 592
3 033 493
219,85
137 650
3 056
équation[ 9]
C
P
=
(
30.911
)
+
(
1.4363
E
−
2
)
×
T
+
(
1.9281
E
−
4
)
×
T
2
+
(
−
1.9805
E
−
7
)
×
T
3
+
(
5.8262
E
−
11
)
×
T
4
{\displaystyle C_{P}=(30.911)+(1.4363E-2)\times T+(1.9281E-4)\times T^{2}+(-1.9805E-7)\times T^{3}+(5.8262E-11)\times T^{4}}
-1 ·K-1 et température en kelvins, de 150 à 1 500 K.-1 ·K-1 à 25 °C.
T
T
Cp
(
J
k
m
o
l
×
K
)
{\displaystyle ({\tfrac {J}{kmol\times K}})}
Cp
(
J
k
g
×
K
)
{\displaystyle ({\tfrac {J}{kg\times K}})}
150
−123,15
36 765
816 240
−33,15
42 919
953 285
11,85
46 465
1 032 330
56,85
50 221
1 115 375
101,85
54 119
1 202 420
146,85
58 095
1 290 465
191,85
62 091
1 379 510
236,85
66 056
1 467 555
281,85
69 943
1 553 600
326,85
73 712
1 637 645
371,85
77 329
1 717 690
416,85
80 763
1 793 735
461,85
83 993
1 865 780
506,85
87 000
1 932 825
551,85
89 774
1 993
T
T
Cp
(
J
k
m
o
l
×
K
)
{\displaystyle ({\tfrac {J}{kmol\times K}})}
Cp
(
J
k
g
×
K
)
{\displaystyle ({\tfrac {J}{kg\times K}})}
870
596,85
92 306
2 049 915
641,85
94 599
2 100 960
686,85
96 656
2 146 1 005
731,85
98 489
2 187 1 050
776,85
100 115
2 223 1 095
821,85
101 557
2 255 1 140
866,85
102 843
2 283 1 185
911,85
104 007
2 309 1 230
956,85
105 089
2 333 1 275
1 001,85
106 134
2 356 1 320
1 046,85
107 195
2 380 1 365
1 091,85
108 327
2 405 1 410
1 136,85
109 593
2 433 1 455
1 181,85
111 063
2 466 1 500
1 226,85
112 811
2 505
Propriétés électroniques
1re énergie d'ionisation
10,16 ± 0,06 eV [ 10]
Propriétés optiques
Indice de réfraction
n
D
25
{\displaystyle {\textit {n}}_{D}^{25}}
[ 3]
Précautions
NFPA 704
Directive 67/548/EEC
T
Numéro index :
616-052-00-8 Symboles :
T :
Toxique Phrases R :
R61 : Risque pendant la grossesse d’effets néfastes pour l’enfant.
Phrases S :
S45 : En cas d’accident ou de malaise, consulter immédiatement un médecin (si possible, lui montrer l’étiquette).
S53 : Éviter l’exposition - se procurer des instructions spéciales avant l’utilisation.
Unités du SI et CNTP
modifier
Le formamide est un amide provenant de l'acide formique . À température ambiante, il se présente comme un liquide incolore et légèrement visqueux, proche de la consistance de la glycérine . C'est un solvant hygroscopique et un réducteur d'odeur proche de celle de l'ammoniac . Il peut se transformer en acide cyanhydrique s'il est soumis à des températures supérieures à 90 °C .
À des températures supérieures à 200 °C , le formamide se transforme en acide cyanhydrique , ammoniac , monoxyde de carbone et eau. Le formamide pourrait jouer un rôle clé dans la formation des molécules complexes à l'origine du vivant[ 11]
densité de vapeur : 1,55 (air = 1)pression de vaporisation : 0,08 mmHg 11 Pa 20 °C
point éclair : 154 °C
pKa : 23,5
se décompose à partir de 180 °C pour donner de l'eau, de l'ammoniac, du monoxyde de carbone et du cyanure d'hydrogène
Production
La réaction entre l'acide formique et l'ammoniac produit du formiate d'ammonium, lequel peut conduire sous l'action de la chaleur au formamide :
HCOOH + NH3 → HCOONH4 HCOONH4 → HCONH2 + H2 O
Utilisations
Le formamide est utilisé dans les applications suivantes[ 12]
Fabrication de l'acide formique, de l'acide cyanhydrique ou de dérivés de triazines ;
Agent de filage (copolymères de l'acrylonitrile), solvant , durcisseur et plastifiant dans la fabrication de matières plastiques
Colles ;Solvant dans les encres, peintures et vernis ou la fabrication de cuirs synthétiques ;
Émulsifiant, inhibiteur de corrosion , additif pour huiles lubrifiantes et fluides hydrauliques,
Solvant d'extraction ;
Produits pharmaceutiques et produits fongicides et pesticides ;
Synthèse de vitamines ;
Réactif analytique de laboratoire : déstabilisation des acides nucléiques (rupture des liaisons hydrogène entre les bases) ;
Tampon favorisant la séparation et l'ionisation de composés apolaires dans les techniques séparatives analytiques, par exemple : chromatographie en phase liquide couplée à la spectrométrie de Masse en Tandem (HPLC - ESI -MS/MS).
Synthèse du 3,4-méthylènedioxyamphétamine (MDA) (psychotrope);
Voir aussi
Liens externes
↑ a b c d e f et g FORMAMIDE , Fiches internationales de sécurité chimique ↑ (en) David R. Lide, Handbook of chemistry and physics , Boca Raton, CRC, 16 juin 2008 , 89e éd. , 2736 p. (ISBN 978-1-4200-6679-1 1-4200-6679-X , p. 9-50 ↑ a et b (en) Yitzhak Marcus, The Properties of Solvents , vol. 4, England, John Wiley & Sons Ltd, 1999 , 239 p. (ISBN 0-471-98369-1 ↑ Masse molaire calculée d’après « Atomic weights of the elements 2007 www.chem.qmul.ac.uk .
↑ (en) James E. Mark, Physical Properties of Polymer Handbook , Springer, 2007 , 2e éd. , 1076 p. (ISBN 978-0-387-69002-5 0-387-69002-6 lire en ligne ) , p. 294↑ (en) Șerban Moldoveanu, Sample preparation in chromatography , Amsterdam/Boston, Elsevier, 2002 , 930 p. (ISBN 0-444-50394-3 , p. 258↑ (en) J. G. Speight, Norbert Adolph Lange, Lange's handbook of chemistry , McGraw-Hill, 2005 , 16e éd. , 1623 p. (ISBN 0-07-143220-5 , p. 2.289↑ a b et c (en) Robert H. Perry et Donald W. Green , Perry's Chemical Engineers' Handbook , USA, McGraw-Hill, 1997 , 7e éd. , 2400 p. (ISBN 0-07-049841-5 , p. 2-50 ↑ (en) Carl L. Yaws, Handbook of Thermodynamic Diagrams , vol. 1, 2 et 3, Huston, Texas, Gulf Pub. Co., 1996 (ISBN 0-88415-857-8 0-88415-858-6 0-88415-859-4 ↑ (en) David R. Lide, Handbook of chemistry and physics , Boca Raton, CRC, 2008 , 89e éd. , 2736 p. (ISBN 978-1-4200-6679-1 , p. 10-205 ↑ L'origine de la vie simulée sur ordinateur , sur {SCIENCES²}. Consulté le 22 septembre 2014.↑ « Formamide - Fiche toxicologique n°285 [PDF] , sur inrs.fr 2012