|
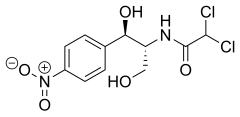
Chloramphénicol
Le chloramphénicol est un antibiotique bactériostatique de la famille des phénicolés. Cet antibiotique peut être utilisé pour traiter la méningite, la peste, le choléra, la fièvre typhoïde uniquement lorsque les antibiotiques plus sûrs ne peuvent pas être employés. Lors du traitement, il est recommandé de contrôler tous les deux jours la composition sanguine. Le chloramphénicol est isolé en 1947 à partir de Streptomyces venezuelae (en). Cet antibiotique fait partie de la liste des médicaments essentiels de l'Organisation mondiale de la santé. Il agit en inhibant la synthèse peptidique en se fixant sur le ribosome bactérien. La molécule est disponible par voie intraveineuse, par voie orale et comme une pommade ophtalmique. Elle présente cependant une toxicité importante qui peut entraîner dans certains cas une aplasie médullaire et n'est pratiquement plus utilisée que par voie locale en médecine humaine du fait de sa toxicité potentielle. Usage médicalLe chloramphénicol est un antibiotique de la famille des phénicolés, c'est le seul antibiotique à disposer d'un groupement nitro. Il a été prescrit d'abord dans le traitement de la fièvre typhoïde, mais l'émergence de souches Salmonella typhi multirésistantes a limité son utilisation. Il est utilisé dans le traitement de cette maladie uniquement si la souche est sensible. Le chloramphénicol est utilisé comme agent de seconde ligne dans le traitement du choléra lorsque la souche Vibrio cholerae résiste à la tétracycline. Le chloramphénicol est une molécule qui franchit plus efficacement la barrière hémato-encéphalique que les céphalosporines. Il est le traitement de premier choix en cas d'abcès cérébral par staphylocoques ou par organismes mixtes ou inconnus. Cet antibiotique est actif contre les trois principales souches responsables de la méningite bactérienne : Neisseria meningitidis, Streptococcus pneumoniae et Haemophilus influenzae[4]. De ce fait, dans les pays occidentaux, le chloramphénicol reste le médicament de choix dans le traitement de la méningite pour les patients atteints présentant une allergie sévère à la pénicilline ou aux céphalosporines. Il est recommandé aux médecins généralistes de disposer de chloramphénicol par voie intraveineuse dans leur sac. Le chloramphénicol est utilisé aux États-Unis dans le traitement empirique initial des enfants atteints de fièvre et d'éruption pétéchiale lorsque le diagnostic différentiel inclut à la fois une septicémie due à Neisseria meningitidis et la fièvre des montagnes Rocheuses, en attendant les résultats des analyses. L'antibiotique est également efficace contre Enterococcus faecium, il peut donc être utilisé dans le traitement d'entérocoques résistant à la vancomycine. Sensibilité de souches bactériennes
Neisseria gonorrhoeae, Neisseria meningitidis, Haemophilus influenzae, salmonelles (en particulier Salmonella enterica sérotype Typhi), shigelles, mais ces dernières sont bien moins sensibles aux phénicolés qu'aux céphalosporines (C3G) ou aux fluoroquinolones. Actifs sur les anaérobies, et sur des bactéries intra-cellulaires dont les rickettsioses. Actuellement, certains Enterococcus faecium et certaines souches de Pseudomonas aeruginosa sont résistantes au chloramphénicol. Des Veillonella spp. et des souches de Staphylococcus capitis ont également développé une résistance au chloramphénicol à des degrés variables. Fiche technique
Précautions de sécurité
Effets secondaires et contre-indicationsAnémie aplasiqueLe traitement au chloramphénicol présente des effets secondaires dont le plus grave est l'anémie aplasique, maladie irréversible et mortelle, mais d'incidence faible (environ 0,1 % des cas). Elle se déclare plusieurs semaines à plusieurs mois après l'arrêt du traitement et pourrait être associée à une prédisposition génétique. Afin de prévenir le développement de la maladie, une numération globulaire du sang doit être réalisée chez les patients. La maladie a une incidence de 1 pour 24 000 à 40 000 patients pour le chloramphénicol ingéré par voie orale[5] et tombe à 1 pour 224 716 patients pour le chloramphénicol appliqué sous forme de gouttes oculaires[6]. Pour cette raison, il n'est plus utilisé qu'en application externe dans les pays occidentaux (collyres dans les infections ophtalmiques) ou parfois dans le cas d'infections sévères et résistantes en milieu hospitalier. L'organisation mondiale de la santé (OMS) le conserve sur sa liste des médicaments autorisés considérant que malgré ce risque, il peut apporter un bénéfice important. Autres effetsLe chloramphénicol a un effet toxique direct sur les mitochondries humaines[7] et peut provoquer des dysfonctionnements de la moelle osseuse au cours du traitement. Cet effet se manifeste d'abord par une chute du taux d'hémoglobine lorsque le patient reçoit une dose cumulative de 20 g. L'anémie est entièrement réversible une fois que le médicament est arrêté et ne prédit pas le développement futur de l'anémie aplasique. Des études chez les souris ont suggéré que les dommages de la moelle osseuse résultant des effets toxiques du chloramphénicol sont aggravés si la moelle osseuse est initialement endommagée[8]. Chez l'enfant, le risque de leucémie est augmenté avec la durée du traitement[9]. L'utilisation de chloramphénicol intraveineux est associée au syndrome du bébé gris (en)[10]. Les nourrissons ne disposant pas encore des enzymes hépatiques entièrement fonctionnelles (comme l'UDP-glucuronyl transférase) ne métabolisent pas le chloramphénicol qui reste dans le corps. Cette présence provoque plusieurs effets indésirables dont l'hypotension et la cyanose. Ce syndrome peut être limité en utilisant le médicament aux doses recommandées et en surveillant les taux sanguins[11],[12],[13]. Mode d'actionMécanisme standardLe chloramphénicol est un antibiotique bactériostatique qui limite la synthèse des protéines en inhibant l'activité peptidyltransférase du ribosome bactérien. L'antibiotique se lie spécifiquement aux résidus A2451 et A2452 de l'ARNr 23S[14] de la sous-unité 50S du ribosome bactérien et empêche la formation de la liaison peptidique. Le chloramphénicol et les macrolides ont les mêmes effets d'inhibition de la synthèse de peptides, le chloramphénicol interagit directement sur le ribosome alors que les macrolides bloquent stériquement la progression de la croissance peptidique[15],[16],[17]. Mécanisme de résistanceIl existe trois mécanismes de résistance au chloramphénicol[18] : une réduction de la perméabilité membranaire de l'antibiotique, une mutation sur la sous-unité 50S du ribosome bactérien et la présence d'une enzyme appelée chloramphénicol acétyltransférase. Le mécanisme le plus commun pour des résistances de faible intensité au chloramphénicol est une baisse de la perméabilité membranaire à l'antibiotique. La mutation de la sous-unité 50S est extrêmement rare. La résistance la plus forte à l'antibiotique provient de la présence du gène cat qui code une enzyme appelée chloramphénicol acétyltransférase qui dérive de la S-acétyl-coenzyme A. Cette enzyme permet d'acétyler un ou deux groupements hydroxyle du chloramphénicol et ainsi d’empêcher sa fixation sur le ribosome. Le gène cat codant la résistance au chloramphénicol peut être trouvé sur des plasmides portant des résistances à d'autres molécules. Ainsi, le plasmide Accot (Ampicilline, Chloramphénicol, cotrimoxazole, tétracycline) est un plasmide qui régule la résistance multidrogues chez le Bacille d'Eberth, responsable de la fièvre typhoïde[19]. PharmacocinétiqueLe chloramphénicol est une molécule fortement soluble dans les lipides ; c'est une molécule de faible poids moléculaire et qui se lie peu aux protéines. Elle pénètre efficacement dans tous les tissus du corps, y compris le cerveau mais sa distribution est non uniforme. Les concentrations de chloramphénicol les plus élevées sont trouvées dans le foie et les reins, les plus faibles concentrations étant trouvées dans le cerveau et le liquide céphalorachidien avec une concentration d'environ 30 à 50 % de la concentration moyenne du corps. Lorsque les méninges sont enflammées, la concentration de chloramphénicol dans les méninges correspond à 89 % de la concentration moyenne. Le chloramphénicol est métabolisé par le foie en une molécule inactive, le chloramphénicol glucuronate. En cas d'insuffisance hépatique, la dose de chloramphénicol doit être ajustée en fonction des concentrations plasmatiques mesurées. Le chloramphénicol est un inhibiteur très efficace des isoformes CYP2C19 et CYP3A4 du cytochrome P450 dans le foie[20]. L'inhibition de l'isoforme CYP2C19 entraîne une diminution du métabolisme et donc une augmentation de la concentration d'antidépresseurs, d'antiépileptiques, d'inhibiteurs de la pompe à protons et d'anticoagulants si ces molécules sont administrées en association avec l'antibiotique. L'inhibition de l'isoforme CYP3A4 entraîne une augmentation de la concentration des inhibiteurs calciques, des immunosuppresseurs, des médicaments chimiothérapeutiques, des benzodiazépines, des antifongiques azolés, des antidépresseurs tricycliques, des antibiotiques macrolides, des ISRS, des statines, des antiarythmiques cardiaques, des antiviraux, des anticoagulants et des inhibiteurs de la PDE5. Le chloramphénicol est un antagoniste de la plupart des céphalosporines, l'utilisation associée de ces deux molécules doit être évitée dans le traitement des infections. DécouverteLe chloramphénicol est isolé en 1947 à partir de culture Streptomyces venezuelae (en) par John Ehrlich[21]. Il est synthétisé pour la première fois par la chimiste Mildred Rebstock à partir de produits chimiques facilement disponibles en [22]. Il devient le premier antibiotique synthétisé industriellement à grande échelle. Les derniers produits (topiques) disponibles ont été retirés du marché français en 2008[23]. Autres usagesLe chloramphénicol est également utilisé en médecine vétérinaire, son emploi est cependant très limité. Il est actuellement considéré comme le traitement le plus efficace de chlamydioses chez les koalas[24],[25]. Des études tendent à démontrer que l'antibiotique pourrait être employé dans le traitement de la chytridiomycose des amphibiens. Il est utilisé en association avec la gentamicine dans des milieux de culture en mycologie pour empêcher la croissance des bactéries et favoriser ainsi celle des champignons. Il est utilisé notamment en Chine et en Argentine dans les ruches pour augmenter la ponte des reines et donc la production de miel[26]. DiversLe chloramphénicol fait partie de la liste des médicaments essentiels de l'Organisation mondiale de la santé (liste mise à jour en )[27]. Notes et références
Voir aussiArticles connexesLiens externes
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Portal di Ensiklopedia Dunia