|
Electrodo estándar de hidrógeno Un electrodo estándar de hidrógeno también llamado electrodo normal de hidrógeno es un electrodo redox que forma la base de la tabla estándar de potenciales de electrodos. Su potencial absoluto se estima en 4.40 ± 0.02 V a 25 °C, pero para realizar una base de comparación con cualquier otra reacción electrolítica, el potencial electrolítico del hidrógeno se fija como 0 en todas las temperaturas.[1] Los potenciales de cualquier otro electrodo se compara con el estándar a la misma temperatura. El electrodo de hidrógeno se basa en la semicelda redox: Esta reacción de oxidación-reducción ocurre en un electrodo de platino. El electrodo es sumergido en una solución ácida y se bombea hidrógeno gasesoso a través de él. La concentración de formas oxidadas y reducidas se mantiene como una unidad. Esto implica que la presión de hidrógeno gaseoso es igual a 1 bar y la concentración de hidrógeno en la solución es 1 mol/L. La ecuación de Nernst debe desarrollarse así: o donde:
Razones a favor del uso del platinoEl uso de platino para el electrodo de hidrógeno se debe a varios factores:
La superficie del platino se platiniza, es decir, se cubre con una capa de negro de platino por lo que se requiere:
Sin embargo, otros metales pueden utilizarse para construir electrodos de utilidad similar, por ejemplo paladio.
InterferenciaA causa de la alta actividad de absorción del electrodo platinizado es muy importante proteger la superficie del mismo y la solución contra la presencia de sustancias orgánicas o de oxígeno de la atmósfera. Los iones inorgánicos que pueden reducir a un estado de valencia más baja también deben ser evitados (por ejemplo Fe3+, CrO42-). Los cationes que pueden reducir un depósito sobre el platino también pueden ser fuente de interferencia: plata, mercurio, cobre, plomo, cadmio y talio. Las sustancias que pueden desactivar la catálisis incluyen al arsénico, sulfitos y otros compuestos de azufre, sustancias coloidales, alcaloides, y material biológico en general.[3] Construcción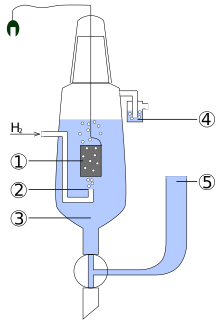 Esquema de un electrodo estándar de hidrógeno:
Véase tambiénReferencias
|
Portal di Ensiklopedia Dunia









