|
Ácido bromhídrico
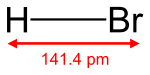
El ácido bromhídrico es la disolución acuosa del bromuro de hidrógeno (HBr). Tiene propiedades de ácido fuerte; reacciona violentamente con bases y es muy corrosivo; altamente irritante para los ojos y para la piel.[2] Tiene un PKa igual a -9, lo que lo hace un ácido más fuerte que el ácido clorhídrico y menos fuerte que el yoduro de hidrógeno. Es uno de los ácidos minerales más fuertes conocidos, y también tiene propiedades oxido-reductoras, reaccionando violentamente con oxidantes fuertes—como nitratos o cloratos— y muchos compuestos orgánicos de forma violenta, con riesgo de incendio y explosión. Ataca a muchos metales formando gas inflamable de hidrógeno.[3] En temperatura ambiente, es un líquido volátil, fumante al aire y más denso que este. No es inflamable y tiene un olor picante muy parecido al del ácido clorhídrico. Su densidad es 2,8 g/cm³ respecto al aire, y por presión y enfriamiento se licúa a −73 °C formando un líquido incoloro, que puede solidificarse a −120 °C en una masa cristalina. El peso de un litro de bromhídrico a la presión normal y a 0 °C de temperatura es de 3,6167 gramos. Al igual que el ácido clorhídrico, el ácido bromhídrico es muy soluble en el agua; reaccionando de forma violenta y liberando gas inflamable así como gases tóxicos; además, da un líquido de propiedades ácidas enérgicas que contiene los iones Br- y H+; un volumen de agua a 10 °C disuelve unos 600 volúmenes de bromhídrico, y la disolución saturada a 0 °C tiene un peso específico de 1,78 y contiene 82 % de HBr.[4] UsosEl ácido bromhídrico se utiliza para elaborar productos químicos y farmacéuticos, principalmente para la producción de bromuros inorgánicos, especialmente el bromuro de zinc, calcio y sodio, también se lo emplea como solvente y en medicación veterinaria. Es un reactivo útil para la regeneración de compuestos organobromados. Ciertos éteres se rompen con ácido bromhídrico. También funciona como catalizador de reacciones de alquilación y de la extracción de ciertos minerales. A partir de ácido bromhídrico se crean importantes compuestos orgánicos útiles para la industria, como lo son: bromuro de alilo, fenol y ácido bromoacético.[5] Referencias
Véase también
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Portal di Ensiklopedia Dunia