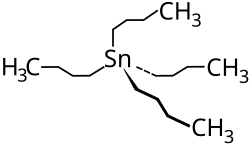
| Strukturformel
|
|
| Allgemeines
|
| Name
|
Tetrabutylzinn
|
| Andere Namen
|
- Tetrabutylstannan
- Zinntetrabutyl
- Tetra-n-butylzinn
|
| Summenformel
|
C16H36Sn
|
| Kurzbeschreibung
|
farblose Flüssigkeit mit charakteristischem Geruch[1]
|
| Externe Identifikatoren/Datenbanken
|
|
|
| Eigenschaften
|
| Molare Masse
|
347,17 g·mol−1
|
| Aggregatzustand
|
flüssig
|
| Dichte
|
1,05 g·cm−3[1]
|
| Schmelzpunkt
|
−97 °C[1]
|
| Siedepunkt
|
140 °C (10 mbar)[1]
|
| Dampfdruck
|
0,0014 mbar mbar (25 °C)[1]
|
| Löslichkeit
|
praktisch unlöslich in Wasser (0,008 g·l−1 bei 20 °C)[1]
|
| Brechungsindex
|
1,4742 (bei 20 °C und 589 nm)[2]
|
| Sicherheitshinweise
|
|
|
| Toxikologische Daten
|
1270 mg·kg−1 (LD50, Ratte, oral)[1]
|
Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet.
Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). Brechungsindex: Na-D-Linie, 20 °C
|
Tetrabutylzinn (abgekürzt TeBT oder TTBT nach englisch Tetrabutyltin) ist eine chemische Verbindung aus der Gruppe der Zinnorganischen Verbindungen.
Gewinnung und Darstellung
Tetrabutylzinn kann durch Umsetzung von Zinntetrachlorid mit Butylmagnesiumchlorid, Butyllithium oder direkt über eine Wurtz-Synthese durch Reaktion mit elementarem Natrium und 1-Chlorbutan gewonnen werden.[3][4]



Eigenschaften
Tetrabutylzinn ist eine farblose Flüssigkeit mit charakteristischem Geruch, die praktisch unlöslich in Wasser ist. Sie hat eine dynamische Viskosität von 4 mPa·s bei 20 °C.[1]
Verwendung
Tetrabutylzinn ist Ausgangsmaterial von Tributylzinn- und Dibutylzinn-Verbindungen, welche Ausgangsstoffe für eine breite Palette von zinnorganischen Verbindungen sind, die als Stabilisatoren für PVC, Biozide, Fungizide und Antifouling-Mittel verwendet werden.[5]
Einzelnachweise
- ↑ a b c d e f g h i j Eintrag zu Tetrabutylzinn in der GESTIS-Stoffdatenbank des IFA, abgerufen am 9. Januar 2019. (JavaScript erforderlich)
- ↑ Datenblatt Tetra-n-butylzinn bei Merck, abgerufen am 11. Januar 2012.
- ↑ Eintrag zu Tetra-n-butyltin in der Hazardous Substances Data Bank (via PubChem), abgerufen am 27. Juli 2012.
- ↑ Bernard Jousseaume: Organometallic Synthesis and Chemistry of Tin and Lead Compounds. In: Microchimica Acta. Band 109, Nr. 1–4, 1992, S. 5–12, doi:10.1007/BF01243203 (englisch).
- ↑ Hoch, M.: Organotin compounds in the environment — an overview. In: Applied Geochemistry. 16. Jahrgang, Nr. 7–8, 2001, S. 719–743, doi:10.1016/S0883-2927(00)00067-6.






