|
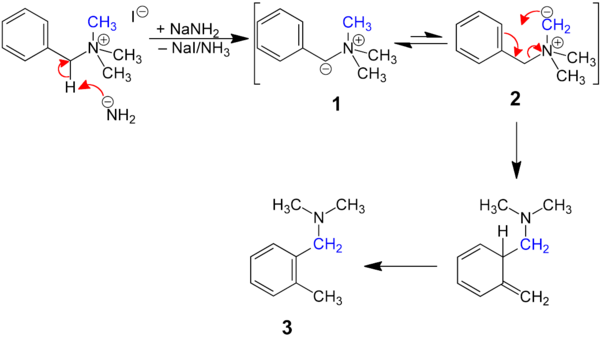
Sommelet-Hauser-UmlagerungDie Sommelet–Hauser-Umlagerung, auch Sommelettsche Umlagerung, ist benannt nach Marcel Sommelet[1] und Charles R. Hauser[2] (1900–1970). Sie zählt in der organischen Chemie zu den Umlagerungsreaktionen. Dabei werden quartäre Benzyl-Ammoniumsalze in tertiäre Amine umgelagert:[3] Die Umlagerung erfolgt unter dem Einfluss von Natriumamid oder einem anderen Alkalimetallamid. Ausgehend von einem Trialkylbenzylammoniumsalz (z. B. Trimethylbenzylammoniumsalz) erhält man durch die Sommelet–Hauser-Umlagerung ein N-Dialkylbenzylamin mit einem Alkylsubstituenten (z. B. Methylsubstituenten) in der ortho-Position des Aromaten:[4] Die Stevens-Umlagerung ist eine Konkurrenzreaktion der Sommelet–Hauser-Umlagerung.[5] ReaktionsmechanismusEines der Wasserstoffatome am Benzyl-Kohlenstoffatom ist unter basischen Bedingungen abspaltbar, wobei ein Ylid 1 resultiert. 1 steht im Gleichgewicht mit dem (weniger favorisierten!) isomeren Ylid 2, das sich nun umlagert ([2,3]-sigmatrope Umlagerung) unter Bildung eines ortho-Chinoids, das unter Rearomatisierung zum ortho-substituierten Amin 3 tautomerisiert.[6] AnwendungsbeispieleDie Sommelet–Hauser-Umlagerung ist breit anwendbar und wurde in der Totalsynthese des antibiotisch wirksamen Naturstoffes Streptonigrin eingesetzt.[5] Einzelnachweise
|
Portal di Ensiklopedia Dunia