|
RadikalanionenRadikalanionen sind Moleküle, die sowohl ein ungepaartes Elektron als auch eine negative Ladung aufweisen. Es handelt sich also gleichzeitig um Radikale und Anionen. Natürliche Vertreter Chinone, die 1,4-Benzochinon als Teilstruktur enthalten, beispielsweise Ubichinon und Plastochinon, sind wichtige Elektronenakzeptoren in biologischen Systemen. Dabei bildet sich zunächst durch Aufnahme eines Elektrons ein Radikalanion.[1] Superoxid ist ein Radikalanion, das durch Reduktion von molekularem Sauerstoff entsteht und ebenfalls verbreitet in biologischen Systemen gebildet wird. Da es hochreaktiv ist und auch mutagen wirken kann, muss es zur Vermeidung von Zellschäden abgebaut werden, was durch Superoxid-Dismutasen passiert.[2] Die blaue Farbe von Lasurit und Lapislazuli entsteht im Wesentlichen durch Trisulfid-Radikalanionen.[3] Synthetische Vertreter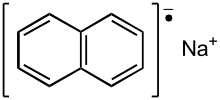 Polycyclische aromatische Kohlenwasserstoffe können unter geeigneten Bedingungen zwei Elektronen aufnehmen, wobei durch die Aufnahme des ersten Elektrons ein Radikalanion entsteht. Hergestellt werden diese Radikalanionen durch Reaktion eines entsprechenden Kohlenwasserstoffs mit Alkalimetallen (Lithium, Natrium, Kalium, Caesium). Geeignete aromatische Verbindungen, die eine solche Reaktion eingehen, sind beispielsweise Naphthalin, Anthracen, Perylen oder Biphenyl. Zum ersten Mal beschrieben wurde die Herstellung 1867 von Marcelin Berthelot, der Naphtalin mit Kalium schmolz. Aromaten-Radikalanionen können das aufgenommene Radikal wiederum auf andere Verbindungen übertragen. Daneben wirken sie als starke Basen. Beispielsweise können viele wenig acide Verbindungen wie Phenylacetylen, Acetylen, Fluoren oder Diphenylmethan mit Natriumnaphthalinid deprotoniert und dann mit Kohlenstoffdioxid zu einer Carbonsäure umgesetzt werden. So entsteht aus Acetylen Propiolsäure und aus Diphenylmethan Diphenylessigsäure. Durch Elektronenübertragung von Natriumnaphtalinid auf Alkylhalogenide entstehen Alkane und Alkene.[4] Einzelnachweise
|