|
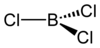
ثلاثي كلوريد البورون
ثلاثي كلوريد البورون هو مركب كيميائي من الكلور والبورون له الصيغة BCl3، ويكون على شكل غاز عديم اللون. التحضيريحضر ثلاثي كلوريد البورون بشكل صناعي من التفاعل المباشر بين عنصري الكلور والبورون، كما يحضّر المركب من تفاعل كلورة أكسيد البورون بوجود الفحم عند درجات حرارة حوالي 500 °س.[2] إن طريقة التحضير تدعى تفاعل كربوحراري وهي مشابهة لعملية كرول. يمكن التحضير بطريقة أخرى من خلال تفاعل المشتق الفينيلي العضوي من حمض البوريك مع كلوريد الألومنيوم:[2] يمكن الحصول على المركب مخبرياً من تفاعل ثلاثي فلوريد البورون مع كلوريد الألومنيوم، حيث يحصل تبادل بين الهاليدات.[3] الخواصإن ثلاثي كلوريد البورون عبارة عن غاز عديم اللون وغير قابل للاشتعال ويتفاعل ويتفكك بعنف مع الماء ومع الكحولات مثل الإيثانول، حيث تتشكل سحب من غاز كلوريد الهيدروجين. يتفكك المركب بالتسخين حيث يعطي كل من غازي الكلور وكلوريد الهيدروجين. يعد المركب من أحماض لويس القوية، حيث يتفاعل بسهولة مع الأمينات الثالثية ومركبات الفوسفين والإيثرات والثيوإيثرات وغيرها.[4] يكون لمركب ثلاثي كلوريد البورون بنية جزيئية مستوية ثلاثية مثل باقي هاليدات البورون، وتكون الرابطة B-Cl ذات طول مقداره 175 بيكومتر. إن تشكل معقدات من نواتج الإضافة يؤدي إلى ازدياد طول الرابطة إلى 184 بيكومتر.  الاستخداماتيستخدم ثلاثي كلوريد البورون كحفّاز في مجال الاصطناع العضوي لتخضير مركبات مثل البورازين، وفي تفاعلات الكلورة. يستخدم المركب أيضاً في مجال علم التعدين من أجل التخلص من مركبات النتريدات والكربيدات والأكاسيد المحتلفة من صهارات الألومنيوم والمغنسيوم والزنك والنحاس. المراجع
|
||||||||||||||||||||||||||||||||||||||||||