|
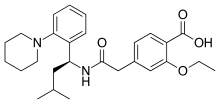
Repaglinida
Repaglinida adalah obat diabetes oral kerja pendek dari kelompok meglitinida untuk pengobatan diabetes melitus tipe 2. Repaglinida dikembangkan pada tahun 1983. Sejak 18 Februari 2016, meglitinida hanya dapat diganti oleh asuransi kesehatan wajib di Jerman dalam kasus individu yang dibenarkan secara medis, karena manfaatnya belum cukup terbukti melalui penelitian.[1] Bahan aktif ini tidak lagi tercantum dalam Pedoman Perawatan Nasional Jerman (NVL) untuk diabetes melitus tipe 2 mulai tahun 2021,[2] tetapi masih diresepkan oleh dokter spesialis diabetes dan dapat digunakan jika laju filtrasi glomerulus > 25 ml/menit.[3] SejarahObat prekursor repaglinida ditemukan pada akhir tahun 1983 oleh para ilmuwan di Dr Karl Thomae GmbH, sebuah produsen obat Jerman yang berlokasi di Biberach an der Riß di Jerman selatan yang diakuisisi oleh Boehringer Ingelheim pada tahun 1990. Obat yang menjadi repaglinida kemudian dilisensikan oleh Boehringer ke Novo Nordisk, yang mengajukan aplikasi Obat Baru Investigasi untuk senyawa tersebut ke Badan Pengawas Obat dan Makanan Amerika Serikat (FDA) pada bulan April 1992. Novo Nordisk mengajukan Aplikasi Obat Baru (NDA) untuk Prandin pada bulan Juli 1997 dan dengan cepat disetujui, memperoleh persetujuan FDA pada bulan Desember 1997. Obat tersebut adalah yang pertama dari kelas meglitinida. Obat tersebut diberi merek Prandin karena onsetnya yang cepat dan durasi kerjanya yang pendek memusatkan efeknya di sekitar waktu makan (prandium adalah makanan Romawi yang sebanding dengan makan siang modern).[4] Kegunaan medisRepaglinida adalah obat oral yang digunakan sebagai tambahan terhadap diet dan olahraga untuk mengontrol gula darah pada diabetes melitus tipe 2.[5] KontraindikasiRepaglinida dikontraindikasikan pada orang dengan:
Efek sampingEfek samping yang umum terjadi meliputi:[5]
Adapun efek samping yang serius meliputi:[5]
Populasi khususKategori kehamilan C: keamanan pada wanita hamil belum ditetapkan.[5] Data terbatas, dan hanya ada satu laporan kasus yang mencatat tidak ada komplikasi akibat penggunaan repaglinida selama kehamilan.[6] Perhatian harus diberikan pada orang dengan penyakit hati dan penurunan fungsi ginjal saat menggunakan obat ini.[5] InteraksiRepaglinida merupakan substrat utama CYP3A4 dan tidak boleh diberikan bersamaan dengan gemfibrozil, klaritromisin, atau antijamur azola seperti itrakonazol atau ketokonazol.[5] Pemberian repaglinida dan satu atau lebih obat ini menyebabkan peningkatan konsentrasi plasma repaglinida dan dapat menyebabkan hipoglikemia. Pemberian repaglinida dan klopidogrel (penghambat CYP2C8) secara bersamaan dapat menyebabkan penurunan kadar glukosa darah yang signifikan karena interaksi obat-obat.[7] Faktanya, penggunaan obat-obatan ini bersamaan bahkan untuk satu hari dapat menyebabkan kadar repaglinida meningkat lebih dari 5 kali lipat...dan dapat menyebabkan hipoglikemia yang signifikan. Repaglinida tidak boleh dikombinasikan dengan sulfonilurea, karena keduanya memiliki mekanisme kerja yang sama.[5] FarmakologiMekanisme kerjaRepaglinida menurunkan glukosa darah dengan merangsang pelepasan insulin dari sel-sel pulau beta pankreas. Obat ini bekerja dengan menutup saluran kalium yang bergantung pada ATP di membran sel-sel beta. Hal ini mendepolarisasi sel-sel beta, membuka saluran kalsium sel, dan masuknya kalsium yang dihasilkan menginduksi sekresi insulin.[5] Farmakokinetik
Hak kekayaan intelektualSetelah beberapa kali mencoba mengajukan perlindungan paten AS, pengajuan dilakukan pada bulan Maret 1990 yang akhirnya menjadi Paten AS 5.216.167 (Juni 1993), 5.312.924 (Mei 1994), dan 6.143.769 (November 2000). Setelah mengajukan NDA untuk repaglinida pada tahun 1997, Novo Nordisk mengajukan perpanjangan paten berdasarkan Undang-Undang Hatch-Waxman. Proses ini, yang disebut pemulihan jangka waktu paten, memungkinkan paten obat diperpanjang berdasarkan waktu yang dihabiskan obat dalam uji klinis dan dalam proses persetujuan. Sebelumnya telah diputuskan oleh Kantor Paten dan Merek Dagang Amerika Serikat bahwa tanggal kedaluwarsa Paten AS 5.216.167 dan 5.312.924 adalah 5 September 2006. Pada bulan Februari 2001, masa berlaku paten Prandin diperpanjang hingga 14 Maret 2009 sebagai tanggapan atas permohonan pemulihan jangka waktu paten Novo Nordisk, dengan Paten AS 5.216.167 yang telah diterbitkan ulang sebagai RE37035.[8] Sebelum berakhirnya jangka waktu paten repaglinida, Novo Nordisk memperoleh paten baru yakni Paten AS 6.677.358 (Januari 2004), yang mencakup terapi kombinasi repaglinida bersama dengan obat antidiabetik generik metformin. Paten baru ini seharusnya berakhir pada bulan Juni 2018. Pada bulan Januari 2011, pengadilan federal memutuskan bahwa paten baru Novo Nordisk tidak sah karena alasan sudah jelas, dan tidak dapat dilaksanakan karena alasan perilaku tidak adil dari pihak pengacara paten Novo Nordisk.[9] Referensi
Pranala luar
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Portal di Ensiklopedia Dunia