Відповідно виділені f атомні орбіталі можуть перекриватися, утворюючи φ молекулярну орбіталь (фі-зв'язок)
| Фі-зв'язок |
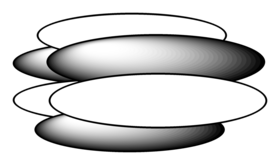 |
Фі-зв'язок (φ-зв'язок) — це ковалентний хімічний зв'язок, де шість долей однієї залученої до зв'язку атомної орбіталі з f-електроном, перекривають шість долей іншої атомної орбіталі. Це перекриття призводить до утворення зв'язуючої молекулярної орбіталі з трьома вузловими площинами, які містять міжядерну вісь і проходять через обидва атоми.
Грецька літера φ в їх назві позначає f-орбіталі електронів, оскільки орбітальна симетрія φ-зв'язку є такою ж, як у звичайної (6-лопатевої) орбіталі типу f, якщо дивитися по осі зв'язку.
У 2005 році був запропонований один кандидат цього типу зв'язку — молекула урану з фі-зв'язком: U-U зв'язок у молекулі U2[1]. Однак пізніші дослідження вчених ETH Цюриху, виявили, що це зв'язок був лише четвертого порядку і які пояснювали цей зв'язок спіно-орбітальною взаємодією[2][3]. Станом на 2020 рік не виявлено жодної молекули з фі-зв'язками.
Примітки