| Ортоарсенатна кислота
|

|
|
| Систематична назва
|
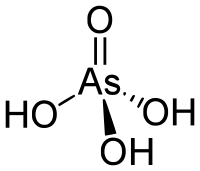
ортоарсенатна кислота
|
| Інші назви
|
миш'якова кислота, ортомиш'якова кислота, арсенатна кислота, ортоарсенова кислота
|
| Ідентифікатори
|
| Номер CAS |
7778-39-4 |
|---|
| PubChem |
234 |
|---|
| Номер EINECS |
231-901-9 |
|---|
| KEGG |
C01478 |
|---|
| ChEBI |
18231 |
|---|
| RTECS |
CG0700000 |
|---|
| SMILES |
O[As](=O)(O)O |
|---|
| InChI |
InChI=1S/AsH3O4/c2-1(3,4)5/h(H3,2,3,4,5) |
|---|
| Номер Гмеліна |
2294 |
|---|
| Властивості
|
| Молекулярна формула
|
H3AsO4
|
| Молярна маса
|
141,94 г/моль
|
| Зовнішній вигляд
|
безбарвні кристали
|
| Густина
|
2,6 г/см3
|
| Тпл
|
35,5 °C
|
| Ткип
|
розклад при > 100 °C
|
| Розчинність (вода)
|
16,7 г/100 мл
|
| Кислотність (pKa)
|
2,19, 6,94, 11,5
|
| Небезпеки
|
| Класифікація ЄС
|
 T T  N N
|
| NFPA 704
|
|
| Температура спалаху
|
Незаймиста
|
| Якщо не зазначено інше, дані наведено для речовин у стандартному стані (за 25 °C, 100 кПа)
|
| Інструкція з використання шаблону
|
| Примітки картки
|
О́ртоарсена́тна кислота — триосновна неорганічна кислота середньої сили складу H3AsO4, трохи слабша за ортофосфатну. Має вигляд білих прозорих кристалів. Розчинна у воді та спирті, осаджується із розчину у формі гемігідрату 2H3AsO4·H2O. Отруйна.
Кислота використовується при виробництві дезінфікуючих засобів, інсектицидів та скла.
Хімічні властивості
У водному розчинні арсенатна кислота дисоціює:
- H3AsO4
 H2AsO−
H2AsO−
4 + H+ (K1 = 6,3 ×10−3)
- H2AsO−
4  HAsO2−
HAsO2−
4 + H+ (K2 = 1,2 × 10−7)
- HAsO2−
4  AsO3−
AsO3−
4 + H+ (K3 = 3,2 × 10−12)
Відповідно можливе утворення трьох рядів солей (арсенатів), наприклад для натрію: Na3AsO4, Na2HAsO4 та NaH2AsO4. Арсенати нерозчинні у воді, за винятком солей лужних металів і амонію.
Арсенат-іон має форму тетраедра, в центрі якого знаходиться атом Арсену, довжина зв'язків As—O 0,175 нм. Якісною реакцією на арсенат-іон є осадження іонами срібла з нейтрального або слаболужного розчину з утворенням арсенату срібла (Ag3AsO4) коричневого кольору.
Отримання
Арсенатну кислоту можна отримати, розчинивши оксид арсену (V) у воді:
- As2O5 + 3H2O → 2H3AsO4
Проте частіше миш'якову кислоту отримують дією концентрованої нітратної кислоти (HNO3) на As або As2O3:
- 3As2O3 + 4HNO3 → 6H3AsO4 + 4NO.
Посилання
Джерела
- Дроздов А.А., Зломанов В.П., Мазо Г.Н., Спиридонов Ф.М. Неорганическая химия. — Москва : ИЦ «Академия», 2004. — Т. 2. — 368 с. — ISBN 5-7695-1436-1.
- Романова Н.В. (1998). Загальна та неорганічна хімія. Київ; Ірпінь: ВТФ «Перун». с. 480. ISBN 966-569-106-6.


