|
Кофермент Q
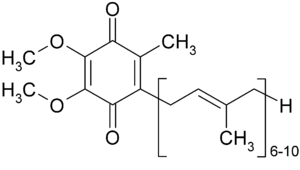
Кофермент Q (МНН: лат. Ubidecarenone, убидекаренон; также известен как кофермент Q10, убихинон, лат. ubiquinone, coenzyme Q10, coenzyme Q) — это группа коферментов — бензохинонов, содержащих хиноидную группу (отсюда обозначение Q) и содержащих несколько изопрениловых групп (например, 10 в случае кофермента Q10). Общие сведенияУбихиноны — это жирорастворимые коферменты, представленные преимущественно в митохондриях эукариотических клетках. Убихинон является компонентом цепи переноса электронов и принимает участие в окислительном фосфорилировании. Максимальное содержание убихинона в органах с наибольшими энергетическими потребностями, например, в сердце и печени. ИсторияВ 1955 году был впервые употреблён термин кофермент Q для обозначения вещества, содержащегося практически во всех живых клетках. В 1957-58 годах учёными Фредериком Крейном и Карлом Фолкерсом были получены препараты убихинона и было установлено его химическое строение. В 1965 году Ямамура с сотрудниками впервые применили кофермент Q для лечения сердечно-сосудистых заболеваний. В 1978 году за описание процессов хемиосмотического фосфорилирования Питер Митчелл удостоен Нобелевской премии по химии. В 1997 году основан Международный центр по изучению убихинона[уточнить]. Физико-химические свойстваПо химической природе кофермент Q имеет сходство в строении молекулы с витаминами Е и К и представляет собой 2,3-диметокси-5-метил-1,4-бензохинон с изопреновой цепью в 6-м положении. Число остатков изопрена в боковой цепи убихинона в разных организмах разнится от 6 до 10. Такие варианты кофермента Q обозначают как Сo Q6, Сo Q7 и т. д. В клетках Saccharomyces cerevisiae содержится Co Q6, Escherichia coli — Co Q8, грызунов — Co Q9. В митохондриях клеток большинства млекопитающих, включая человека, встречается убихинон только с 10 изопреновыми звеньями[1]. Кофермент Q представляет собой желто-оранжевые кристаллы без вкуса и запаха. Температура плавления 49—51° С. Растворим в диэтиловом эфире, очень слабо растворим в этаноле, практически нерастворим в воде. На свету постепенно разлагается и окрашивается. С водой образует эмульсию с концентрацией 10 %, 20 % и 40 %. Биосинтез убихинонаВ организме человека кофермент Q синтезируется из мевалоновой кислоты и производных тирозина и фенилаланина[1]. Биохимическая рольКофермент Q принимает участие в реакциях окислительного фосфорилирования, является звеном в цепи переноса электронов в митохондриях. Ингибиторы работы убихинона останавливают реакции окислительного фосфорилирования. Кофермент Q является звеном в цепи переноса электронов, принимает участие в переносе электронов с NADH-дегидрогеназного комплекса (комплекс I) и сукцинатдегидрогеназного комплекса (II) на комплекс III, и участвует таким образом в синтезе АТФ. Также кофермент Q является антиоксидантом и, в отличие от других антиоксидантов, регенерируется организмом. Кроме того, кофермент Q восстанавливает антиоксидантную активность витамина Е — α-токоферола. Антиоксидантное действие кофермента Q обусловлено главным образом его восстановленной формой (Co QH2). Активность восстановленной формы кофермента Q на три порядка выше невосстановленной. Реакцию нейтрализации свободных радикалов восстановленным коферментом Q можно записать следующим образом Содержание в различных тканях организмаКофермент Q необходим для нормальной жизнедеятельности живых организмов и, прежде всего, для функционирования тканей с высоким уровнем энергетического обмена. Наибольшая концентрация кофермента Q — в тканях сердечной мышцы. Естественный уровень кофермента Q в плазме крови человека составляет около 0.8-1.2 мкг/мл[2][3]. ДефицитОсновными причинами, которые могут вести к недостатку CoQ10 у людей: уменьшение биосинтеза и повышенный расход организмом. Основным источником кофермента является биосинтез, для него требуется исправная работа по крайней мере 12 генов, и мутация в них может приводить к недостатку. Также недостаток Q10 может развиваться из-за других генетических дефектов, в частности из-за мутации митохондриальной ДНК, генов ETFDH, APTX, FXN, и BRAF[4]. Содержание кофермента Q в различных продуктах
Приготовление продуктов через жарку уменьшает содержание CoQ10 на 14–32%.[5] В развитых странах ежедневное поступление Q10 с пищей оценивается отдельным исследованиями в 3-6 мг, большей частью из мяса[6]. Пищевые добавки с коферментом Q10Кофермент Q10 не был одобрен американским регулятором FDA в качестве лекарственного средства для применения при каких-либо заболеваниях[7]. Способы улучшения биодоступности кофермента Q10Кофермент Q10 является жирорастворимым соединением с большим размером молекулы. Усвоение кофермента Q10 организмом происходит так же, как и всех жирорастворимых веществ. Его всасывание, как и всех жирорастворимых веществ, происходит в тонком кишечнике с обязательным этапом предварительного эмульгирования желчью и образованием мицелл. В составе мицелл он проникает в клетки кишечника. Эффективность всасывания зависит от:
Производители[какие?] прибегают к использованию различных способов для улучшения биодоступности в выпускаемых препаратах кофермента Q10. Уменьшение размеров частицОчевидным путём повышения биодоступности является уменьшение частиц кофермента Q10 до микро- и наноразмеров. На примере многих лекарственных веществ было показано, что уменьшение размеров частиц приводит к изменению биодоступности и эффективности[8]. Однако в целом, применительно к коферменту Q10[9], уменьшение размеров частиц не приводит к большому успеху в повышении биодоступности[10]. Заключение в капсулы с масломХорошо известен тот факт, что всасывание жирорастворимых веществ улучшается, если в пище присутствуют липиды. Поэтому некоторые производители[какие?] для повышения биодоступности кофермента Q10 в препарате заключают его в капсулы с маслом. Повышение растворимости в водеПовышение биодоступности лекарственных веществ путём улучшения его растворимости в воде является часто используемым и применим также и к коферменту Q10. Примером такого подхода является получение водно-масляной микроэмульсии. Жирорастворимая форма Q10 с помощью пищевого эмульгатора переводится в водорастворимую форму, при этом образуются микроэмульсия, состоящая из водной фазы и ассоциатов Q10-эмульгатор. Технология молекулярного капсулирования позволяет переводить жирорастворимые вещества в водорастворимую форму; избежать в процессе всасывания этапа эмульгирования желчью жирорастворимого вещества; уменьшить размер частиц жирорастворимого вещества до всасываемых размеров. Это обеспечивает максимальное усваивание препарата, увеличивает биодоступность по сравнению с жирорастворимой формой Q10 в 2,6 раза[11] и делает препарат более эффективным. Применение в медицинеКардиологияПо данным независимого метаанализа 2014 года, проведённого Кокрейном, не было обнаружено убедительных доказательств в пользу использования Кофермента Q10 при лечении сердечной недостаточности[12]. Также недостаточны доказательства того, что кофермент Q10 способствует снижению риска сердечных заболеваний[13]. Препараты на основе кофермента Q позиционируются отдельными авторами для применения при профилактике и терапии заболеваний сердечно-сосудистой системы. Было показано, что кофермент Q эффективен[14] в комплексной терапии:
Сердечная недостаточностьБольшинство исследований по клиническому применению кофермента Q10 было проведено именно при сердечной недостаточности. Также было показано, что тяжесть сердечной недостаточности коррелирует с низким уровнем кофермента Q[23]. Наиболее масштабное исследование было проведено в 1994 году в Италии: в исследовании приняли участие 2 664 человека с сердечной недостаточностью[24]. За три месяца лечения у значительной части больных наблюдалось заметное улучшение состояния. При этом нормализовались следующие показатели: цианоз (у 78,1%), отеки (у 78,6%), субъективное ощущение больными аритмии (у 63,4%), бессонница (у 66,28%), головокружение (у 73,1%). Побочные явления наблюдались у 36 больных (1,5 %), из которых только у двадцати человек они были связаны с применением кофермента Q. Ишемическая болезнь сердцаЭффективность применения препаратов кофермента Q при ишемической болезни сердца показана лишь в отдельных клинических исследованиях на малых группах. В одном из исследований 73 пациента после острого инфаркта миокарда наряду со стандартной терапией получали кофермент Q, участники контрольной группы (71 пациент) продолжали стандартную терапию. Через двенадцать месяцев применения было выявлено, что в группе, принимавшей препараты кофермента Q, в 2 раза реже случались сердечно-сосудистые события (24% против 45%), нефатальные инфаркты миокарда (13,7 % против 25 %) и кардиальная смерть. При этом тошнота намного чаще отмечалась у больных контрольной группы (40,8 % против 6,8 %), что свидетельствует об отсутствии побочных эффектов[17]. Выявлен возможный механизм положительного действия кофермента Q — предотвращение развития синдрома удлинённого QT. Как известно, данный синдром связан с более частой кардиальной смертью, особенно у больных инфарктом миокарда. Исследователи в течение 1 года наблюдали больных с острым инфарктом миокарда. Через 6 часов после начала острого инфаркта миокарда больные на фоне одинакового лечения, применяемого в постинфарктном периоде, получали либо плацебо, либо комплекс антиоксидантов, состоящий из кофермента Q и селена. У 40% больных контрольной группы наблюдалось удлинение интервала QT > 440 мсек., в группе, получавшей антиоксиданты, удлинения интервала не наблюдалось. В течение года умерло от повторных инфарктов шесть больных контрольной группы и ни одного пациента из основной группы (за исключением одной смерти от некардиальной причины)[16]. Артериальная гипертензияПо данным обзора группы Cochrane в 2009 году, клинические исследования влияния CoQ10 на артериальное давление являются ненадежными, и на их основе не может быть сделано вывода об эффективности CoQ10 для снижения давления[25]. В более раннем обзоре, выполненном в Австралии, было показан гипотензивное действие кофермента Q. Были проанализированы 12 клинических исследований применения кофермента Q при артериальной гипертензии. По данным трех рандомизированных контролируемых исследований (суммарно на 120 пациентах) прием кофермента Q при артериальной гипертензии приводил к снижению систолического артериального давления в среднем на 12-20 мм рт. ст., а диастолического — на 6-10 мм рт. ст. Таким образом, по предположению авторов кофермент Q имеет некоторый потенциал для пациентов с гипертензией как средство, снижающее давление[18]. Совместный прием кофермента Q и препаратов статиновСтатины представляют собой вещества, ингибирующие 3-гидрокси-3-метилглутарил-коэнзим-А-редуктазу и снижающие синтез мевалоната — основного метаболического компонента на пути синтеза холестерина. Применение этих препаратов может вызывать жалобы пациентов на мышечную боль или миопатию. Так как путь к синтезу мевалоната также ведет к синтезу изопреноидной цепи кофермента Q10, различные исследования были посвящены изучению CoQ10 как возможного этиологического фактора статиновой миопатии. Данный вопрос широко изучался и хорошо описан в двух обзорных статьях[26][27]. Было подчеркнуто, что, помимо снижения концентраций CoQ10 в плазме, лечение статинами также приводит к снижению концентраций CoQ10 в лимфоцитах. Несмотря на то, что не существует однозначных данных по эффекту статинов на концентрацию CoQ10 в скелетной мышце[28][29], в 2005 году было показано, что высокие дозы статинов действительно приводят к снижению концентрации CoQ10 и уменьшению активности дыхательной цепи митохондрий в мышцах, что, возможно, связано со снижением числа или объёма мышечных митохондрий[30]. В исследовании 2008 года была выявлена обратная зависимость между изменениями концентрации CoQ10, вызванными аторвастатином, и мозговым натрийуретическим пропептидом (МНПП). Был сделан вывод, что длительное лечение аторвастатином может увеличить уровни МНПП в плазме крови у пациентов с ишемической болезнью сердца при сопутствующем значительном снижении концентраций CoQ10[31]. Что касается эффективности, в одном исследовании не было выявлено улучшения переносимости статинов или снижения миалгии[32], тогда как Касо и др.[33] сообщили о положительном эффекте CoQ10 на выраженность боли и влияние боли на повседневную активность в группе пациентов, получавших статины, с симптомами миопатии. См. такжеПримечания
Ссылки
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||