|
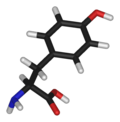
Tirosina
  A tirosina (abreviadamente Tyr ou Y)[4] ou 4-hidroxifenilalanina, É um dos 20 aminoácidos que fazem parte das proteínas. É um α-aminoácido com uma cadeia lateral formada por CH2 ligado a um grupo fenol, o que a torna uma cadeia lateral cíclica aromática com um grupo OH, que lhe confere um carácter polar branco. Os seus codões são o UAC e o UAU. É um aminoácido proteinogénico não essencial. O seu nome tem origem do grego tyri, que significa queijo, dado que foi descoberta em 1846 pelo químico alemão Justus von Liebig na proteína caseína do queijo.[5][6] O seu grupo funcional é designado tirosil. Funções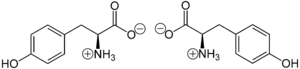 Para além do seu papel como componente das proteínas, a tirosina tem funções especiais devido ao seu grupo fenol. Constitui parte importante das proteínas que intervêm em processos de transdução de sinais na célula. Funciona como um receptor de grupos fosfato que se transferem por meio de proteínas quinases. A fosforilação do seu grupo hidroxilo modifica a actividade da proteína alvo. Um resíduo de tirosina tem também uma função muito importante na fotossíntese. No fotossistema II dos cloroplastos actua como um doador de electrões na redução da clorofila oxidada. Neste processo, a tirosina sofre desprotonação do seu grupo OH fenólico. Este radical é depois reduzido no fotossistema II pelos clusters de manganésio. Fontes alimentaresA tirosina pode sintetizar-se no corpo a partir de fenilalanina, pelo que não é essencial. A tirosina abunda em vários alimentos ricos em conteúdo proteico, como soja, frango, peru, peixe, amendoins, amêndoas, abacates, produtos lácteos, feijão de Lima, sementes de cabaça, e de sésamo.[7] BiossínteseNão pode ser completamente sintetizada pelos animais, apesar de poder ser gerada por hidroxilação da fenilalanina, se esta última existir em excesso. Esse aminoácido também é utilizado na síntese da adrenalina e da dopamina, neurotransmissores do corpo humano. Referências
Ligações externas |
||||||||||||||||||||||||||||||||||||||||||||||