|
ポテンシャルエネルギー曲面ポテンシャルエネルギー曲面(ポテンシャルエネルギーきょくめん、英: potential energy surface, PES)とは、特定のパラメータ(原子のデカルト座標や結合角、二面角など)に対して系のエネルギーを表したものである。エネルギーは単一の座標の関数である場合もあれば、複数の座標の場合もある。座標が単一の場合はポテンシャルエネルギー曲線またはエネルギー断面と呼ばれる。モース長距離ポテンシャルはその一例である。 地形とのアナロジーは理解の助けになる。2自由度系の例として二つの結合長を持つ系では、それぞれの結合長の値が基底面の平面座標にあたり、それらの関数であるエネルギーの値はその座標の高度を表している[1]。 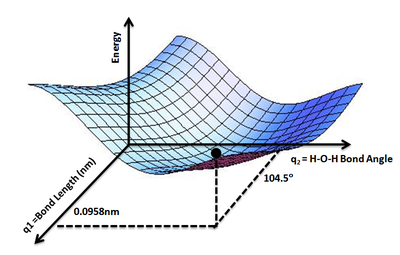 PESの概念は化学や物理学の中でも理論的な領域で応用がある。例えば分子のエネルギーを最小化する形状を求めたり、化学反応の速度を計算するなど、原子からなる構造の特性を理論的に研究する上で有用である。 数学的定義と計算ある原子の組の配置は原子位置を要素とするベクトル R によって記述される。ベクトル R は原子のデカルト座標の組として表してもいいし、原子間距離と結合角の組でも構わない。 系の全原子位置 R の関数として表したポテンシャルエネルギーの値を E(R) とする。前述のように地形とのアナロジーを用いると、E は地形面の高さにあたる。 原子位置の関数としてのPESを化学反応の研究に用いるには、考えられるすべての原子配列に対してエネルギーを計算しなければならない。特定の原子配列のエネルギーを計算する方法については計算化学の記事に譲り、ここでは E(R) を近似することでエネルギーと位置の関係についての情報を高い粒度で求める方法に重点を置く。 非常に単純な化学系や、原子間相互作用を簡略化した近似を用いる場合には、エネルギーを原子位置の関数として表す式を解析的に導くことも可能である。例として、H + H2 系におけるロンドン・アイリング・ポランニー・佐藤ポテンシャルは3つのH-H原子間距離の関数である[2][3][4]。 より複雑なシステムの場合、特定の原子配列に関するエネルギーの計算コストが高くなりすぎ、広範囲のPESを作れないことが多い。その場合はPES上の限られた点でのみ計算を行い、シェパード法のような計算コストの低い補間法を用いてギャップを埋めていく方法がある[5]。 応用PESは分子構造と化学反応のダイナミクスを分析するための概念的なツールとなる。PES上に必要なだけ点を取って値の評価を行えば、位置に関するエネルギーの1次および2次導関数(それぞれ勾配と曲率にあたる)に従ってそれらの点を分類することができる。勾配ゼロの点は停留点と呼ばれ、物理的に重要である。停留点のうちエネルギー最小の点は物理的に安定な化学種にあたり、鞍点は遷移状態にあたる。遷移状態とは、反応物と生成物を結ぶ最低エネルギーの経路(反応座標)上でエネルギーが最大となる点を意味する。 引力的および斥力的な曲面化学反応のポテンシャルエネルギー曲面には「引力的」と「斥力的」の区別がある。反応物の結合長が活性錯体になるとき伸びる量と、生成物の結合長が活性錯体のときから見て短くなった量を比べてどちらが大きいかによる分類である[6][7]。A + B-C → A-B + C の型の反応では、新しく形成されたA-B結合の結合長変化が R*AB = R0AB − RAB と定義される。ここで RAB は遷移状態の、R0AB は生成分子のA-B結合長を表す。同様に切断される結合の結合長変化が R*BC = RBC − R0BC と定義される。R0BC は反応物分子のB-C結合長である[8]。 発熱反応においては、R*AB > R*BC ならば反応物どうしが互いに近づくと遷移状態に達する。よってこのPESは「引力的」である。遷移状態を超えたのちもA-B結合長は減少し続けるので、解放された反応エネルギーの多くはA-B結合の振動エネルギーに変換される[8][9]。例としては銛打ち反応K + Br2 → K-Br + Br がある。この反応では反応物どうしの長距離引力が原因となってK+ ••• Br− ••• Br と近似できるような活性錯体が生まれる[8]。振動的に励起された生成分子は赤外線化学発光によって検出できる[10][11]。 逆に R*AB < R*BC ならば、生成物が遠ざかることで遷移状態に達するため、斥力的なPESである[8][9]。反応 H + Cl2 → HCl + Cl は斥力的PESの例である。原子A(Hにあたる)がBやC(Clにあたる)より軽いこの反応では、反応エネルギーは主に生成物の並進運動のエネルギーとして放出される。F + H2 → HF + H のように原子AがBやCより重い反応になると、PESが斥力的であっても、放出されるエネルギーは振動と並進が混在している[8]。 吸熱反応の場合、反応を引き起こすのに適したエネルギーの種類がPESの型によって決まる。引力的な曲面で反応を誘起するには反応物が持つ並進エネルギーが効果的であり、斥力的な曲面では反応物が振動的に励起されている方が効果的である[8]。後者の例として[12]、HCl の全エネルギーが同じならば、F + HCl(v=1) → Cl + HF の反応は F + HCl(v=0) → Cl + HFよりも約5倍速い[13]。 歴史化学反応におけるポテンシャルエネルギー曲面の概念は、1913年にフランスの物理学者ルネ・マルスランによって最初に提案された[14]。初めてポテンシャルエネルギー曲面の半経験的計算が行われたのは1931年のことで、ヘンリー・アイリングとマイケル・ポランニーがH + H2反応について行った。アイリングは1935年にポテンシャルエネルギー曲面を用いて遷移状態理論における反応速度定数を計算した。 関連項目
脚注
|