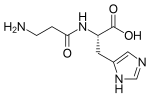
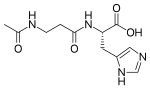
La serilalanina , un dipeptide composto da serina (nero) e alanina (blu). Un dipeptide è un composto organico formato da due aminoacidi legati da un legame peptidico . Diversi dipeptidi sono fisiologicamente importanti e alcuni sono sia fisiologicamente che commercialmente significativi.
Struttura
Lineare
Come tutte le strutture proteiche, un dipeptide ha un'estremità da cui sporge il gruppo carbossilico chiamata estremità C-terminale , e un'altra estremità da cui sporge il gruppo amminico chiamata estremità N-terminale . Queste due porzioni sono quelle che generalmente reagiscono con le altre molecole.
A temperatura ambiente, i dipeptidi sono quasi tutti dei solidi bianchi, molto più solubili in acqua degli aminoacidi progenitori.[ 1] alanilglutammina ha una solubilità di 586 g/L, circa 10 volte la solubilità della glutammina che è 35 g/L. Poiché i dipeptidi sono inclini all'idrolisi , l'elevata solubilità viene sfruttata nell'alimentazione umana e non.[ 2]
Ciclica
La ciclizzazione di un dipeptide porta alla formazione di dichetopiperazine . Spesso questa classe di molecole è formata da amminoacidi non proteinogenici .[ 3]
Esempi rilevanti
Voci correlate
^ (EN Synthesis and application of dipeptides; current status and perspectives Applied Microbiology and Biotechnology , vol. 81, n. 1, 1º novembre 2008, pp. 13–22, DOI :10.1007/s00253-008-1590-3 . URL consultato il 19 marzo 2022 . ^ (EN Glutamine dipeptides in clinical nutrition Nutrition , vol. 13, n. 7, 1º luglio 1997, pp. 731–737, DOI :10.1016/S0899-9007(97)83035-3 . URL consultato il 19 marzo 2022 . ^ Alan D. Borthwick, 2,5-Diketopiperazines: Synthesis, Reactions, Medicinal Chemistry, and Bioactive Natural Products Chemical Reviews , vol. 112, n. 7, 11 luglio 2012, pp. 3641–3716, DOI :10.1021/cr200398y . URL consultato il 19 marzo 2022 . ^ E. C. Bate Smith, The buffering of muscle in rigor; protein, phosphate and carnosine The Journal of Physiology , vol. 92, n. 3, 14 aprile 1938, pp. 336–343, DOI :10.1113/jphysiol.1938.sp003605 . URL consultato il 19 marzo 2022 . ^ a b V. Prakash Reddy, Matthew R. Garrett e George Perry, Carnosine: A Versatile Antioxidant and Antiglycating Agent Science of Aging Knowledge Environment , vol. 2005, n. 18, 4 maggio 2005, DOI :10.1126/sageke.2005.18.pe12 . URL consultato il 19 marzo 2022 . ^ (EN Effects of Beta-Alanine on Muscle Carnosine and Exercise Performance: A Review of the Current Literature Nutrients , vol. 2, n. 1, 2010-01, pp. 75–98, DOI :10.3390/nu2010075 . URL consultato il 19 marzo 2022 . ^ Audrey Baguet, Jan Bourgois e Lander Vanhee, Important role of muscle carnosine in rowing performance Journal of Applied Physiology , vol. 109, n. 4, 1º ottobre 2010, pp. 1096–1101, DOI :10.1152/japplphysiol.00141.2010 . URL consultato il 19 marzo 2022 . ^ A. Boldyrev e H. Abe, Metabolic transformation of neuropeptide carnosine modifies its biological activity Cellular and Molecular Neurobiology , vol. 19, n. 1, 1999-02, pp. 163–175, DOI :10.1023/a:1006933028389 . URL consultato il 19 marzo 2022 .
Altri progetti
Portale Chimica : il portale della scienza della composizione, delle proprietà e delle trasformazioni della materia