|
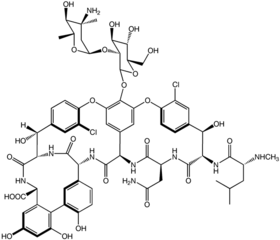
| Vancomycine
|
|
| Identification |
| No CAS
|
1404-90-6
|
| No ECHA
|
100.014.338 |
| No CE
|
215-772-6
|
| Code ATC
|
A07AA09, J01XA01
|
| DrugBank
|
DB00512
|
| PubChem
|
14969
|
| SMILES
|
CC1C(C(CC(O1)OC2C(C(C(OC2OC3=C4C=C5C=C3OC6=C(C=C(C=C6)C(C(C(=O)NC(C(=O)NC5C(=O)NC7C8=CC(=C(C=C8)O)C9=C(C=C(C=C9C(NC(=O)C(C(C1=CC(=C(O4)C=C1)Cl)O)NC7=O)C(=O)O)O)O)CC(=O)N)NC(=O)C(CC(C)C)NC)O)Cl)CO)O)O)(C)N)O PubChem, vue 3D |
| InChI
|
InChI : vue 3D InChI=1/C66H75Cl2N9O24/c1-23(2)12-34(71-5)58(88)76-49-51(83)26-7-10-38(32(67)14-26)97-40-16-28-17-41(55(40)101-65-56(54(86)53(85)42(22-78)99-65)100-44-21-66(4,70)57(87)24(3)96-44)98-39-11-8-27(15-33(39)68)52(84)50-63(93)75-48(64(94)95)31-18-29(79)19-37(81)45(31)30-13-25(6-9-36(30)80)46(60(90)77-50)74-61(91)47(28)73-59(89)35(20-43(69)82)72-62(49)92/h6-11,13-19,23-24,34-35,42,44,46-54,56-57,65,71,78-81,83-87H,12,20-22,70H2,1-5H3,(H2,69,82)(H,72,92)(H,73,89)(H,74,91)(H,75,93)(H,76,88)(H,77,90)(H,94,95)/t24-,34+,35-,42+,44-,46+,47+,48-,49+,50-,51+,52+,53+,54-,56+,57+,65-,66-/m0/s1/f/h72-77,94H,69H2 |
| Apparence
|
Solide
|
| Propriétés chimiques |
| Formule
|
C66H75Cl2N9O24 [Isomères]
|
| Masse molaire[1]
|
1 449,254 ± 0,071 g/mol
C 54,7 %, H 5,22 %, Cl 4,89 %, N 8,7 %, O 26,5 %,
|
| Écotoxicologie |
| DL50
|
430 mg·kg-1 souris i.v.
5 000 mg·kg-1 souris s.c.
1 734 mg·kg-1 souris i.p.
|
| Données pharmacocinétiques |
| Biodisponibilité
|
~0 % par voie orale
|
| Métabolisme
|
Non métabolisée
|
| Demi-vie d’élim.
|
4 à 11 h (adultes)
6 à 10 h (insuff. rénaux)
|
| Excrétion
|
Rénale
|
| Considérations thérapeutiques |
| Classe thérapeutique
|
Antibiotique glycopeptide
|
| Voie d’administration
|
Intraveineuse
|
| Grossesse
|
Utilisable
en cas de nécessité
|
|
| Unités du SI et CNTP, sauf indication contraire. |
modifier  |
La vancomycine est un antibiotique de la famille des glycopeptides. Volumineuse (1 500 à 2 000 daltons) et complexe, cette molécule est, au même titre que les β-lactamines, une inhibitrice de la synthèse du peptidoglycane de la paroi bactérienne (c'est-à-dire qu'elle tue la bactérie en l'empêchant de construire son enveloppe).
Cependant, du fait de son poids élevé, elle ne peut emprunter les pores (porines) de la membrane externe des bactéries Gram négatifs. Son spectre d’action est donc limité aux Gram positifs.
La vancomycine est bactéricide, mais cette bactéricidie est lente à apparaître ; sa biodisponibilité par voie orale est négligeable, la voie intraveineuse s’impose donc dans toutes les indications sauf une, le traitement par voie orale de la colite pseudomembraneuse.
Les principaux effets secondaires sont une atteinte rénale et auditive, il est donc justifié d’entreprendre une surveillance régulière des taux plasmatiques de vancomycine.
Enfin, son coût n'est pas négligeable et elle est souvent un traitement de dernier recours.
Après l'apparition de nombreux cas d'antibiorésistance, une variante vancomycine 2.0., puis vancomycine 3.0. (2017) ont été mises au point. La version n°3 associe 3 propriétés antibiotiques différentes dans la même molécule, ce qui devrait rendre plus difficile l'apparition de résistances chez les bactéries. En 2017, elle est annoncée par le fabricant comme étant 25 000 fois plus puissante que la précédente[2].
Indications des glycopeptides
En curatif, elles se limitent aux situations suivantes :
Deux situations prophylactiques sont éventuellement possibles :
- antibioprophylaxie de l’endocardite bactérienne chez des patients porteurs d’une cardiopathie à risque, allergiques aux β-lactamines et devant subir un geste à risque ;
- antibioprophylaxie des infections du site opératoire dans des chirurgies à risque staphylococcique (chirurgie cardiaque, vasculaire, orthopédique, neurochirurgie), dans des circonstances où le risque d’infection à staphylocoque résistant à la méticilline est accru (reprise chirurgicale précoce surtout) ou chez des patients allergiques aux β-lactamines.
Spectre d’action
La vancomycine exerce son action uniquement sur les Gram positifs :
- staphylocoques, tel le Staphylococcus aureus ou les staphylocoques à coagulase négative, même résistant à la méticilline (dans ce cas, les résistances restent exceptionnelles) ;
- streptocoques, quels qu’ils soient, y compris les souches de sensibilité diminuée à la pénicilline ;
- les entérocoques (mais il est possible de rencontrer en clinique humaine des souches d’entérocoques [surtout chez E faecium] résistant aux glycopeptides) ;
- anaérobies stricts à Gram positifs : cocci anaérobies, Clostridium (C perfringens et C difficile), la vancomycine par voie orale est active dans le cas des colites pseudomembraneuses à C difficile ;
- Listeria monocytogène : activité bactériostatique in vitro, mais la diffusion de la vancomycine est aléatoire dans le liquide céphalorachidien lorsque les méninges sont enflammées ; en clinique, ces méningites sont donc traitées à l'ampicilline, et même si le traitement empirique en début de prise en charge d'une méningite inclut déjà de la vancomycine IV, on y ajoute de l'ampicilline si les circonstances font suspecter Listeria comme agent causal (par exemple, dans le cas d'un patient âgé ou immunosupprimé).
Pharmacodynamie
Comme pour les β-lactamines, la vancomycine est inhibitrice de la synthèse du peptidoglycane de la paroi bactérienne . Son mécanisme d’action est toutefois différent : elle se fixe au niveau des extrémités peptidyl-D-Ala-D-Ala des précurseurs lipopeptidiques lorsqu'ils émergent de la membrane cytoplasmique, durant leur transport à travers celle-ci, et inhibe ainsi les étapes de transglycosylation et de transpeptidation, nécessaires à la bonne synthèse du peptidoglycane, action subséquente de la transpeptidase (qui catalyse l'enlèvement du D-Ala terminal et la réticulation du peptidoglycane).
Plus prosaïquement, elle agit en se liant aux composants de la paroi des bactéries à Gram positifs et en provoquant la dégradation de celle-ci.
Pharmacocinétique
- La biodisponibilité orale est négligeable. Par voie parentérale, l'administration intraveineuse d'une dose de 1 g permet d'obtenir, deux heures après l'injection, des taux sériques moyens de 25 μg·ml-1. Vers la 11e heure, la concentration est de 3 à 12 μg·ml-1.
- La liaison aux protéines plasmatiques est de 30 à 60 % aux concentrations thérapeutiques.
- La demi-vie sérique, très variable d'un sujet à l'autre, est de 4 à 11 heures.
- La diffusion de la vancomycine est bonne dans les liquides pleural, synovial, péritonéal et péricardique ; par contre, elle est nulle dans le liquide céphalorachidien lorsque les méninges sont saines et aléatoire lorsque celles-ci sont enflammées.
- La vancomycine n'est pas métabolisée dans l'organisme et son excrétion se fait à environ 90 % par le rein sous forme active (dont 75 % en 24 heures).
Effets secondaires
- Les réactions anaphylactoïdes, induites par une histamino-libération comportent des douleurs de type pulsatile dans les muscles du dos et du cou, des réactions de flush cutané du cou et des épaules, avec une fine éruption transitoire, éventuellement urticarienne : c’est le syndrome de « l’homme-rouge ». Exceptionnellement, une hypotension, voire un collapsus cardiovasculaire (en particulier chez l'enfant et le nourrisson) ont été observés lors d'injections rapides. Dans la plupart des cas, ces réactions peuvent être évitées par une perfusion lente (en 60 min minimum) et une dilution suffisante.
- Nausées et vomissements sont des effets indésirables possibles.
- La toxicité veineuse locale (endoveinite) est consécutive à l'administration par voie périphérique. Elle incite à préférer une voie centrale.
- Les risques d'ototoxicité cochléaire et de néphrotoxicité (tubulopathie) sont accrus de façon sensible lorsque les concentrations plasmatiques de vancomycine sont élevées ou le traitement prolongé. Ils le sont d’autant plus que le patient présente une insuffisance rénale. Quelques cas d'atteinte rénale irréversible ont été décrits. L'ototoxicité, surtout rencontrée lors de concentrations plasmatiques supérieures à 70–80 mg·l-1, et la néphrotoxicité sont potentialisées par l'administration conjointe à d’autres molécules oto- et néphrotoxique, tels les aminosides.
- Les réactions d’hypersensibilité s’observent principalement à partir du 7e jour : éruption cutanée généralisée, hyperéosinophilie, fièvre.
- De rares cas de thrombopénies (de cause immuno-allergique, c'est-à-dire par formation d'anticorps antiplaquettes sanguines[3]) et de neutropénies, parfois sévères mais rapidement réversibles à l'arrêt du traitement, ont été signalés lors de traitements prolongés.
- Une prise de poids a été décrite lors d'une étude dans le cadre du traitement des endocardites[4].
Résistance
Utilisée depuis 1956 et malgré son usage en dernier recours, la vancomycine n'en est pas pour autant à l'abri du développement de résistances. Il existe ainsi des ERV, entérocoques résistant à la vancomycine, chez lesquels la structure D-Ala-D-Ala des précurseurs du peptidoglycane est remplacée par une structure D-Ala-D-Lactate ne permettant pas la liaison de la vancomycine. Très peu de traitements de dernière ligne sont disponibles contre ces bactéries. On citera par exemple le linézolide. Le risque d'apparition de telles résistances parmi d'autres groupes de bactéries, dont les staphylocoques, en restreint d'autant plus l'usage.
Liens externes
- Compendium suisse des médicaments : spécialités contenant Vancomycine
Références
- ↑ Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- ↑ Robert Service (2017), Superantibiotic is 25,000 times more potent than its predecessor, 30 mai 2017
- ↑ Annette Von Drygalski, Brian R. Curtis, Daniel W. Bougie, Janice G. McFarland, Scott Ahl, Indra Limbu, Kelty R. Baker, Richard H. Aster, Vancomycin-induced immune thrombocytopenia, New Eng J Med, 2007;356:904-910
- ↑ Thuny F, Richet H, Casalta JP, Angelakis E, Habib G, Raoult D, Vancomycin Treatment of Infective Endocarditis Is Linked with Recently Acquired Obesity, PLoS ONE 5(2): e9074. doi:10.1371/journal.pone.0009074
- Y Domart. Glycopeptides. Encycl Méd Chir (Elsevier, Paris), Encyclopédie pratique de médecine, 5-0060, 1998, 2 p
- J. Tankovic, [Antibacterial antibiotics. General data on mode of action and mechanisms of resistance]. Rev Prat. 2000;50(4);425-32 PMID 10748677
|
