|
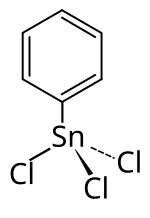
| Strukturformel
|
|
| Allgemeines
|
| Name
|
Phenylzinntrichlorid
|
| Andere Namen
|
- Trichlorphenylstannan
- Phenyltrichlorstannan
- Trichloridophenylzinn
|
| Summenformel
|
C6H5SnCl3
|
| Kurzbeschreibung
|
farblose bis blassgelbe Flüssigkeit[1]
|
| Externe Identifikatoren/Datenbanken
|
|
|
| Eigenschaften
|
| Molare Masse
|
302,17 g·mol−1
|
| Aggregatzustand
|
flüssig[2]
|
| Dichte
|
1,839 g·cm−3 (25 °C)[2]
|
| Siedepunkt
|
142–143 °C (25 mmHg)[2]
|
| Dampfdruck
|
0,37 hPa (25 °C)[3]
|
| Löslichkeit
|
nahezu unlöslich in Wasser[1] (13,9 g/l bei 25 °C)[3] (5,2 mg/l bei 20 °C)[4]
|
| Brechungsindex
|
1,585 (20 °C)[2]
|
| Sicherheitshinweise
|
|
|
Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet.
Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). Brechungsindex: Na-D-Linie, 20 °C
|
Phenylzinntrichlorid ist eine chemische Verbindung aus der Gruppe der zinnorganischen Verbindungen.
Gewinnung und Darstellung
Phenylzinntrichlorid kann unter anderem durch Reaktion von Zinntetrachlorid mit Tetraphenylzinn gewonnen werden (Kocheshkov-Umlagerung):[5][6]

Eigenschaften
Die physikalischen und chemischen Eigenschaften von Monoarylzinntrihalogeniden, wie Phenylzinntrichlorid, ähneln denen der entsprechenden Zinntetrahalogenide.[5]
Physikalische Eigenschaften
Phenylzinntrichlorid ist durchaus wasserlöslich, wird aber nur wenig hydrolysiert.[5] Es hat einen Flammpunkt von 113 °C.[2] Im 13C-Kernresonansspektrum (NMR) zeigt es folgende Signale:[7]
|
Sn–C1– |
–C2 |
–C3 |
–C4
|
| ppm |
135,8 |
133,9 |
130,3 |
132,9
|
| J(13C–119Sn) |
1120 |
78,8 |
126 |
121
|
Im 119Sn–NMR liefert es ein Signal bei −61,0 ppm. Der Zinn-Kohlenstoff-Abstand in Kristall liegt bei 2,12 Å.[7]
Das Molekül hat ein Dipolmoment von 4.30 Debye.[8]
Chemische Eigenschaften
Wie andere zinnorganische Verbindungen ist Phenylzinntrichlorid eine Lewis-Säure und bildet mit Basen, wie Pyridin, Piperidin, Morpholin oder Anilin entsprechende Addukte, in denen das zentrale Zinnatom sechsfach koordiniert ist.[9]
Durch Umsetzung von Phenylzinntrichlorid mit Diethylaluminiumhydrid in Diethylether kann Phenylzinntrihydrid gewonnen werden:[10]
![{\displaystyle \mathrm {Cl_{3}Sn(C_{6}H_{5})\ +\ 3\ Et_{2}AlH\ {\xrightarrow[{Et_{2}O}]{\ }}H_{3}Sn(C_{6}H_{5})\ \ +\ 3Et_{2}AlCl\ \ \ Et=Ethyl} }](https://wikimedia.org/api/rest_v1/media/math/render/svg/c25d9d6c496b946e5003a9b47ebbe031238756ab)
Einzelnachweise
- ↑ a b
Eintrag zu Phenylzinntrichlorid bei TCI Europe, abgerufen am 19. Oktober 2015.
- ↑ a b c d e f g
Datenblatt Phenyltin trichloride, 98% bei Sigma-Aldrich, abgerufen am 19. Oktober 2015 (PDF).
- ↑ a b
Phenylzinnverbindungen [MAK Value Documentation in German language, 2010]. In: The MAK Collection for Occupational Health and Safety. 31. Januar 2012, doi:10.1002/3527600418.mb240668verd0048.
- ↑
Rita Cornelis, Joseph A. Caruso, Helen Crews, Klaus G. Heumann: Handbook of Elemental Speciation, Handbook of Elemental Speciation II Species in the Environment, Food, Medicine and Occupational Health. John Wiley & Sons, 2005, ISBN 0-470-85599-1, S. 425 (eingeschränkte Vorschau in der Google-Buchsuche).
- ↑ a b c
G. J. M. van der Kerk, J. G. A. Luijten, J. G. Noltes: Neue Ergebnisse der Organozinn-Forschung. In: Angewandte Chemie. Band 70, Nr. 10, 21. Mai 1958, S. 298–306, doi:10.1002/ange.19580701004.
- ↑
Alwyn George Davies: Organotin chemistry. Band 1. Wiley-VCH Verlag GmbH & Co. KGaA, 2004, ISBN 3-527-31023-1 (Seite 167 in der Google-Buchsuche).
- ↑ a b
Cathrin Zeppek, Johann Pichler, Ana Torvisco, Michaela Flock, Frank Uhlig: Aryltin chlorides and hydrides: Preparation, detailed NMR studies and DFT calculations. In: Journal of Organometallic Chemistry. Band 740, September 2013, S. 41–49, doi:10.1016/j.jorganchem.2013.03.012.
- ↑
Jörg Lorberth, Heinrich Nöth: Dipolmomente einiger Organozinnchloride. In: Chemische Berichte. Band 98, Nr. 3, März 1965, S. 969–976, doi:10.1002/cber.19650980342.
- ↑
K. L. Jaura, K. Chander, K. K. Sharma: Addition Compounds of Organotin Halides. V. Adducts of phenyl tin Trichloride with amines. In: Zeitschrift für anorganische und allgemeine Chemie. Band 375, Nr. 1, Juli 1970, S. 107–110, doi:10.1002/zaac.19703750116.
- ↑
Wilhelm P. Neumann, Horst Niermann: Organozinnverbindungen, II. Darstellung von Organozinn-mono-, -di- und -tri-hydriden. In: Justus Liebigs Annalen der Chemie. Band 653, Nr. 1, 24. Mai 1962, S. 164, doi:10.1002/jlac.19626530119.
|




![{\displaystyle \mathrm {Cl_{3}Sn(C_{6}H_{5})\ +\ 3\ Et_{2}AlH\ {\xrightarrow[{Et_{2}O}]{\ }}H_{3}Sn(C_{6}H_{5})\ \ +\ 3Et_{2}AlCl\ \ \ Et=Ethyl} }](https://wikimedia.org/api/rest_v1/media/math/render/svg/c25d9d6c496b946e5003a9b47ebbe031238756ab)