|
Hantzschsche PyrrolsyntheseDie Hantzschsche Pyrrolsynthese (Hantzsch’sche Pyrrolsynthese), auch bekannt als die Hantzsch-Pyrrolsynthese, ist eine Namensreaktion der organischen Chemie. Sie wurde nach dem deutschen Chemiker Arthur Hantzsch (1857–1935) benannt, der sie im Jahre 1890 veröffentlichte.[1] Sie dient zur Synthese von Pyrrol und dessen Derivaten.[2][3][4] Die Reaktion ist mit der Paal-Knorr-Synthese und der Knorr-Pyrrolsynthese verwandt. ÜbersichtWährend der Synthese reagieren β-Ketoester (schwarz) mit einem Amin (blau) und anschließend unter Schließung eines Ringes mit einem α-Halogenketon (grün) zu einem Pyrrolderivat:
Anstelle eines Amins kann auch Ammoniak für die Reaktion verwendet werden. Dann bildet sich ein am Stickstoffatom unsubstituiertes Pyrrolderivat. MechanismusDer Mechanismus wird mit einem allgemeinen β-Ketoester einem α-Halogenketon und einem primären Amin veranschaulicht.
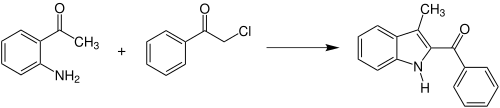
Zu Beginn reagiert der β-Ketoester 1 mit einem primären Amin über mehrere Zwischenstufen zu einem Enamin 2. Dann greift das Enamin im Zuge einer nucleophilen Substitution das α-Halogenketon an und ein Halogenid wird abgespalten. Dieses Halogenid spaltet ein Wasserstoff vom Stickstoff 3 ab und verlässt die Reaktion als Halogenwasserstoff (hier als HX dargestellt). Damit ist ein Imin 4 entstanden, dessen Imingruppe im nächsten Schritt gedreht wird 5. Es folgt eine Isomerisierung des Imins zum Enamin-Tautomer 6. Dann wird das Kohlenstoffatom der Carbonylgruppe 6 von der Aminogruppe angegriffen und damit der Fünfring 7 geschlossen. Nach der Umlagerung eines Protons 7 wird Wasser aus dem Molekül 8 abgespalten. Es entsteht das Produkt 9 in Form eines Pyrrolderivats.[1][5] ModifikationenAnstelle der drei ursprünglichen Edukte kann die Reaktion auch zwischen einem Enamin des β-Ketoester und einem α-Halogenketon durchgeführt werden. Außerdem kann die Reaktion durch die Wahl der Edukte dazu benutzt werden Indol- bzw. Carbazolderivate zu synthetisieren.[1] So reagieren beispielsweise o-Aminoacetophenon und α-Chloracetophenon zu 2-Benzoyl-3-methyl-indol:[1][6] Einzelnachweise
|