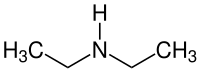
Strukturformel
Allgemeines
Name
Diethylamin
Andere Namen
Summenformel
C4 H11 N
Kurzbeschreibung
farblose, leichtentzündliche Flüssigkeit mit aminartigem Geruch[ 1]
Externe Identifikatoren/Datenbanken
Eigenschaften
Molare Masse
73,14 g·mol−1
Aggregatzustand
flüssig
Dichte
0,71 g·cm−3 [ 1]
Schmelzpunkt
−50 °C [ 1]
Siedepunkt
56 °C[ 1]
Dampfdruck
256 hPa (20 °C)[ 1]
392 hPa (30 °C)[ 1]
581 hPa (40 °C)[ 1]
838 hPa (50 °C)[ 1]
pK S -Wert
10,98 (protoniert)[ 2] [ 3]
Löslichkeit
vollständig mischbar mit Wasser[ 1]
Brechungsindex
1,3864[ 4]
Sicherheitshinweise
MAK
DFG /Schweiz: 5 ml·m−3 bzw. 15 mg·m−3 [ 1] [ 6]
Toxikologische Daten
540 mg·kg−1 (LD50 , Ratte , oral )[ 4]
Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet.Standardbedingungen (0 °C, 1000 hPa). Brechungsindex: Na-D-Linie , 20 °C
Diethylamin ist eine chemische Verbindung aus der Gruppe der aliphatischen sekundären Amine .
Gewinnung und Darstellung
Diethylamin kann durch Reaktion von Ethanol mit Ammoniak gewonnen werden, wobei auch Ethylamin und Triethylamin entstehen.
Eigenschaften
Die wässrige Lösung von Diethylamin reagiert stark alkalisch . Ab etwa 500 °C zersetzt sich Diethylamin.[ 1] Viskosität von 0,34 mPa·s bei 25 °C.[ 4]
Sicherheitstechnische Kenndaten
Diethylamin bildet mit Luft leicht entzündliche Dampf-Luft-Gemische. Die Verbindung hat einen Flammpunkt unterhalb von −20 °C.[ 1] Explosionsbereich liegt zwischen 1,7 Vol.‑% (50 g/m3 ) als untere Explosionsgrenze (UEG) und 10,1 Vol.‑% (305 g/m3 ) als obere Explosionsgrenze (OEG).[ 1] [ 7] Grenzspaltweite wurde mit 1,15 mm (50 °C) bestimmt.[ 1] Explosionsgruppe IIA.[ 1] [ 7] Zündtemperatur beträgt 305 °C.[ 1] [ 7] Temperaturklasse T2.
Verwendung
Diethylamin wird zur Herstellung von Kautschuk -, Textil-, Flotationschemikalien , von Kunstharzen, Farb- und Arzneistoffen, Insektiziden , galvanischen Bädern und Polymerisationsverzögerern sowie als pH-Wert -Regler und Puffersubstanz verwendet. Es kann auch zur Herstellung des Nervengiftes Tabun verwendet werden[ 8] [ 9]
Supramolekulare Struktur
Supramolekulare Helix Diethylamin ist das kleinste und einfachste Molekül das eine supramolekulare Helix als Aggregat mit niedrigster Energie aufweist. Andere ähnlich kleine wasserstoffverbrückte Moleküle bevorzugen zyklische Strukturen.[ 10]
Verwandte und abgeleitete Verbindungen
Einzelnachweise
↑ a b c d e f g h i j k l m n o p q r Eintrag zu Diethylamin GESTIS-Stoffdatenbank des IFA , abgerufen am 3. Januar 2023.
↑ H. K. Hall: Correlation of the Base Strengths of Amines. In: Journal of the American Chemical Society. 79, 1957, S. 5441, doi :10.1021/ja01577a030
↑ Steven Pedersen: Understanding the Principles of Organic Chemistry: A Laboratory Course. Cengage Learning, 2010, ISBN 978-0-495-82993-5 , S. 23 (eingeschränkte Vorschau in der Google-Buchsuche).
↑ a b c Datenblatt Diethylamin Merck , abgerufen am 21. Januar 2011.
↑ Eintrag zu Diethylamine Classification and Labelling Inventory der Europäischen Chemikalienagentur (ECHA), abgerufen am 1. Februar 2016. Hersteller bzw. Inverkehrbringer können die harmonisierte Einstufung und Kennzeichnung erweitern .
↑ Schweizerische Unfallversicherungsanstalt (Suva): Grenzwerte – Aktuelle MAK- und BAT-Werte 109-89-7 ), abgerufen am 30. Dezember 2024.↑ a b c Sorbe - Sicherheitstechnische Kenndaten chemischer Stoffe, 131. Ergänzungslieferung 8/2009, ecomed-Verlag.
↑ Robert Turkington: Chemicals Used for Illegal Purposes . John Wiley & Sons, 2009, ISBN 978-0-470-18780-7 , S. 324 (books.google.de ).
↑ Daniel Savi, Ueli Kasser, Rolf Widmer: Flüssigkeiten in Kondensatoren - Bestimmung von Flüssigkeiten in elektrischen Kondensatoren mit Definition und Zuordnung von bedenklichen Stoffen - Schlussbericht. swico.ch. 6. Mai 2019, S. 48 , abgerufen am 14. September 2020 . ↑ Felix Hanke, Chloe J. Pugh, Ellis F. Kay, Joshua B. Taylor, Stephen M. Todd, Craig M. Robertson, Benjamin J. Slater, Alexander Steiner: The simplest supramolecular helix . In: Chemical Communications Band 54 , 2018, doi :10.1039/C8CC03295E
↑ Externe Identifikatoren von bzw. Datenbank-Links zu Diethylammoniumbromid : CAS-Nr. : 6274-12-0 EG-Nr. : 228-466-2, ECHA -InfoCard: 100.025.879 , PubChem : 22665 Wikidata : Q82860734 .
↑ Externe Identifikatoren von bzw. Datenbank-Links zu Diethylaminsalicylat : CAS-Nr. : 4419-92-5 EG-Nr. : 224-586-4, ECHA -InfoCard: 100.022.353 , PubChem : 9837223 , ChemSpider : 19278 , Wikidata : Q27262917 .
↑ Externe Identifikatoren von bzw. Datenbank-Links zu Diethylammoniumacetat : CAS-Nr. : 20726-63-0 EG-Nr. : 243-990-1, ECHA -InfoCard: 100.039.976 , PubChem : 167925 Wikidata : Q81993222 .