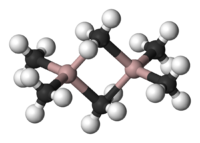
三甲基铝
IUPAC名
识别
CAS号
75-24-1 Y
PubChem
16682925
ChemSpider
10606585
SMILES
InChI
1/3CH3.Al/h3*1H3;/rC3H9Al/c1-4(2)3/h1-3H3
InChIKey
JLTRXTDYQLMHGR-MZZUXTGEAJ
性质
化学式
C6 H18 Al2
摩尔质量
144.17 g/mol3 H9 Al) g·mol⁻¹
外观
无色液体
密度
0.752 g/cm3
熔点
15 °C(288 K)
沸点
125 °C(398 K)([ 1] [ 2]
溶解性 (水 )
与水反应
蒸氣壓
1.2 kPa (20 °C)[ 1]
黏度
1.12 cP (20 °C)
热力学
Δf H m ⦵ 298K
−136.4 kJ/mol[ 2]
S ⦵ 298K 209.4 J/mol·K[ 2]
热容
155.6 J/mol·K[ 2]
危险性
警示术语
R:R14 R17 R34
安全术语
S:S16 S43 S45
欧盟分类
F C
GHS危险性符号 [ 1]
GHS提示词
危险
H-术语
H250 , H260 , H314 [ 1]
P-术语
P222 , P223 , P231+232 , P280 , P370+378 , P422 [ 1]
主要危害
自燃性
NFPA 704
若非注明,所有数据均出自标准状态(25 ℃,100 kPa) 下。
三甲基铝 是一个化合物 ,化学式是Al 2 (CH3 )6 , 可以缩写为Al2 Me6 , (AlMe3 )2 或者TMA。它是一种自燃 的无色液体,在工业上是很重要的有机铝化合物 。它的蒸气散发到空气中后会产生白烟(氧化铝 )。
Al2 Me6 在常温常压下是二聚体 [ 3] 乙硼烷 相似。像乙硼烷一样,这个化合物同样有两个三中心两电子键 :在两个铝原子之间有一个共用的甲基。端位的Al-C键和中间的Al-C键的距离分别是1.97和2.14埃 [ 4]
三中心两电子键是"缺少电子"的分子而且倾向于与路易斯碱 反应,产物含有两中心两电子键。例如和氨 反应生成加合物 R3 N-AlMe3 。Al2 Me6 与氯化铝 反应生成的(AlMe2 Cl)2 是另一个遵守八隅体规则 的反应产物。
AlMe3 的单体含有一个铝 原子 和三个甲基 ,这种单体仅会在高温低压下存在[ 3] VSEPR理论 预言了它如同BMe3 一样是三角平面(有一个三重轴 )对称 。后来电子衍射 的结果也证实了这个预言。[ 5]
TMA可以通过两步反应制取,总反应式如下:
2 Al + 6 CH3 Cl + 6 Na → Al2 (CH3 )6 + 6 NaCl TMA主要用来生产甲基铝氧烷 ,用于活化烯 烃 聚合的齐格勒-纳塔催化剂 。TMA也作为甲基化试剂。用于亚甲基酯 和酮 的Tebbe试剂 就是由TMA制备的。TMA也用在探空火箭 上,用作研究上层大气风模式的示踪剂 。
通过化学气相沉积 或原子层沉积 过程,TMA也可用于制造半导体 的沉积高介電係數 电介质 薄膜 ,例如Al2 O3 。
TMA与叔胺 DABCO 形成化合物,这比直接处理TMA本身更安全[ 6]
在Cp2 ZrCl2 (二氯二茂锆)的催化 下,(CH3 )2 Al-CH3 能够与炔烃反应生成烯基铝,这个反应在被称为carboalumination的有机合成 反应中起作用[ 7]
NASA 的ATREX任务利用TMA与空气接触产生的白烟研究高空急流。
TMA是有机金属化学气相沉积法 (MOVPE)制造含铝半导体 (如AlAs , AlN , AlP , AlSb , AlGaAs , AlInGaAs , AlInGaP , AlGaN , AlInGaN , AlInGaNP 等)中有机金属 的重要来源。TMA的质量标准主要关注元素杂质、氧化杂质和有机杂质的含量。
^ 1.0 1.1 1.2 1.3 1.4 来源:Sigma-Aldrich Co., Trimethylaluminum (2014-05-05查阅).
^ 2.0 2.1 2.2 2.3 http://chemister.ru/Database/properties-en.php?dbid=1&id=3290 (英文) ^ 3.0 3.1 Carlsson, J.; Gorbatkin, S.; Lubben, D.; Greene, J. E. Thermodynamics of the homogeneous and heterogeneous decomposition of trimethylaluminum, monomethylaluminum, and dimethylaluminumhydride: Effects of scavengers and ultraviolet-laser photolysis. Journal of Vacuum Science and Technology B. 1991, 9 (6): 2759–2770. doi:10.1116/1.585642 ^ Holleman, A. F.; Wiberg, E. Inorganic Chemistry. San Diego: Academic Press. 2001. ISBN 0-12-352651-5 ^ Almennin, A.; Halvorse, S.; Haaland, A. Gas Phase Electron Diffraction Investigation of Molecular Structures of Trimethylaluminum Monomer and Dimer. Acta Chemica Scandinavica. 2005, 44 (15): 2232–2234. doi:10.3891/acta.chem.scand.25-1937 ^ Biswas, K.; Prieto, O.; Goldsmith, P. J.; Woodward, S. Remarkably Stable (Me3 Al)2 · DABCO and Stereoselective Nickel-Catalyzed AlR3 (R = Me, Et) Additions to Aldehydes. Angewandte Chemie International Edition . 2005, 44 (15): 2232–2234. PMID 15768433 doi:10.1002/anie.200462569 ^ Negishi, E.; Matsushita, H. (1984). "Palladium-Catalyzed Synthesis of 1,4-Dienes by Allylation of Alkenyalane: α-Farnesene [1,3,6,10-Dodecatetraene, 3,7,11-trimethyl-] ". Org. Synth. 62 : 31; Coll. Vol. 7 : 245.