|
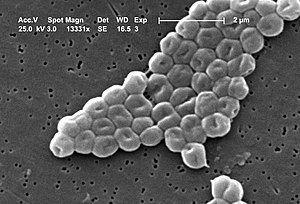
AcinetobacterАцинетобактерії (Acinetobacter, від грец. α- — «не», κίνησις — «рух», βακτήριον — «щось маленьке», пізніше — «бактерія» — тобто «нерухома бактерія») — рід грам-негативних бактерій класу гамма-протеобактерій. Представники роду нерухомі, негативні на оксидазу та зазвичай спостерігаються парами. Ці бактерії — важливі організми ґрунту, важливі гравці у мінералізації таких речовин як ароматичні сполуки. Також бактерії Acinetobacter є відносно частим збудником опортуністичних інфекцій у лікарнях[1], харчових отруєнь і діареї мандрівників. Ацинетобактерії утворюють дрібні (1,0-1,5 × 1,5-2,5 мкм), капсульні нерухомі палички, на що прямо вказує їхня назва [від грец. а-, відмова, + kinesis, рух, + bakter бактерія]. В мазках розташовуються парами, короткими ланцюжками або безладними скупченнями. Джгутиків не мають, але завдяки наявності полярних фімбрій на щільних середовищах для бактерій характерна псевдорухливість. Добре ростуть на звичайних середовищах, утворюючи колонії, що нагадують колонії ентеробактерій. Середовище існування Ацинетобактерії широко поширені в природі, їх виділяють з води, ґрунту, пастеризованого молока, заморожених продуктів, а також з повітря стаціонарів і змивів з різного медичного обладнання, розчинів і препаратів (в тому числі крові).[2] Їхня здатність виживати на вологих і сухих поверхнях, а також витримувати вплив різних поширених дезінфекційних засобів дозволяє деяким видам ацинетобактерій виживати в лікарняних умовах.[2] Крім того, багато які види ацинетобактерій можуть рости в широкому діапазоні температур, що дозволяє їм виживати в найрізноманітніших середовищах.[2] Вони виявлені на шкірних покривах 25% клінічно здорових людей (особливо медичного персоналу), а також на слизовій оболонці носогорла (понад 7% обстежених індивідуумів). У здорових людей наявність колоній ацинетобактерій на шкірі корелює із низькою частотою випадків алергії;[3] Вважається, що ацинетобактерії захищають від алергії.[4] Ацинетобактерії часто виділяють при ураженнях шкірних покривів, дихальних шляхів (наприклад, позитивні результати отримані у 45% пацієнтів з трахеостомії), сечовивідного тракту і статевих органів, при кон'юнктивітах, а також ендокардитах, менінгітах, перитонітах і септицемія. Ацинетобактерії — другі (після псевдомонад) по частоті виділення з клінічних зразків неферментуючі грамнегативні палички. Останнім часом реєструють збільшення частоти внутрішньолікарняних інфекцій, викликаних ацинетобактеріями, у пацієнтів з порушеннями імунітету, які важко піддаються лікуванню (становлять 5-25% всіх внутрішньолікарняних інфекцій). Патогенез уражень ацинетобактеріями Прямо пов'язаний з порушеннями імунітету, оскільки ацинетобактерії позбавлені будь-яких факторів патогенності, за виключенням ліпополісахаридів клітинної стінки. Капсула пригнічує ефективність фагоцитарних реакцій і полегшує адгезію до епітелію, а здатність до секреції бактеріоцинів полегшує його колонізацію. Принципи мікробіологічної діагностики При розпізнаванні ацинетобактерій слід пам'ятати, що в мазках з нативного матеріалу домінують кокові та кокобацилярні, а в мазках із культур — паличкоподібні форми. Мікроорганізми ростуть на простих середовищах, утворюючи блискучі блакитні колонії. На КА через 48 год формують опуклі сірувато-білі колонії (2-3 мм), іноді оточені зоною гемолізу. ЛікуванняАцинетобактерії мають природну стійкість до багатьох класів антибіотиків, включаючи пеніцилін, хлорамфенікол, і часто до аміноглікозидів. Повідомлялося про резистентність до фторхінолонів під час терапії, що також призводило до підвищення резистентності до інших класів препаратів через активне виведення (ефлюкс) лікарських засобів з клітин цих бактерій. Центри з контролю та профілактики захворювань США (CDC) повідомили про різке підвищення стійкості різноманітних штамів ацинетобактерій до антибіотиків, і карбапенеми визнані золотим стандартом лікування останньої надії.[5] Ацинетобактерії незвичайні тим, що вони чутливі до сульбактаму, який зазвичай використовується для пригнічення бактеріальної бета-лактамази, але це приклад антибактеріальних властивостей самого сульбактаму.[6] Нещодавно сульбактам-дурлобактам, нове антибактеріальне поєднання, яке проходить третю фазу випробувань, показало гарну активність in vitro у тому числі проти резистентних до карбапенему ізолятів A. baumannii (чутливість 92%).[7] У листопаді 2004 року Центри з контролю та профілактики захворювань США (CDC) повідомили про зростання кількості випадків зараження крові A. baumannii у пацієнтів військових госпіталів, в яких лікувалися військовослужбовці, поранені в Іраку та Кувейті під час операції «Іракська свобода» та в Афганістані під час операції «Нескорена свобода».[8] Більшість з цих випадків були стійкими до багатьох лікарських засобів. В одній з вибірок ізолятів з армійського медичного центру Уолтера Ріда 13 (35%) були чутливі лише до іміпенему, а два (4%) були стійкі до всіх протестованих препаратів. Для лікування інфекцій, спричинених штамами A. baumannii зі стійкістю до багатьох антибіотиків, використовувався один антимікробний препарат - колістин (поліміксин Е); однак тестування на чутливість до колістину для ізолятів, описаних у цьому звіті, не проводилося. Оскільки A. baumannii можуть виживати на сухих поверхнях до 20 днів, вони становлять високий ризик поширення та зараження в лікарнях, потенційно наражаючи пацієнтів з ослабленим імунітетом та інших пацієнтів на ризик розвитку стійких до ліків інфекцій, які часто є смертельними та зазвичай дорогими в лікуванні. Були задокументовані випробування вакцин для профілактики інфекцій, спричинених ацинетобактеріями.[9][10] Повідомляється, що ця бактерія чутлива до фагової терапії.[11] Також повідомлялося, що антисенсорні олігомери, що пригнічують гени, а саме пептидно-кон’юговані фосфородиамідат-морфолінові олігонуклеотиди, пригнічують ріст ацинетобактерій у тестах, проведених на тваринах, інфікованих стійкими до антибіотиків штамами A. baumannii.[12][13] Поєднання сульбактам/дурлобактам (Xacduro) було схвалено для медичного використання в Сполучених Штатах у травні 2023 року.[14] Метод запобігання поширенню інфекціїВелика кількість внутрішньолікарняних інфекцій у британських лікарнях спонукала британську Національну службу охорони здоров’я дослідити дієвість аніонів в очищенні повітря, і виявилось, що повторні повітряно-крапельні інфекції ацинетобактеріями у палатах успішно усувалися шляхом встановлення негативного іонізатора повітря — завдяки йому рівень інфекцій впав до нуля.[15][16] Така дієвість пояснюється не бактерицидним впливом аніонів, а впливом озону[17] та тим, що аніони негативно заряджають поверхні пластикового медичного обладнання, завдяки чому вони відштовхують, а не притягують бактерії, що переносяться повітрям.[18] Зовнішні посилання
Виноски
|